
【ドラッグデリバリーシステム】鉱物とタンパクで薬を届ける
医療やヘルスケアに興味がある方は聞いたことがあると思いますが、最近ドラッグデリバリー技術がとても注目されています。
ドラッグデリバリーとはその名の通り、薬を患部まで届ける技術です。通常Drug Delivery System(DDS)といわれており、副作用が出やすいがんをはじめとした治療に期待されています。
今回紹介するのはこのドラッグデリバリーシステムの論文です。
私自身、この分野はド素人ですので、感想多めのふわっとした紹介になりますが、ドラッグデリバリーについて見ていきましょう。
一般的なドラッグデリバリーシステム
ドラッグデリバリーシステムの基本的な考え方は、誰でもわかる簡単なものです。
副作用がきつい抗がん剤などの強めの薬を目にも見えないぐらい小さなカプセルなんかに入れて、患部まで届けます。そして患部に届いたところでカプセルが開いて、中から薬が出てきて治療するという流れなんですね。
そもそも副作用は正常な細胞に影響を与えてしまうため起こるわけなので、病気の原因のみをピンポイントでアタックすれば副作用を減らすことができるということです。
ここで重要になってくるのが、薬を体内の所定の位置まできちんと届けないといけないので、どうにかして操作してやらなければなりません。
自動で患部に集まるような仕組みにするのか、それとも外からコントロールしてやるのかいろいろな方法が試されています。
そしてもう1つ重要なことはきちんと患部で中から薬が出てくるのかということです。せっかく届いた宅配もダンボールが開かなかったらどうしようもないのと同じです。
鉱物とタンパクを使った新しいタイプのDDS
ようやく本題になりますが、今回は上記の2つの課題、①正確に患部に届ける方法と、②正確に中から薬が出てくる仕組みを小さな粒子で実現した論文の1つになります。
まず、今回使用されたドラッグデリバリーの粒子は炭酸カルシウムと酸化鉄を中心にして、その表面にタンパク質とタンニンが覆っているようなコアシェル構造の粒子です。
コアになるの鉱物(いわば小さな石ころ)とシェルになるやわらかいタンパク質の組み合わせによってできた新たなタイプのドラッグデリバリーシステムです。
ここで、よくわからないのが鉱物である炭酸カルシウム(CaCO3)と酸化鉄(Fe3O4)というところですよね。下の図を見るとわかるように、この2つはスケール感が違います。

炭酸カルシウムの母体(灰色)の中に小さな酸化鉄ナノ粒子(赤茶色の粒)が含まれているという状況のようです。
どうやらこのような組み合わせで作ると、通常数マイクロメートルの高分子粒子よりも小さく設計することができるとのことです。
磁力によって患部に届ける
まずは1つ目の課題、患部にどうやって届けるのかというところですが、この小さな酸化鉄ナノ粒子が重要な役割を果たします。
実は、酸化鉄ナノ粒子は磁石に引き寄せられる性質を持っています。正しくは磁界という磁石の影響を受けるとそれに従って動くんです。
この性質を使うことで、自由に患部まで届けけられると論文ではいっています。実際いろいろな課題がありそうですが、基礎研究なのでここはそっとしておきましょう。
酵素を使って薬を放出
そして2つ目のポイントが正しく薬を放出できるのか? ?という点です。現在、1種のドラッグデリバリーシステムでは、酵素を使って粒子を溶かして中から薬を放出させる方法がとられているようです。
この研究グループも、同様にトリプシンという酵素を使うときれいに薬を放出できることを確かめています。当然、論文中では他にも様々な酵素や緩衝液を使って、その放出具合を見ています。
ただ、ここで1つ疑問になるのがこんな複雑なものが本当に治療に役立つのか?というところですよね。なんだか、すごそうなのはわかったけれど、それってホントに意味あるの? という問いにも答えています。
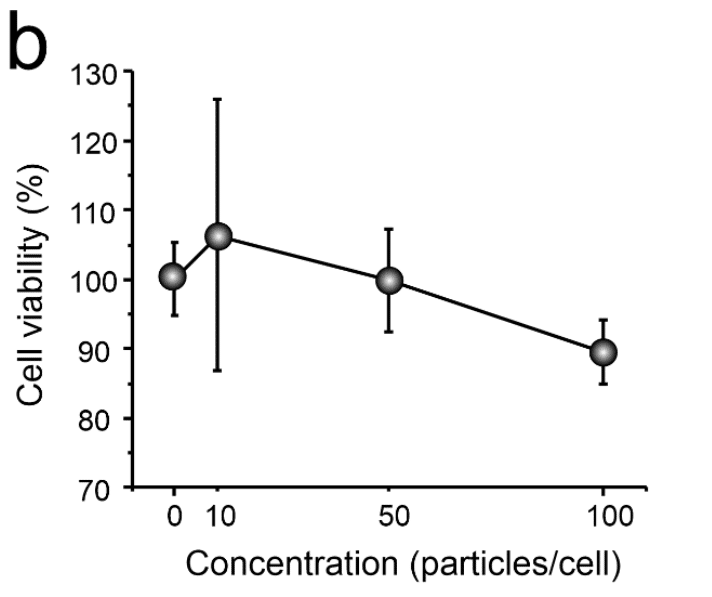
実際に 、研究グループが作製したドラッグデリバリーシステムを使って標的であるがん細胞に使用しました。すると、がん細胞の増殖を抑制することができました。
最後に
今回は、1例としてドラッグデリバリーシステムの論文を紹介してみました。読んでいると酵素とか細胞とか私の全くわからない分野の言葉がたくさん出てきて、勉強が足りないな…と感じました。
もし間違ってるところなどがありましたら優しく指摘してもらえると嬉しいです。
そして、これはあくまで1例ですので、世の中にはこのようなドラッグデリバリーシステムの研究は山のようにされています。常に製品がアップデートされるように、基礎技術も少しずつ研究が進められてより良いものになっていくでしょう。
参考文献
Degradation of Hybrid Drug Delivery Carriers with a Mineral Core and a Protein–Tannin Shell under Proteolytic Hydrolases
