
1-2. 原子の構造
こんにちは。おのれーです。
前回は「原子」とはどのようなものなのかを見てきました。今回は、もう少し深く突っ込んで、原子の構造について見ていきたいと思います。
■原子はどのような構造をしているのか?
原子は物質をつくる最小の粒子です。原子説を唱えたドルトンも、「それ以上分割することはできない」と言っているので、「原子に中身なんてあるの??」と思うかもしれません。
でも、あるんです。原子の中身。
生物のからだをつくる最小単位である「細胞」の中にも、「核」「ミトコンドリア」「ゴルジ体」などのさまざまなパーツが含まれています。同じように原子もいくつかのパーツでできています。
具体的には、「陽子」「中性子」「電子」という3種類のパーツが原子にはあります。
陽子は、プラスの電荷(正電荷)をもつ粒子であり、中性子は、電荷をもたない(電気的に中性)粒子です。この2種類の粒子は原子の中心に存在していて、その粒子のかたまりのことを「原子核」とよんでいます。
原子核はとても小さく(直径約0.000000000000001 m)、原子の大きさ(直径約0.0000000001 m)を野球場くらいの大きさ(直径約200 m)とすると、原子核の大きさはマウンドの砂粒くらいの大きさ(直径約2 mm)に相当します。

一方、電子はマイナスの電荷(負電荷)をもつ粒子です。電子は、とても軽い粒子であり、原子核のまわりをものすごい速さで飛び回っています。"原子の大きさ"といわれたら、この電子が飛び回れる空間の大きさと考えてもよいでしょう。
まとめると、次のようになります。

■原子の質量はどのように表せばよいか?
原子はそれ自体が小さく、軽い(質量が小さい)粒子ですが、原子を構成する粒子の質量には次のような関係があります。
陽子1個の質量 ≒ 中性子1個の質量 ≒ 電子1840個の質量
仮に体重が50 kgだとしたら、その1840分の1はたった27 g、だいたい水大さじ2杯分です。体重計も認識してくれないほど小さな量ですよね。
そう考えると、電子って、めちゃくちゃ軽いんですね。
だから、自由に飛び回っていられるのかも・・・
つまり、原子の質量は原子核にかたよっているといえるので、
原子の質量 ≒ 原子核の質量
と考えることができます。
ということで、ちょっとざっくりすぎるのですが、原子の質量の目安として、原子核に含まれている陽子数と中性子数の和を「質量数」とし、"原子の質量は質量数に比例する"と考えます。
陽子の数+中性子の数=質量数
■原子全体の電荷はどうなっている?
原子には、正電荷をもつ陽子と負電荷をもつ電子が含まれていますが、原子全体の電荷はどうなっているのでしょうか?
もし、原子が電荷をもっていたら?
何を触っても、そこら中でバチッ!!と感電してしまうはずです。私たちがものを触っても平気なのは(静電気の季節は除く)、原子全体では電荷をもっていない(電気的に中性である)からです。
原子が電気的に中性であるためには、原子に含まれる正電荷と負電荷が攣り合っている必要があります。陽子の持つ正電荷の大きさと、電子の持つ負電荷の大きさの絶対値は同じですので、電荷を打ち消すためには、陽子の数と電子の数は等しくなる必要があります。
また、原子核に含まれる陽子の数は元素ごとに決まっているので、同じ元素の原子であれば、次のような関係が成立します。
陽子の数=電子の数=原子番号 (その元素を特徴づける番号)
■原子に含まれるパーツを記号で表すときには?
今回出てきた「陽子」「中性子」「電子」が原子の中にいくつずつ含まれているかは、次のように表します。

中性子数は、質量数から陽子数(原子番号)を引けば求められるので、元素記号の左側に書いてある上の数字から下の数字を引けばいいと覚えておくと便利です。
今回はここまでです。ちょっと数字が出てきたりしてややこしいかもしれませんが、試験でもよく聞かれるところでもあるので、確認しておきましょう。
最後にワンポイントチェック
1.原子を構成する3つのパーツの名称と電荷は?
2.質量数とはどんなもの?どうやって求める?
3.原子番号とはどんなもの?どうやって求める?
4.次の記号で表される原子の元素名、質量数、原子番号、中性子数を求めてみよう。
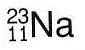
さて、次回は原子の質量に注目をしていきます。お楽しみに!
この記事が気に入ったらサポートをしてみませんか?
