
上位・最上位高校受験の常識~理科編~#2化学の計算
はじめに
中学生の理科なんて暗記科目だと思っていませんか?そう思っている方々に朗報です。理科は計算がすべてです。
しかし、中学校の授業は語句の紹介が主であまり計算を扱いません。それではダメなんです。上位・最上位高校の入試問題を解くことはできません。今から、そんな「計算の理科」について詳しくお伝えします。
読む時間がない人は問題だけ見てもらって構いません。
「計算の理科」…具体的には?
理科の計算といっても
・物理の計算
・化学の計算
・地学の計算
・生物の計算
この4種類があります。え?生物と地学では計算じゃなく暗記がメインだろって?大部分ではそうでしょう。しかし、この記事を読む中学生が受けるような上位・最上位高校では暗記部分「知識」は常識です。つまり暗記で差はつきません。
計算で差がつくのです。
この記事ではその4種類の中でも化学の計算に関する学習するべき内容、勉強方法などについて、説明します。他の3種類の計算について知りたい方は以下の記事をご覧ください。
上位・最上位高校受験の常識~理科編~
物理の計算
地学の計算
coming soon
生物の計算
soming soon
化学の計算とは?
化学の計算といえば、化学反応の計算です。
化学反応の計算で大切なのは、
原子の個数の比 原子量
を考えることです。ちなみに、これは高校化学で習うmolの概念を簡単にとらえたものです。詳しくは高校までお楽しみ、、、
原子量とは、原子の単位量あたりの重さです。例えば、H=1、O=16、C=12みたいなものです。
化学計算のツール
何も知らなくては化学計算はできません。先ほど、材料としての「個数の比」というのを紹介しました。材料を調理するための道具として、
・アボガドロの法則
・質量保存の法則
・定比例の法則
が必要となってきます。
アボガドロの法則
アボガドロの法則は以下の通りです。
すべての気体は、同温・同圧の同体積中に同数の気体分子を含む。
つまり、同じ気体分子の量ならば、それらの気体の体積は同じということです。発展させると、
気体の反応において、
化学反応式での分子の係数比=体積比
こんな例を考えてみましょう。

この反応は、メタンの燃焼ですね?
この反応の時、水も気体だとすると、体積比は、
CH₄ : O₂ : CO₂ : H₂O = 1:2:1:2
となります。
質量保存の法則
これは中学校の授業でも習うほど有名な法則なので、大丈夫ですね
定比例の法則
定比例の法則は以下の通りです。
化合物を構成する元素の質量比は一定である。
この法則は一見すると当たり前のことのように見えますが、上で紹介した原子量と組み合わせることで、化学計算がただの作業と化します。
例えば、またさっきの例
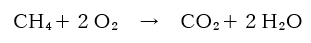
を考えてみましょう。C=12 H=1 O=16 という重さを原子一つ当たり持っています。(実際は1mol=6.0×10²³個あたり)
この時、 CH₄=12+4×1=16
O₂=32
CO₂=44
H₂O=18
と置けます。←この時定比例の法則をつかっている
※左辺=16+64=44+36=右辺と質量保存の法則が成立している。

こう置いたことで、以下のような問題が瞬殺できます。
問題
酸素16グラムを完全に反応させたときにでる二酸化炭素の量は??
答え:
質量で、酸素O₂:二酸化炭素CO₂=64:44より、
CO₂=11g
高校受験の問題では、実験によって完全に反応する質量比を自分で建てて、(Cu:O₂=4:1 やCu:H₂=8:1など)計算していくのですが、これらの比も、Cu=64という情報があれば自分で建てることができます。
実験の値から求めてもいいのですが、器具の重さを引いたり比例の関係がどうとか非常に面倒くさいですよね。高校理科に感謝!!
もちろん、実験から値を求めることのほうが大事です。なぜなら原子量を一つ一つ覚えないといけないからです。

これに加えて、Al=27も必要ですね。
問題演習 灘
最後は、灘高校の問題で終わりましょう。ちなみに、原子量はH=、C=12、 O=16、Cl=35.5、Ca=40

答え:
CaCO₃+2HCl=CaCl₂+CO₂+H₂Oだから、
100 :73 :111 :44:18
(1)CO₂=39.6gだから、CaCO₃=xgとして
CaCO₃:CO₂=100:44=x:39.6
これを解くとx=90
よって、石灰石100gの中に、CaCO₃90gが含まれているから、90%
(2)加熱して残るのは、不純物とCaCl₂だから、
不純物10g+CaCl₂99.9g=109.9g(※100:111=90:y)
どうでしょうか?解けましたか??
この問題、実は高校の定期テストででるレベルの問題です。
解けた人は灘に受かれるんだという自信をもって、解けなかった人も高校範囲なんだと落ち込まずに勉強に励んでいってください。
化学計算問題集のすゝめ
この系統の問題の演習をしたい人には、
・最高水準理科中3 =結構標準レベル
・洛南、灘の過去問 =ほぼ毎年出るからやってもいい。洛南<<<灘
がおすすめです。
灘の過去問をやる人へ
計算問題の最後の問題は解けても解けなくてもいいです。むずすぎます。
メルカリで安く買えます。
まとめ
化学の計算において重要なのは、原子量と原子の個数
これを極めると、ほとんどの化学計算の問題が解けるようになります。ぜひ化学の計算を極めてください!!
written by いますがり
ライター紹介
いますがり
地元の公立中学校からきた数学が好きな現役高校生。好きな数学の単元は関数。最近の趣味は関数グラフで遊ぶこと。最近地学に浮気してるかも,,,
受験の朋(じゅけんのとも)
現役高校生が立ち上げた、高校受験を経験することで得た、上位高校に合格するために必要な情報(ノウハウ)を共有するためのウェブメディア。現在メンバーは6人(2024/10/16現在)
ツイッター(じゅけともメンバーが思ったことを自由に投稿)
受験の朋【高校受験】(@jukennotomo)さん / X
アメブロ(基本的にnoteと同内容)https://ameblo.jp/juketomo/entrylist.html
公式LINE(質問・リクエスト・連絡など)
https://lin.ee/mr7pFzy
受験の朋では一緒に活動してくれる高校生を募集しています!ぜひ気軽にご応募ください。現在は4つの高校の生徒がともに活動を行っております。
応募・詳細は下のリンクからお願いします。
この記事がいいなと思ったら下のハートマークを押して評価をお願いします!!活動の励みになります!
