
6 単一遺伝子欠損と自己炎症:ループスとの関連 Single Gene Defects and Autoinflammation Relation to Lupus
Dubois' Lupus Erythematosus and Related Syndromes, Tenth Edition
Pearl:単発性自己免疫疾患および自己炎症性疾患(単一遺伝子性の全身性エリテマトーデスを含む)は、I型インターフェロン(IFN)系の調節異常を特徴とするインターフェロン異常症に分類される
comment:Monogenic autoimmune and autoinflammatory disorders (including monogenic systemic lupus erythematosus [SLE]) are classed as interferonopathies, a complex group of genetic disorders that are characterized by dysregulation of the type I interferon (IFN) system
・SLEは典型的なインターフェロン(IFN)依存性疾患である。SLE患者の約40%から50%は、血清IFNが上昇するか、全血または末梢血単核球(PBMC)中のIFN刺激遺伝子(IFN-stimulated genes:ISG)の発現が増加し、疾患活動性と正の相関を示す。
・抗原提示分子のアップレギュレーション、共刺激受容体、細胞傷害性T細胞やナチュラルキラー(NK)細胞のプライミングと活性化、自己抗体産生などが含まれ、これら全てが自己反応性B細胞やT細胞を活性化し、抑制性T細胞を減少させ、最終的には自己免疫によりSLE患者の細胞や組織を破壊する。
・核酸感知異常がSLEにおけるIFN誘導と病態の一因であることが広く認識されているように、インターフェロン異常症を引き起こす変異は、細胞が自己の核酸を除去する能力に影響を与えるか、あるいは細胞質の核酸感知を制御するタンパク質をコードする遺伝子に影響を与えるかのいずれかである。
Pearl:パターン認識受容体(PRR)であるトール様受容体(TLR)3、7、9は、それぞれ二本鎖(ds)RNA、一本鎖(ss)RNA、DNAを認識するように進化してきた
comment:The pattern recognition receptors (PRRs) toll-like receptor (TLRs) 3, 7, and 9 have evolved to recognize double-stranded (ds)RNA, single-stranded (ss) RNA and DNA,respectively.
・I型IFN(IFN-I)には、IFN-α(13のアイソフォームが同定されている)とIFN-βのサブタイプがある。両者ともIFNAR1とIFNAR2のIFN受容体複合体に結合し、JAK/STAT経路の活性化を通じてシグナル伝達カスケードを開始し、最終的にISGの発現を誘導する。
・IFN-I誘導は、ウイルス性、細菌性、自己の核酸など、核酸センシングに大きく反応する。パターン認識受容体(PRR)であるトール様受容体(TLR)3、7、9は、それぞれ二本鎖(ds)RNA、一本鎖(ss)RNA、DNAを認識するように進化してきた。これらは主に免疫細胞で発現し、エンドソームに位置し、内在化したRNAやDNAに反応する。

https://www.igm.hokudai.ac.jp/sci/files/innate_virus.pdf
・抗マラリア薬であるヒドロキシクロロキンは、主に②エンドソーム内で酸依存性のTLRの活性化の抑制と、③核酸エピトープに結合して、TLRに結合・刺激するのを阻害する、がSLE治療としての機序として考えられています。

Pearl:cGASは2013年に発見された細胞質二本鎖DNA(dsDNA)センサーで、配列に依存せずにDNAを認識する
comment: cGAS is a cytosolic double-stranded DNA (dsDNA) sensor discovered in 2013 that recognizes DNA in a sequence independent manner
・cGASは2013年に発見された細胞質二本鎖DNA(dsDNA)センサーで、配列に依存せずにDNAを認識する。いったん活性化されると、STINGを活性化する二次メッセンジャーである環状グアノシン一リン酸-アデノシン一リン酸(cGAMP)を合成する。
・不活性型STINGは単量体で、小胞体(ER)に存在する。一旦cGAMPと結合すると、二量体化してゴルジ体に移動し、そこでTANK結合キナーゼ1(TBK1)をリクルートする。これらのSTING-TBK1会合体(STINGシグナルソーム)は、TBK1によるSTING上のセリン366のリン酸化をもたらし、転写因子IRF3のリクルートと活性化をもたらす。
・STINGはまた、IκB(IκB)キナーゼ(IKK)と結合し、NFκBの活性化を促進する。そしてIRF3とNFκBは、IFN-βと炎症性サイトカインを誘導するために共に機能する。
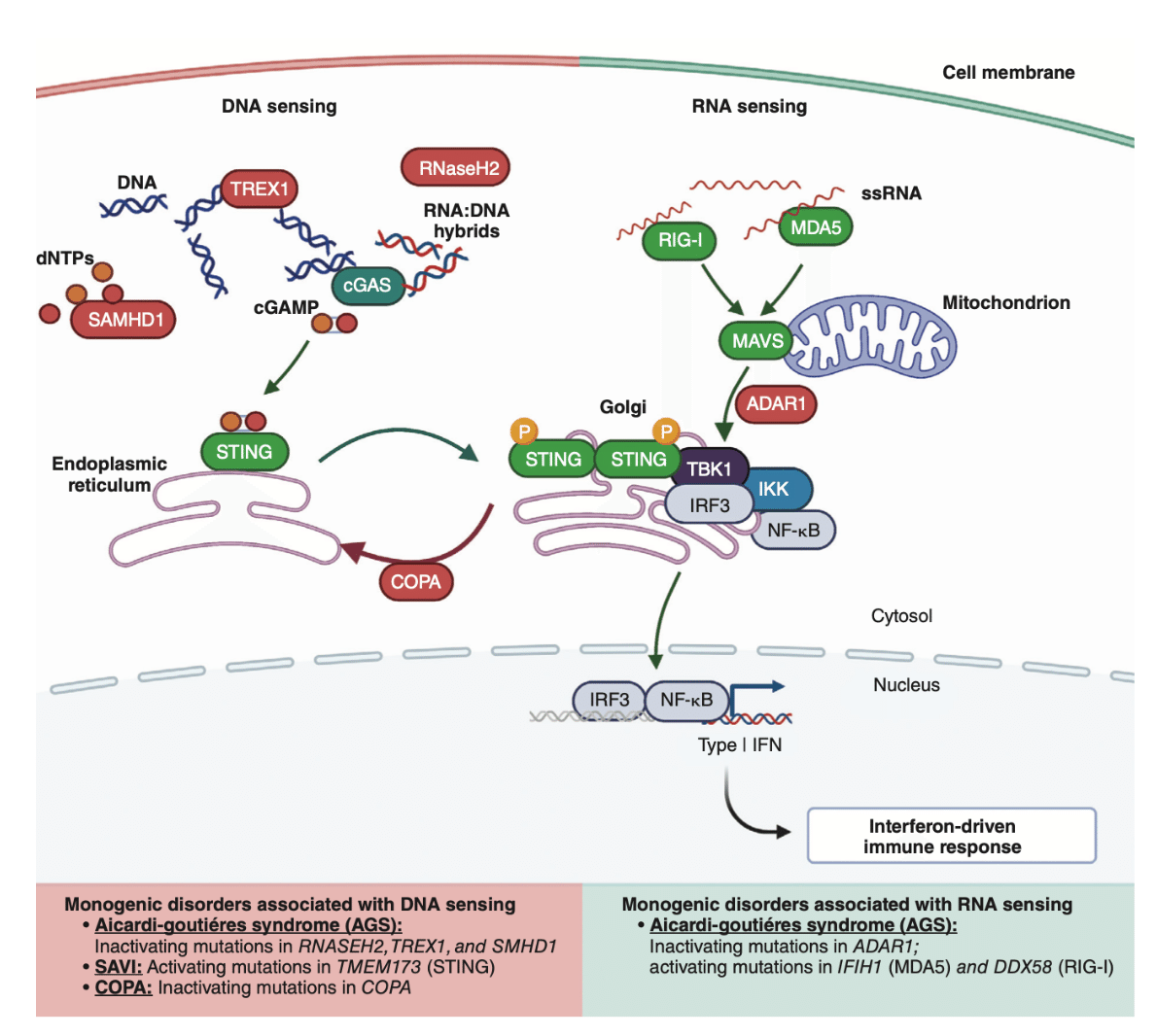
Pearl:RIG-IとMDA5は、dsRNAに対して異なる結合選好性を持ち、MDA5はRIG-Iに比べて長いdsRNAを結合する
comment:RIG-I and MDA5 have distinct binding preferences for dsRNA, with MDA5 binding longer dsRNA compared with RIG-I.
・RIG-I様受容体(RLR)は、レチノイン酸誘導性遺伝子I(RIG-I)(DDX58)、メラノーマ分化関連タンパク質5(MDA5)、遺伝学・生理学研究所2(LGP2)の3つのメンバーから構成されている。
・RNAとの結合後、RIG-IとMDA5は構造変化を起こし、オリゴマー化し、CARD-CARD相互作用を介してMAVSと相互作用し、その結果TBK1が活性化され、IRF3とNF-κBを介した遺伝子発現が起こる。
・LGP2はRNAと結合するが、単独でシグナル伝達を行うのではなく、MDA5とdsRNAの相互作用を増強することでRNAの認識を促進し、RNAと結合して隔離したり、RIG-Iの活性を阻害することでアンタゴニストとしても働く。
・dsRNAの長さがポイント、というのが不思議でした。あとLGP2は、aboratory of genetics and physiology2の略で、日本語にすると「遺伝学・生理学研究所 2」となりましたが、、いいんでしょうか?
Myth:I型IFNの過剰発現はSLEに関連するが、その他の自己免疫疾患には関連しない
reality:Overexpression of type I IFNs helps drive loss of tolerance and is associated with autoimmune disease, including SLE, Sjögren syndrome, systemic sclerosis, and dermatomyositis.
・I型IFNの過剰発現は寛容の喪失を促進し、SLE、シェーグレン症候群、全身性硬化症、皮膚筋炎などの自己免疫疾患と関連している。
・Textbook of Autoinflammationからの表です。SLEのみならず、強皮症、皮膚筋炎、シェーグレンいずれもtype1 IFN pathyと獲得免疫異常の軸に分類されます。

・インターフェロン異常症は、臨床的に多様な単発性自己炎症性疾患のグループであり、I型IFN経路の調節異常によって引き起こされる。
・臨床的には、インターフェロン異常症のいくつかの特徴は共有されている:早期発症、凍瘡、網状皮斑(斑状の皮膚)、脂肪織炎(皮膚の下の脂肪の炎症)、中枢神経系(CNS)の病変、および間質性肺疾患が最も代表的である。
Pearl:アイカルディ・グティエール症候群(AGS)は、典型的なインターフェロン異常症であり、通常、早期発症の脳症として現れ、重篤な知的障害および身体障害をもたらす
comment:AGS is the prototypical interferonopathy, which manifests usually as an early-onset encephalopathy that typically results in severe intellectual and physical disability
・罹患者のサブグループは、神経学的異常、肝脾腫、肝酵素上昇、血小板減少を伴って出生時に診断される。罹患者の大多数は、生後数週間以降に様々な時期に発症し、重篤な脳症と異常発達を示す。 診断は、頭蓋CTで大脳基底核と白質の石灰化が確認され、MRIで白質ジストロフィー変化が確認された後に確定される。血清中および脳脊髄液中のIFN-Iの上昇が検出され、RNA/DNA感知経路の調節異常が示唆される。
・自己免疫症状(自己抗体の存在、関節痛、皮膚、肺、腎臓の病変)はSLEでみられる症状と重なり、寛容の喪失とSLE様自己免疫疾患の発症を促すI型IFNとRNA/DNA感受性の役割を裏付けている。
・神経病変はAGSの顕著な特徴である。I型IFNとcGAS-STING経路がミクログリア機能を制御し、神経炎症と神経変性に関与することが研究で示されている。I型IFNはまた、マウスにおいて脳の発達に悪影響を及ぼすことが示されており、I型IFNの胎児期の過剰発現が神経学的病変に関与する重要な要素であることを論じている。
・興味深いことに、SLEにおける精神神経症状は比較的よくみられるが、I型IFNやcGAS-STING経路の過剰発現との直接的な関連は直接証明されていない。
Pearl:STING-associated vasculopathy with onset in infancy(SAVI)は、全身性炎症、血管障害、炎症性肺疾患を特徴とするI型インターフェロン障害である
comment:STING-associated vasculopathy with onset in infancy (SAVI) is a type I interferonopathy that is characterized by systemic inflammation, vasculopathy, and inflammatory lung disease
・2014年に初めて報告されたSAVIは、 TMEM173遺伝子の機能獲得型変異によりI型IFN産生が亢進した結果であることが発見され、SAVIはI型インターフェロン異常症であることが示された。
・典型的な患者は、全身性の炎症、胸部CTでの間質性肺疾患、重度の皮膚血管症を呈する。70人のSAVI患者のうち、最も一般的なSAVIの症状や特徴は、ILD(80%)、血管障害(77%)、発育不全(70%)、肺線維症(47%)、発熱(45%)、関節炎(26%)である。STINGは多くの細胞型で発現するが、SAVIでは肺が最も影響を受ける臓器系である。
Myth:常染色体優性遺伝のCOPA症候群の原因遺伝子のCOPA遺伝子変異があれば、100%発症する
reality:Because of the relatively low penetrance of COPA syndrome (approximately 75%), it is suggested that additional environmental or genetic factors exist to trigger onset of the disease
・COPA症候群は、最近、肺、腎臓、関節を主に侵す常染色体優性遺伝性の自己炎症性疾患として報告されたコートマー蛋白サブユニットα(COPA)をコードする COPA遺伝子のヘテロ接合体変異によって引き起こされる。このまれな疾患は小児期に発症することが多いが、比較的浸透率が低いため、成人発症型や無症状型では診断されないことがある。
・COPA症候群を引き起こす点突然変異はすべて、カーゴタンパク質上のジリジンモチーフを認識するWD40ドメイン内に存在する。その中で最も一般的な698G>A(Arg233His)は、既知の患者の70%近くを占める(17家系60人弱)。
・ COPA症候群は比較的低浸透率(約75%)であるため、発症の引き金となる環境因子や遺伝因子がさらに存在することが示唆されている。
・ 患者は通常5歳以前に再発性びまん性肺胞出血(DAH)、ILD、関節炎、ループス様腎症症状を呈する。
・2番目に多く観察されるのは関節病変で、有症状患者の75%近くを占める。罹患関節は主に膝と手の指節間関節であり、10代前半に発症する。
・関節病変は一般的に、リウマトイド因子、抗核抗体、抗好中球細胞質抗体、ACPAなどの関節炎関連自己抗体と関連する。特筆すべきは、SLEの特徴である抗二本鎖DNA抗体がCOPA患者ではみられないことである。
・COPA患者は従来、ステロイドと、疾患修飾性抗リウマチ薬(DMARDs)や生物学的製剤などの免疫抑制剤で治療されてきた。免疫抑制レジメンの有効性が報告されているが、COPAとSTINGの関係が明らかになり、IFN/IFNARシグナリングの下流にあるJAK阻害剤への関心が高まっている。
・脊椎軟骨異形成症(SPENCD)は、様々な神経学的症状(痙縮、発達遅延、頭蓋内石灰化)と免疫異常に加えて、稀な骨格形成異常である。免疫異常には免疫不全と自己免疫の合併がみられ、症状はSLEと重複する。実際、SLEの米国リウマチ学会(ACR)基準を満たす患者もいる。
・ちなみに最近は優性遺伝、劣性遺伝という言い方から、顕性遺伝、潜性遺伝という言い方に変更する流れがあるようです(まだあまり浸透していない印象)。
Pearl:単一遺伝子異常によるSLEは、小児期発症SLEまたは家族性SLEを呈する
comment:Similar to the interferonopathies, patients with monogenic forms of SLE present
with childhood-onset SLE or familial SLE.
・インターフェロン異常症と同様に、単一遺伝子異常のSLE患者は小児期発症SLEまたは家族性SLEを呈する。これまでに同定された遺伝子は、補体因子やDNAを分解する酵素の変異に加えて、AGSで同定された遺伝子( TREX1、SAMHD1、RNASEH2A-C、ADAR1)とほぼ重なっている。
Pearl:UVBの照射は、皮膚におけるISG発現が増加するだけでなく、末梢血細胞および腎臓組織におけるISG発現も増加する
comment:In mice, a single dose of UVB not only increased ISG expression in the skin but also increased ISG expression in both peripheral blood cells and kidney tissue, indicating that UVB exposure of the skin can induce a systemic inflammatory response.
・UVBへの暴露は、酸化DNA損傷と皮膚における8-OH-dG病変の蓄積を促進する。
・健康なヒトの皮膚にUVBを単回照射したところ、IFN-Iシグネチャーが増加したことから、UVB照射が皮膚におけるI型IFN活性化の重要な原因であることが示された。
・マウスでは、UVBを単回照射すると、皮膚におけるISG発現が増加するだけでなく、末梢血細胞および腎臓組織におけるISG発現も増加したことから、皮膚へのUVB照射が全身性の炎症反応を誘発することが示された。重要なことは、これらの反応がcGAS依存的であったことである。
・興味深いことに、UVBは皮膚から腎臓への好中球の遊走を誘発し、UV光による皮膚の炎症と腎障害との直接的な関連を示した。

・UVAは、SLEへの関与はUVBほどは強くないとされます。
・日焼け止めについてChatGPTに聞いてみました:
・Sun protection(太陽光からの保護)の強度を示す指標には、**SPF(Sun Protection Factor)ともう一つはPA(Protection Grade of UVA)**です。
SPF(Sun Protection Factor): 主にUVB(紫外線B)からの防御力を示します。数値が高いほど、UVBによる皮膚ダメージ(例えば日焼けやDNA損傷)を防ぐ効果が強いことを意味します。
PA(Protection Grade of UVA): 主にUVA(紫外線A)からの防御力を示します。通常、"PA+"から"PA++++"の4段階で表され、"+"の数が多いほどUVAからの防御力が高いことを示します。UVAは皮膚の深部にまで到達し、しわやしみなどの光老化を引き起こす原因となるため、PAの評価も重要です。
Pearl:補体の欠損とI型IFNの上昇とSLEとの関連は現在のところ不明であるが、潜在的に免疫刺激性/免疫原性の死細胞や残骸(したがって核酸)のクリアランス不全が原因ではないかと考えられている
comment:The link between complement deficiency and upregulation of type I IFN and SLE is currently unknown, but it is thought that defective clearance of potentially immunostimulatory/immunogenic dead cells and debris (and hence nucleic acids) may be the cause.
・ほとんどの症例は早期発症で、年齢中央値は6歳である。
・C1q欠損症では、一般的に皮膚と腎臓の病変がみられ、精神神経系の病変を伴うことは少ない。 C1qはアポトーシス残屑の取り込みを制御し、自己抗原を全身から除去するという重要な役割を担っているため、C1q欠損マウスがアポトーシス体のクリアランス障害を示すのは驚くべきことではない。C1qはまた、in vitroでPBMCおよび単球によるIFN-α産生を負に制御することが示されており、IFN産生の制御におけるC1qのより直接的な役割を示唆している。pDCに対するC1qの阻害作用の結果として、C1q欠乏症患者はI型IFNの発現も増加している可能性がある。

