慢性腎疾患:炭水化物摂取量増加で死亡リスク増加、タンパク質(動物性・植物性を含む)、多価不飽和脂肪、植物性脂肪で炭水化物摂取量を置き換えで死亡リスク減少
慢性腎疾患においては、タンパク質制限が推奨され、「日本腎臓学会のガイドラインでは、標準体重当たり0.6~0.7g/日」とされる。様々な議論があったことは知っているが、未だ、修正されていない。今回、分析手法の問題で、それが、覆されている。
Ren, Qidong, Yangzhong Zhou, Huiting Luo, Gang Chen, Yan Han, Ke Zheng, Yan Qin, and Xuemei Li. “Associations of Low-Carbohydrate with Mortality in Chronic Kidney Dise Ase.” Renal Failure 45, no. 1 (December 2023): 2202284. https://doi.org/10.1080/0886022X.2023.2202284 .
【背景】 食事管理は、慢性腎臓病(CKD)の進行を遅らせるための効果的な方法である。しかし、炭水化物の摂取がCKD患者に与える影響について調査した研究は非常に少ない。この前向きコホート研究では、米国の成人CKD患者を対象に、炭水化物摂取量と全死因死亡率の関連を調査した。
【方法】 多変量Cox比例ハザードモデルおよび等カロリー置換分析を用いて、大栄養素と全死亡リスクとの関連を検討した。National Health and Nutrition Examination Survey(NHANES、2003~2014年)の20歳以上の米国成人CKD患者計3683人(平均年齢±SD、62.4±17.1、女性56.5%)を解析し、そのうちCKD患者1082人が追跡期間中央値67(IQR36~99)カ月で死亡した。
【結果】 炭水化物や糖質を含め、ほとんどのマクロ栄養素が全死亡リスクと非線型的に関連していた。
CKDの参加者は、炭水化物から30~45%のエネルギーを摂取した場合(60%と比較して平均HR0.76、95%CI0.62~0.93)、砂糖から5~20%のエネルギーを摂取した場合(40%と比較して平均HR 0.75 、95%CI 0.59~0.96 )死亡リスクが低くなった。
炭水化物からのエネルギー摂取をタンパク質に置き換える(最大30%)および/または糖質を非糖質炭水化物に置き換える(最大55%)と、総エネルギー摂取量は変わらないが、全死亡リスクは減少した。
【結論】 食事指導は、現在の食事状況に応じて行うべきであり、炭水化物の構成成分も考慮する必要がある。
【www.DeepL.com/Translator(無料版)で翻訳しました。】
序文要約 written with ChatGPT4
最適な食事は、いくつかの慢性疾患のリスクを減らし、寿命を延ばすことと関連しています[Citation1]。しかし、最適な食事の基準は、ガイドラインによって異なります。健康な食事は様々な食品を摂取することを含むと広く認識されていますが、各カテゴリーの具体的な比率や制限は異なって推奨されています[Citation2]。WHOは、過去の研究に基づき、全体のエネルギー摂取量の30%を超えないよう全体の脂肪を、そして10%以下に自由糖を制限することを推奨しています[Citation3][Citation4–6]。しかし、いくつかの研究では、全体の脂肪摂取が心血管疾患と関連せず、むしろ死亡リスクを減らすことが見つかりました[Citation7,Citation8]。炭水化物摂取に関しても議論が存在しています。
こうした背景の中、特に慢性腎疾患(CKD)を持つ人々に対する最適な食事についてのアドバイスは、ガイドラインにより差があります。CKDの人々は、残存する腎機能が食事パターンにより影響を受けやすく、最適な食事はCKDの進行を効果的に防ぐことができます[Citation15]。従来、高タンパク質食は糸球体過濾過の亢進と蛋白尿の増加により腎の悪化を加速するとされてきました[Citation16,Citation17]。しかし、CKDの進行における炭水化物摂取の役割は十分に研究されていません。一般的な人々に対してWHOが推奨する低脂肪、低炭水化物の食事はタンパク質を主なエネルギー源とする一方で、低タンパク質食は依然としてCKD患者向けの主要なガイドラインとなっています。そのため、炭水化物、脂肪、タンパク質の全エネルギー摂取量に対する最終的な比率は未解明であり、低炭水化物食がCKD患者に適しているかどうかは不明です。私たちは、NHANESからのデータを使用して、CKD患者における低炭水化物食と全死因死亡率との関連を調査するための前向きコホート研究を実施しました。
マルチバリアブルのCox比例ハザードモデルを用いてハザード比(HR)を推定しました。更に、全参加者を炭水化物摂取量に基づいて低から高までのパーセンタイルに分け、各グループ間の死亡リスクの差を調査しました。HRトレンドの有意性は、順序付けられた線形回帰を用いてテストされました。さらに、P-splinesが非線形関係を推定するために導入されました。この分析では、「各マクロ栄養素からのエネルギー摂取の割合」という連続変数が露出変数として使用され、一連の共変量がフル調整モデルで調整されました。
結果:要約 written with ChatGPT4


要約です。
分析には、欠落している死亡状況と極端または異常な食事を持つ参加者を除いて、合計19,269人の参加者が含まれました。これには、CKD(平均年齢±SD、62.4±17.1、女性の56.5%)の参加者3,683人が含まれ、そのうち1,929人がeGFRが低下(eGFR < 60 mL / min·1.73m2)し、2,359人がアルブミン尿症(ACR > = 30 mg/g)がありました。
CKDのない参加者と比較して、CKDの参加者は平均年齢が高く(平均年齢±SD 65.5±17.1 vs 47.2±17.2、p < 0.001)、合併症が多かった。
CKDの参加者の摂取炭水化物量によって、CKDの有無の参加者の特性が示されました。
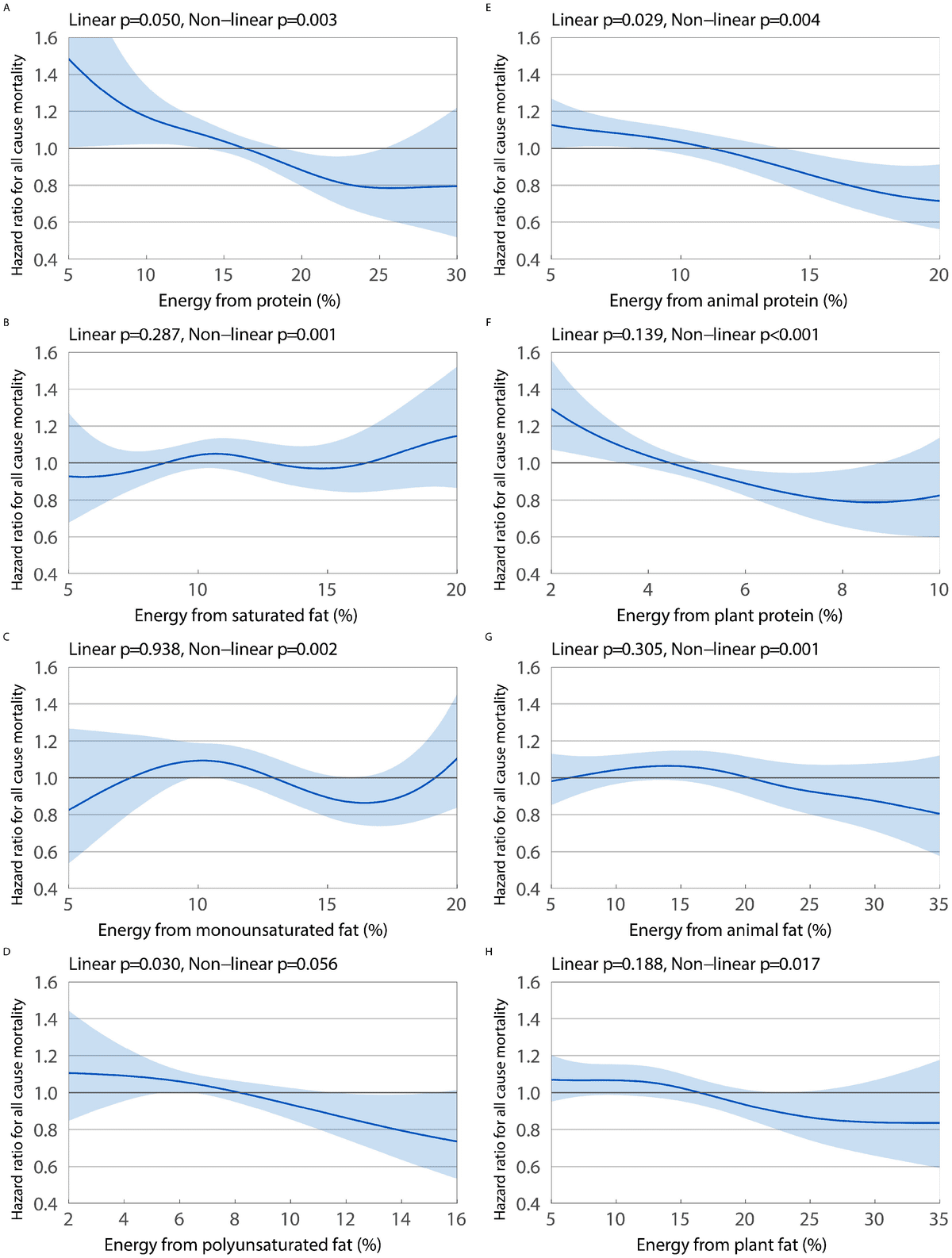
マクロ栄養素と全原因死亡率との関連性は図1に示されています。
感度分析では、異常な食事を報告したCKDの参加者を含めるか、12ヶ月以内に死亡したCKDの参加者を除外することで行われました。
CKDの参加者は、炭水化物または糖からのエネルギー摂取量に基づいて分位数に分けられました。炭水化物摂取量が最小分位数から最大分位数に向かって増加すると、全原因死亡率のリスクが有意に増加しました。
推定糸球体濾過率(eGFR)と尿アルブミンクレアチニン比(ACR)に基づいてCKDの参加者を異なるサブグループに分けました。
エネルギー摂取量を炭水化物と糖で置換すると、全原因死亡率が高くなりました。そのため、等カロリー置換がこれら二つのマクロ栄養素を調査するために行われました。
discussion 要約 written with ChatGPT4
この研究では、慢性腎臓病(CKD)患者の参加者において、炭水化物(糖質、非糖質炭水化物を含む)と全死因死亡率との間に非線形の関連性が観察されました。また、同様の結果は、タンパク質、脂質、飽和脂肪、一価不飽和脂肪、多価不飽和脂肪、動物性タンパク質、植物性タンパク質、動物性脂肪、タンパク質脂肪と全死因死亡率との間でも見られました。これらの結果は、感度分析とサブグループ分析で主に一貫していました。さらに、炭水化物摂取量が増えると死亡リスクが高まることが分かり、詳細な調査で糖質摂取量が多いほど死亡リスクが高いことが明らかになりました。タンパク質(動物性・植物性を含む)、多価不飽和脂肪、植物性脂肪で炭水化物摂取量を置き換えると死亡リスクが減少することが分かりました。同様に、糖質摂取量を非糖質炭水化物、タンパク質(動物性・植物性を含む)、多価不飽和脂肪、植物性脂肪で置き換えると死亡リスクが減少することが示されました。ここでは、大量栄養素とCKD患者の全死因死亡率との間の多様な関連性を示しました。私たちは、単一の大量栄養素と結果との線形関連性に焦点を当てている多くの以前の研究とは異なり、大量栄養素とその成分の非線形関連性を調査しました。CKD患者の異なる食事パターンによる死亡リスクの変化を探るために、等カロリー交換分析を実施しました。
過去の研究では、炭水化物摂取量と死亡率との間の直線的な関連性についての結果が一致していませんでした。いくつかの研究では、一般集団で非線形の関連性が示唆されています。大規模コホート研究やメタ分析では、炭水化物摂取量と死亡率との間にU字型の関連性が見つかりました。彼らは、炭水化物の摂取が高すぎるか低すぎると、死亡リスクが増加すると提唱しています。UKバイオバンクコホートを使用した研究でも、同様の非線形関連性が報告されました。しかし、炭水化物摂取量が低い場合のリスクは有意にならず、結果としてJ字型の曲線が得られました。CKD患者では、炭水化物摂取量と全死因死亡率との間にほぼS字型の関連性が見つかり、炭水化物摂取量が増えると死亡リスクが高まることがわかりました。過去のCKD患者に対する食事研究のほとんどはタンパク質に焦点を当てており、臨床実践ではCKD患者には低タンパク質食が一般的に推奨されています。腎臓疾患の既存の人口におけるいくつかのランダム化比較試験(RCT)とメタ分析では、低タンパク質食がCKDの進行を遅らせ、透析療法の開始を効果的に遅らせる重要な役割を果たすことが支持されています。しかし、栄養不良やタンパク質エネルギー消耗の懸念、低タンパク質食の効果についての矛盾した結果があるため、低タンパク質食を守る必要性や戦略については議論があります。低タンパク質食の効果は、糖尿病などの合併症やタンパク質の源によっても影響を受けます。一日の全エネルギー需要を満たすために、低炭水化物食は、ある意味では高タンパク質食や高脂肪食です。たとえば、アトキンスダイエットやゾーンダイエットはそうです。24名の予備糖尿病患者を対象としたRCTでは、高タンパク質食が高炭水化物食と比べて保護効果を示しました。この研究では、CKD患者の参加者におけるタンパク質摂取量(0.9g/kg)は、一般的な低タンパク質食範囲(0.6-0.8g/kg)には含まれておらず、タンパク質を30%まで炭水化物と置き換えると高タンパク質食(1.7g/kg)になります。炭水化物摂取量が少ないほど死亡リスクが低いことと、タンパク質(植物性および動物性タンパク質を含む)と炭水化物との置き換えによる死亡リスクの減少を観察しました。同時に、タンパク質摂取量が多いほどCKD患者の死亡リスクが低いことも見つかりました。いくつかの研究でも、高タンパク質食が有益である可能性を示しています。一つの可能性として、高タンパク質摂取量により十分な栄養が提供され、筋肉量を維持するのに役立つと考えられます。十分な筋力があると、患者はより多くの身体活動を行うことができ、転倒や骨折に巻き込まれる可能性が減少し、これが死亡リスクを減少させる可能性があります。また、高タンパク質摂取量は、より多くの生物活性ペプチドを提供する可能性があります。これらの生物活性ペプチドは、抗炎症、抗高血圧、抗酸化、抗微生物活動を持つと報告されています。これらの保護活動は、死亡リスクを低下させる可能性があります。しかし、CKD患者における高タンパク質食の効果はまだ議論の余地があり、より長期的で大規模なサンプルの研究が必要です。
本研究の主な強みは、米国成人の国内代表的なNHANESデータを使用して、初めて低炭水化物食とCKD患者の全死因死亡率との関連性を調査し、直線関連性を仮定しなかったことです。また、非線形関連性を評価するために多変量自己回帰スプラインを使用し、等カロリー交換分析を実施することで、食事パターンの全死因死亡率への可能な影響を考慮しました。本研究の制約としては、食事データが24時間の食事リコールから得られたこと、食事行動の変化を評価する追跡データがないこと、食事摂取量の報告の誤差を完全に排除することができないこと、観察研究の性質上、交絡因子を完全に制御することができないこと、などが挙げられます。
それにもかかわらず、今回の研究結果は、CKD患者の食事摂取の選択と全死因死亡率との関連性について重要な知見を提供し、さらなる研究を行うための基盤を提供します。
