静脈血栓塞栓抗凝固治療:大出血リスク アピキサバンが少ない
静脈血栓塞栓抗凝固治療:大出血リスク アピキサバンが少ない
国際的なガイドラインに従って、多くのVTE患者が抗凝固療法の延長を受けている。臨床の現場では、VTEに対する延長治療を行うかどうかの決定には、治療を行わずに再発するリスクと治療中の出血リスクとのバランスを患者ごとに考慮する必要がある。しかし、DOACによる延長治療中の出血リスクはほとんど不明である。1年を超える延長治療に関するデータは、RCTや前向きコホート研究から不足している。レジストリのデータでは、ほとんどの研究が約6ヵ月の追跡を伴う初期治療を対象としている 。
本研究の目的は、初回VTE患者における初回治療時(0~6ヵ月)と延長治療時(6ヵ月~5年)の両方において、抗凝固薬治療の選択による大出血のリスクを明らかにすること
Glise Sandblad, Katarina, Sam Schulman, Annika Rosengren, Jan Sörbo, Jacob Philipson, and Per-Olof Hansson. “Association of Type of Oral Anticoagulation with Risk of Bleeding in 4 5,114 Patients with Venous Thromboembolism during Initial and Extended Treatment-A Nationwide Register-Based Study.” Journal of Internal Medicine, August 28, 2023, 10.1111/joim.13712 . .
【背景】 静脈血栓塞栓症(VTE)における様々な抗凝固薬の安全性に関するデータは、特に長期治療に関しては乏しい。
【目的】 初回治療(最初の6ヵ月)および延長治療(6ヵ月~5年)における抗凝固療法の選択による大出血率を比較すること。
【方法】 2014年から2020年の間に初回VTEを発症したがん未発症患者を含む全国規模の登録ベースの研究。Cox比例ハザードモデルを用いて出血率を比較した。
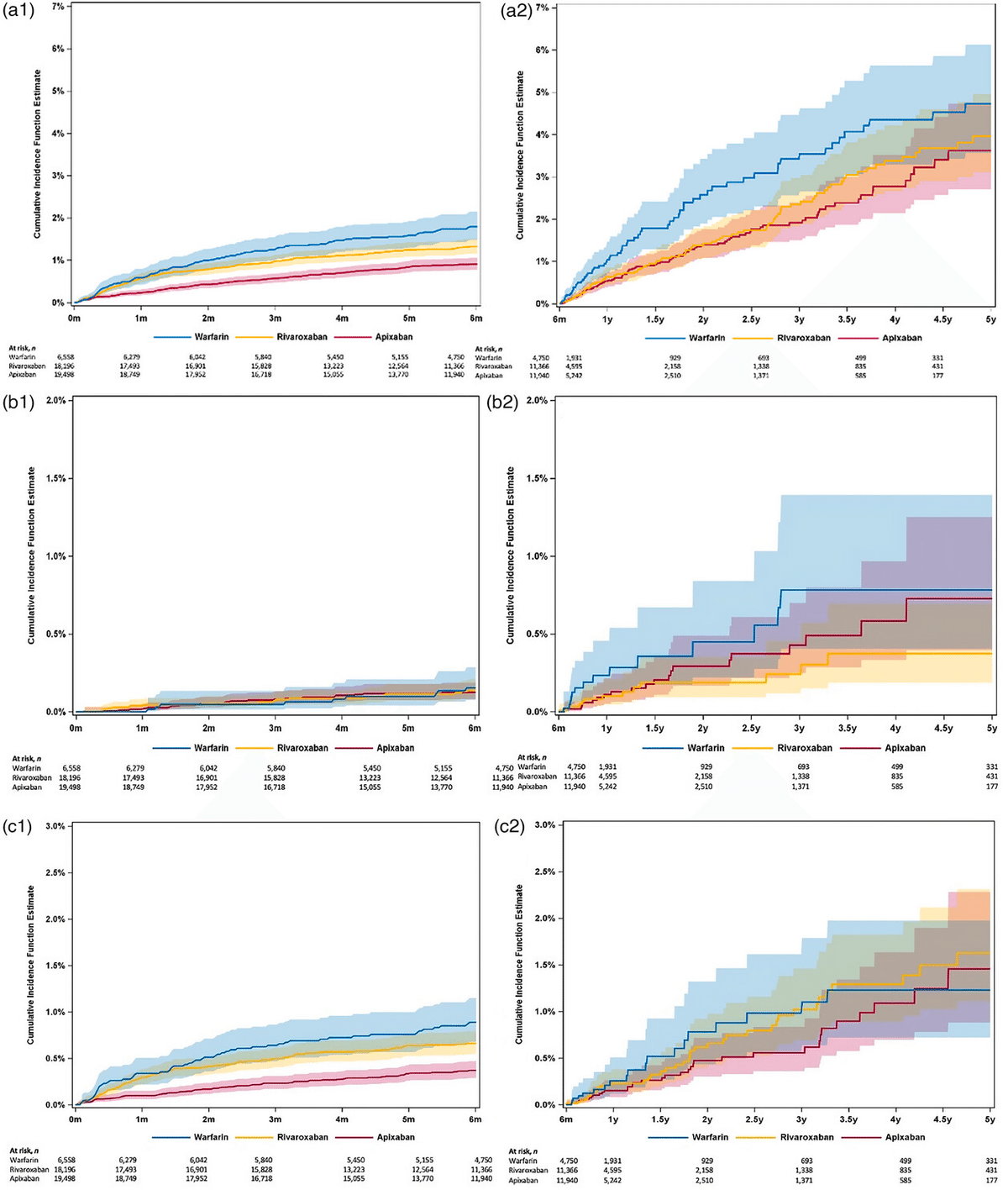
【結果】 ワルファリン投与中の6558例、リバーロキサバン投与中の18,196例、アピキサバン投与中の19,498例を対象とした。6ヵ月時点では、4750例(72.4%)がワルファリン、11,366例(62.5%)がリバーロキサバン、11,940例(61.2%)がアピキサバンを継続投与していた。
初回治療中の大出血率は、ワルファリン、リバーロキサバン、アピキサバンでそれぞれ100患者年あたり3.86(95%CI 3.14-4.58)、2.93(2.55-3.31)、1.95(1.65-2.25)であり、調整ハザード比(aHR)は0. リバーロキサバン対ワルファリンで89(95%CI 0.71-1.12)、アピキサバン対ワルファリンで0.55(0.43-0.71)、アピキサバン対リバーロキサバンで0.62(0.50-0.76)であった。
延長治療中の大出血発生率は、ワルファリン、リバーロキサバン、アピキサバンでそれぞれ100患者年あたり1.55(1.19-1.91)、1.05(0.85-1.26)、0.96(0.78-1.15)であり、aHRは0.72(0.53-0.99)であった。 リバーロキサバン対ワルファリンでは72(0.53-0.99)、アピキサバン対ワルファリンでは0.60(0.44-0.82)、アピキサバン対リバーロキサバンでは0.85(0.64-1.12)であった。出血の既往と年齢の上昇は、初回治療中および延長治療中の出血の危険因子であった。
【結論】 アピキサバンは初回治療中の出血リスクがワルファリンやリバーロキサバンよりも低かった。延長治療中の出血リスクはアピキサバンとリバーロキサバンで同程度であり,ワルファリンで高かった。
【www.DeepL.com/Translator(無料版)で翻訳しました。】

Discussion要約 written with Bard
がんと診断されていない初回VTE患者を対象とした全国規模の登録ベースのコホート研究が実施された。
主な知見は、アピキサバンおよびリバーロキサバンによる長期抗凝固療法中(6ヵ月以上)の患者の全体的な出血リスクが低く、出血率は臨床試験と同程度であったことである。
アピキサバンまたはリバーロキサバンによる治療は,ワルファリンによる治療よりも多変量調整後の出血リスクが低く,アピキサバンとリバーロキサバンの間に差はなかった。
治療開始後6ヵ月間は、アピキサバン投与群の方がワルファリン投与群やリバーロキサバン投与群よりも出血リスクが低かった。
初回治療中および延長治療中の大出血の最も重要な危険因子は、年齢の上昇と出血の既往であった。
延長治療中の頭蓋内出血のリスクはワルファリンよりもリバーロキサバンのほうが低かったが、消化管出血のリスクには抗凝固療法の違いによる差はみられなかった。
65歳未満の患者では治療期間にかかわらず出血率は低かった。
年齢が高いこと,出血の既往があること,慢性閉塞性肺疾患,腎不全,抗血小板薬または選択的セロトニン再取り込み阻害薬による治療は,多変量調整後,延長治療中の出血の危険因子であった。

心不全、慢性閉塞性肺疾患(COPD)、糖尿病、腎不全、肝疾患、虚血性心疾患、末梢動脈疾患、虚血性脳卒中、出血性脳卒中、全身性結合組織疾患、炎症性腸疾患、認知症。また,抗凝固薬治療中に抗血小板薬,プロトンポンプ阻害薬,選択的セロトニン再取り込み阻害薬(SSRI),スタチン系薬剤を併用している場合にも調整を行った。
COPDが出血リスクなのはなぜだろう?
