2-1 薬物動態と薬物相互作用
ここでは、
・薬物の ADME の過程の詳細
・薬物相互作用の機序
について、特に経口投与の時の流れを説明します。
吸収
吸収過程では、消化管側から、細胞膜を通過して、吸収されます。
したがって、細胞膜を通過しやすい物質が、吸収されやすいといえます。
細胞膜の構造は、脂質二重膜構造の中に、機能を有するタンパク質が埋め込まれた構造をしています。脂質二重膜は、リン脂質がモザイク状に並んでおり、外側に向けて、水に溶けやすい部分が並んでおり、脂質膜の中央部分は、疎水性の部分が並んでおり、いわゆる油と親和性が高い部分となっています。
血液の中や細胞の中は、物質は水に溶けた状態で存在していますが、細胞膜を通り抜けるには、油を通り抜ける必要があります。

吸収過程の機序
吸収されやすい物質の特徴として、以下のようなものがあります。
①脂溶性・低分子
リン脂質の隙間を通りやすい物質は、まず、脂溶性が高く、小さい低分子の物質であること。
②担体輸送の基質
膜タンパク質として埋め込まれているタンパク質には、物質を運ぶイオンチャネルやトランスポーターなどの役割を果たすものがあります。これらの基質となるものは、積極的に運ばれるので、膜を通過することが可能です。
③分子型
化学物質の中には、水に溶けた時に電離(陽電荷もしくは陰電荷を帯びる)するものがあります。これは、水中で、電荷を帯びている「イオン型」と、電荷を帯びていない「分子型」が自由に入れ替わっています。
イオン型は、水に溶けやすい形(親水性が高い)であり、分子型は、親水性は低い(=油との親和性が高い)形と言えます。
そのため、細胞膜の通過性については、分子型は細胞膜を通過しやすい形です。
水中においてイオン型と分子型の割合を決めるのは、pH です。環境の pH によって、分子型が多い条件だと、細胞膜を通過しやすいし、イオン型が多い条件だと、細胞膜を通過しにくい、と言えます。
例えば、胃酸分泌を抑制する薬を飲むと、胃内 pH を下げている胃酸分泌が減るため、pH がアルカリ性側に近づいてしまうことで、一部の薬は相互作用を受けます。

吸収過程の相互作用
吸収過程における薬物相互作用の機序:
吸収された薬物が、血液中に移行して、薬効を発揮します。
そのため、吸収を阻害すると、薬物血中濃度は低下し、薬効は減弱し、薬は効かなくなります。
吸収過程における薬物相互作用の代表例として、抗菌薬の一部と、牛乳の相互作用があります。

吸収過程における相互作用の代表例として、一部の抗菌薬と牛乳等の相互作用があります。
一部の抗菌薬というのは、抗菌薬のうち、
テトラサイクリン系とニューキノロン系という薬効群が該当します。
消化管の中で、金属イオンと出会うと、
お互いに強く結合してしまうため、抗菌薬が吸収されなくなります。
これは、抗菌薬と、特に2価(2+になる)の金属イオンとの間で起こる反応です。
臨床でも遭遇する頻度が高い相互作用です。
特に、緩下剤としてよく使われる「酸化マグネシウム」に注意が必要です。
では、この相互作用を回避するためには、どうしたらよいのでしょうか?
消化管の中で二つの薬物が出会うため、起こる相互作用です。
間隔をあけて服用することで回避することができます。
抗菌薬を先に投与して、2時間以上空けると、酸化マグネシウムを服用しても薬効低下は問題とはなりません。
例えば、夕食後に抗菌薬を服用して、就寝前に酸化マグネシウムを服用する、というのは、相互作用を回避するための、一つの方法です。
吸収過程における相互作用には、消化管運動に影響するために起こる相互作用などもあります。

分布
分布とは、血中から組織への移行のしやすさ、及び、組織への蓄積性を表すものだと説明しました。
分布を左右する大切な要素が、血漿タンパク質です。
薬物は、血液中において、血漿タンパク質と結合して存在しています。その血漿タンパク質とは、主にアルブミンです。薬物は血漿タンパク質と結合したり離れたりして存在しており、結合しやすさ(タンパク結合率)は、薬物によって異なります。
血管内から細胞膜を通過して、組織へと移行する時にも、やはり、細胞膜を通過します。
重要なのは、血漿タンパク質と結合している「結合型」の薬物は、細胞膜を通過できませんが、血漿タンパク質と結合していない「遊離型」の薬物は、細胞膜を通過することができる、ということです。
遊離型の薬物は、目的の作用部位(臓器や組織)へと移行して、薬効を発揮します。
次に、一旦、組織中に移行した薬物が、血管内に移行する過程を考えます。
組織の細胞中にもタンパク質は存在します。組織でタンパク質と結合すると、結合型は細胞膜を通過しないので、そのまま、細胞の中に残ります。
しかし、遊離型は、細胞膜を通過して、血管内に移行します。その後、代謝を受けたり、排泄を受けたりして、体外へと排出されます。
このように、組織で、タンパク質を強く結合する薬物の場合、体内に長くとどまる、という特徴を示します。
このように、タンパク質と結合する時の、結合しやすさや結合の強さによって、組織への移行しやすさ、組織への蓄積性が左右されます。
また、薬物が最も移行しにくい組織の一つに、脳があります。
脳血管の周囲は、強固なバリアがあるため、薬物などは、血管を出て組織に移行することは、非常に困難です。このバリアを、血液-脳関門(blodd brain barrier, BBB)といいます。

分布過程の相互作用
分布過程における薬物相互作用の機序:
イメージとして、薬物がタンパク質との結合を奪い合うために起こります。
例えば、Aという薬を先に服用しました。
これは、タンパク結合率が比較的高い薬物であり、5個中の4個がアルブミンと結合しており、1/5は遊離型として存在しています。前述した通り、薬効を発揮するのは「遊離型」ですので、この1個が薬効を発揮している状態です。
そこに、Aよりもアルブミンと強く結合する B を併用した場合、アルブミンとの結合は、Bに奪われてしまいます。そのため、Aは、5個が遊離型として存在しています。つまり、5個が薬効を発揮するため、先ほどと比較すると、5倍強く薬効を発揮すると考えられます。
効き目が強く出るのならば良いのですが、効きすぎは、薬による悪影響(有害事象)が強く出ることにつながります。
特に注意が必要な場合として、タンパク結合率が高い薬物、低アルブミン血症の場合、があります。

タンパク結合率の強さによって、薬物相互作用の影響がどのように違うのかを見てみましょう。
例えば、タンパク結合率が20%の薬。
遊離型は8個、結合型が2個存在しています。薬効を示すのは、8個分です。
ここに、タンパク結合を置換する薬との相互作用が起きた場合、全てが置き換えられたとすると、遊離型は10個、結合型は0個になりました。薬効を示すのは10個分です。
しかし、8個が10個に微増しただけで、それほど、大きな影響が出るようには、見えません。
次に、タンパク結合率が90%の薬の場合。
遊離型は1個、結合型が9個存在しています。薬効を示すのは1個分です。
ここに相互作用が起きた場合、遊離型は10個、結合型は0個になりました。薬効を示すのは、10個分です。
このように、1個から10個と、遊離型の薬剤が大幅に増えてしまいました。
このように、タンパク結合率が高い薬物の場合では、相互作用に注意が必要です。
また、先ほど、低アルブミン血症にも注意が必要だと言いました。
アルブミンが少ないと、結合型の割合も少なくなり、結果として、遊離型の薬物の割合が上昇してしまうと考えられます。
そのため、低アルブミン血症の場合、薬物の効果が強くでる(効きすぎる)ことが起こります。

代謝
代謝過程において、重要な役割を担っているのは、代謝酵素である、シトクロム P450です(ちとクロームと呼ばれることもあります)。cytochrome P450 の頭文字をとって CYP(シップ)と書きます。
これは、肝臓において、いわゆる“解毒”をしている酵素です。これは特定の一つを指している言葉ではなく、酸化還元反応を起こしている酵素の総称として、CYP といいます。
酵素反応は、工場に例えられます。
工場では、原料を加工して、製品を生産します。
原料のことを、「基質」といい、生産した製品のことを、「生成物」といいます。
酵素は、反応を媒介する工場作業員のようなもので、それ自身は変化しませんが、原料を加工します。
この工場が、肝臓にあります。
CYP は、500個程度のアミノ酸が並んでできており、アミノ酸配列の相同性(どれだけ似ているか)を元に細かく分類されています(分子種に分類されています)。
その分類の中で、最も重要なのが、CYP3A4(シップスリーエーフォー)です。肝臓にある CYP の大部分を占めています。
また、CYP には、酵素活性に個体差があるものがあります。例えば、CYP3A4 を作る遺伝子の一部分が変化すると、酵素の性能が異なります。
これを、遺伝子多型といいます。

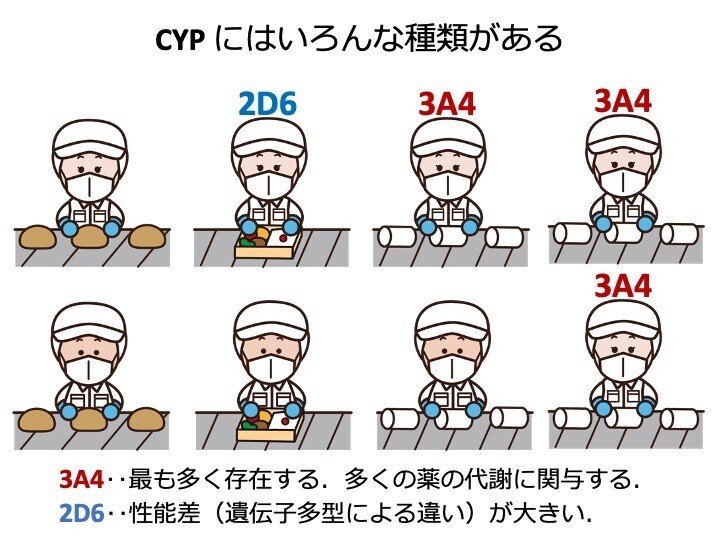
CYP にはいろんな分子種があります。
特に大切なものとして、二つあります。
CYP3A4
これは、最も多く存在しており、非常に沢山の薬物の代謝に関与しています。
CYP2D6
これは、例えば弁当を作る工程に例えると、非常に複雑なので、作業員が器用か、不器用かによって、作業効率が大きく異なります。(あくまでもイメージとして)
遺伝子多型によって、酵素活性が大きく異なるのが、特に、この CYP2D6です。
代謝過程の相互作用
次に、代謝過程における薬物相互作用が、どのような影響をあたえるかを見ていきましょう。
代謝過程における薬物相互作用は、2種類があります。「酵素誘導」「酵素阻害」です。
酵素誘導
「酵素誘導」とは、工場の作業員を増やすようなものです。作業員が増えると、原料を消費して、大量の製品を作ることができます。
つまり、酵素誘導の結果、薬物の血中濃度は減少します。
実際には、酵素誘導を起こす薬物が作用すると、遺伝子からのタンパクの翻訳が活性化されることで、酵素が増えることにつながります。
「酵素誘導」とは、遺伝子を翻訳して酵素を作ることを誘導する命令を出すことです。これにより、酵素は増加します。
その結果、酵素反応が盛んに起こるので、薬物の血中濃度は減少し、薬効が減弱する、つまり、せっかく飲んだ薬が効かない、という結果になります。

酵素阻害
次に、「酵素阻害」とは、工場の作業員の手を縛って邪魔をしているようなものです。
原料を加工することができないので、原料は減らずに、どんどん溜まっていきます。
つまり、酵素阻害の結果、薬物の血中濃度は増加します。
この結果、薬物の血中濃度が適度に増加すると、薬効が強く現れて良いことのように思えるかもしれませんが、血中濃度が上昇しすぎると、同時に、薬物の毒性も現れてしまいます。
つまり、副作用の可能性が高くなる、といえます(有害事象とは、薬物服用後に起こった全ての影響を指す言葉で、「副作用」よりも幅が広い言葉です。後述します)。
実際には、「酵素阻害」とは、酵素の活性中心などに結合して、酵素反応を邪魔します。
どの程度しっかりと結合して邪魔するのか(一旦邪魔すると離れないなど)、どの酵素に結合するのか(選択性)は、阻害剤の性質によって様々です。

代謝過程における薬物相互作用をまとめておきます。
通常、代謝によって、薬物が分解され、薬物の量は減少します。
「酵素誘導」により、酵素は増加します。
その結果、酵素反応が盛んに起こるので、薬物の血中濃度は減少し、薬効が減弱する、つまり、せっかく飲んだ薬が効かない、という結果になります。
「酵素阻害」の結果、酵素反応が起こらないため、薬物は減少しない、つまり、薬物血中濃度は増加します。その結果、薬効が増強するにとどまらず、薬物の毒性も増強し、有害事象が発生してしまいます。
この関係性を正しく理解しておきましょう。

沢山の分子種があると説明しましたが、薬物によって、どの分子種の酵素で代謝を受けるか決まっています。また、阻害薬や誘導薬も、どの分子種に影響するか決まっています。
表には、その一覧を上げていますが、大切なポイントはこの通りです。
(※表には、CYP3A と書いていますが、CYP3A4 は CYP3A のグループの中の一つの種類です)
◯多くの薬物の代謝に関わっているのが、CYP3A(特に、CYP3A4)
◯酵素阻害薬
・アゾール系抗真菌薬(イトラコナゾール、ケトコナゾール)
多くの薬物代謝に関わる CYP3A4 を強く阻害します
・シメチジン【H2-ブロッカー】…胃酸分泌抑制薬
全ての CYP を阻害します
◯酵素誘導薬
・古典的抗てんかん薬(フェノバルビタール、カルバマゼピン)
自身も CYP で代謝されますが、酵素誘導も引き起こします
(*「古典的」という言い方は、新規の抗てんかん薬は薬物相互作用がないものもあり、従来から用いられている抗てんかん薬を指して、「古典的」と総称するため、このように記載しています)
・リファンピシン【抗結核薬】
多くの種類の CYP に対して、酵素誘導を引き起こします
※どちらも、長期間にわたって服薬継続する薬であり、その管理が重要になります
酵素阻害作用を示す薬物は非常に沢山ありますが、酵素誘導を引き起こす薬は、少ないです。
また、表を見ると、影響を及ぼす酵素は一つだけではなかったり、誘導薬でありながら、自身も別の分子種の基質となっていたり、非常に複雑ですので、相互作用が起こらないように、まずは、できるだけ少ない薬で治療すること、治療薬が必要な場合、相互作用が起こらないような薬を選択することが重要です。

排泄
腎排泄の機序について、説明していきます。
腎臓での排泄において、腎臓の機能単位として、ネフロンがあります。ネフロンは、ボーマンのうと糸球体からなる腎小体と腎細管を一つの単位として、左右の腎臓にネフロンが各100万個あると言われています。
腎臓における薬物の排泄に関わる過程は、3つの過程からなります。
①糸球体濾過
②尿細管分泌
③尿細管再吸収

糸球体濾過
糸球体濾過では、老廃物が濾過される過程です。網目を濾すため、タンパク質のような高分子のものは、通常(腎障害がない状態では)、濾されることはありません。低分子の薬物が濾し出されます。
薬物に関しては、
タンパク質と結合している結合型は、糸球体濾過を受けませんが、
タンパク質と結合していない遊離型は、糸球体濾過によって、体外へと排出されます。
従って、「分布」の過程と同様に、薬物相互作用によって、タンパク結合率が変化した場合には、薬物の血中濃度も変化することになります。
タンパク結合が置換され、遊離型薬物が増えると、それだけ、体外に排出されるため、血中濃度は減少します。
次に、糸球体濾過に薬物が与える影響に関与する要因に、腎血流量があります。
腎血流量が多いと、その分、大量に濾過を受けるといえます。
そのため、腎血流量を減少させる薬物Bを併用すると、特に薬物 A の体外への排泄において腎排泄の割合が高い場合、濾過量が減少するため、血中濃度が上昇し、有害事象の可能性も高くなります。
この例に、NSAIDs があります。

尿細管分泌
尿細管分泌とは、血液中の薬物を、尿中へと排泄させるための過程です。
薬物の分泌は、近位尿細管でおこっています。輸送担体を用いて、積極的に排泄しようとしています。
この輸送担体には、有機アニオントランスポーター(OAT)などがあります。
A薬は、輸送担体によって尿中に分泌され、排泄されます。
その輸送担体を阻害する B 薬を併用すると、尿中に分泌されず、体内に残るため、血中濃度が上昇し、有害事象の可能性も高くなります。
教科書にも掲載されている相互作用で言うと、メトトレキサートと NSAIDs の相互作用がこれに該当します。
他にも、例えば、「この薬はリンゴジュースなどの果物ジュースで服用しないでください」というのは、この相互作用を防ぐためのものです。
尿細管再吸収
尿細管再吸収は、尿の生成においては、水分の再吸収などが起こっています。
薬物の場合、遠位尿細管では、能動輸送によって薬物が原尿から血管の方へ、再吸収されています。
吸収過程と同様に、分子型の薬物が再吸収されやすいです。
この分子型とイオン型の割合は、尿 pH によって変わります。
併用薬によって尿 pH が変わると、薬物の血中濃度も変わります。
酸性薬物であるフェノバルビタールは、
・尿をアルカリ化すると、イオン型分率が増える
→再吸収が阻害され、排泄が促進される
→薬物血中濃度は減少する=効果が減弱する
そのため、炭酸水素ナトリウムを併用すると、これは尿をアルカリ化させるため、フェノバルビタールの効果は減弱します。

まとめ
ADME の各過程の特徴と相互作用の機序
「吸収」「分布」「代謝」「排泄」
臨床で遭遇する頻度の高い相互作用は、「代謝」過程における相互作用
記事内のイラスト [PDF]
※メンバーマガジンに、PPT のダウンロード先を掲載しています
いいなと思ったら応援しよう!

