
125)アルカリ食はがんや慢性疾患を減らし寿命を延ばす
体がみるみる若返るミトコンドリア活性化術125
ミトコンドリアを活性化して体を若返らせる医薬品やサプリメントを解説しています。
【体液の水素イオン濃度が増えた状態をアシドーシス(酸性血症)という】
水の中に物質が溶けていると、その水溶液は酸性、中性、アルカリ性のうちのいずれかの性質を示します。水溶液中に存在する水素イオン(H+)が多いほど酸性になります。
例えば、塩酸などの酸を水に加えるとpH が下がります。 溶液の酸性度はプロトン(水素イオン)の濃度([H+])によって決まります。水素イオン濃度(mol/L)は[H+]で示します。
水素イオン指数(pH)は水素イオンの濃度([H+])を表す物理量で、[H+]を簡単に表現するための指標です。pHは水素イオン濃度の逆数の常用対数で示されます。pHは次式のように表されます。
pH= −log10[H+]
つまり、水素イオン濃度[H+]が0.001 mol/Lであれば pH=−log1010-3 = 3で、pHが3となります。水素イオン濃度[H+]が0.01 mol/LであればpHは2です。水素イオン濃度が高いほどpHは小さい値になります。
水溶液のpHが7より小さいときは酸性、7より大きいときはアルカリ性、7付近のときは中性になります。pHが小さいほど水素イオン濃度は高く、pHが1減少すると水素イオン濃度は10倍になります。逆にpHが1増加すると水素イオン濃度は10分の1になります。
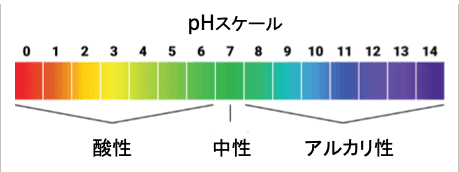
正常な動脈血のpHは7.35〜7.45という非常に狭い範囲で調節されています。血液や体液のpHが通常よりも酸性に傾く状態をアシドーシス(acidosis)と言います。日本語で酸性血症と言います。動脈血のpHが7.35未満になると、アシドーシスとみなされます。
アシドーシスの反対はアルカローシス(alkalosis)です。アルカローシスは、体液のpHが正常よりもアルカリ性(pHが7.45以上)になる状態です。これは、血液中の酸性度が低下し、アルカリ成分の割合が増加することを意味します。
【軽度のアシドーシスが慢性疾患を増やしている】
西洋諸国の多くの人は軽度(低グレード)のアシドーシスの状態にあり、これが様々な慢性病を増やしていることが指摘されています。以下のような論文があります。
Low-grade metabolic acidosis as a driver of chronic disease: a 21st century public health crisis(慢性疾患の原因としての低グレード代謝性アシドーシス:21世紀の公衆衛生危機)Open Heart. 2021; 8(2): e001730.
アシドーシスは体内に酸が滞留し、体内の重炭酸塩貯蔵量が減少すると発生します。血液中の酸が多すぎる状態は、体の緩衝能力が正常な pH レベルを維持できなくなった場合に発生します。
低グレード(low-grade)とは、明らかな害や目立った害はないが、体内に酸が蓄積し、重炭酸塩の貯蔵量が枯渇し、体内の多数の組織に損傷が発生していることを意味します。低グレードのアシドーシスでは、血液中の重炭酸塩レベルと水素イオン濃度(pH )がわずかに低下しますが、依然として「正常」範囲内にあります。
軽度(低グレード)であっても、このようなアシドーシスの状態が数十年にわたり続くと、それが様々な慢性疾患の発生を促進しているという指摘です。
低グレードのアシドーシスは西洋諸国の多くの人が罹患しているにもかかわらず、それに気づいていない慢性疾患であると言っています。21世紀の公衆衛生上の危機だと言っています。
低グレードのアシドーシスでは、総血液緩衝能が低下するため、追加の酸を除去するために筋肉、骨、結合組織への依存度が高くなります。低グレードアシドーシスの害は、年齢とともに増加し、腎臓の酸を排泄する能力が低下するため腎機能が低下します。体内の酸負荷の増加は、長期的には腎機能を悪化させます。
体の酸性化は様々なメカニズムで老化を促進し、慢性疾患と増やし、寿命を縮めることは多くの研究で明らかになっています。
【体液の水素イオン濃度は重炭酸緩衝系で調節される】
体内のpHは非常に狭い範囲で厳密に制御されています。正常な動脈血のpHは7.35〜7.45という非常に狭い範囲で調節されています。このpHの調節は酸と塩基のバランスで行われます。「酸」というのは水素イオン(H+)を放出する物質で、「塩基」というのは水素イオン(H+)を受け取る物質です(下図)。

酸塩基のバランスを一定に保つ働きは体のいろいろなところで行なわれていますが、その中でも代表的な部位は、血液・体液、肺、腎臓です。
血液・体液における酸塩基平衡の調節で最も重要なのが重炭酸緩衝系です。この系は、重炭酸イオン(HCO3-)が塩基となってプロトン(水素イオン)を受けとって中和してpHを一定に維持します。
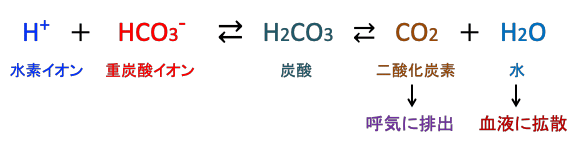
図:体内で産生される水素イオンを重炭酸イオンが中和して炭酸になり、炭酸は二酸化炭素と水に変換され、二酸化炭素は肺から排出されて血液・体液のpHが一定に維持される。
【炭酸脱水酵素は重炭酸緩衝系の働きを高める】
炭酸脱水酵素(Carbonic Anhydrase)は炭酸(H2CO3)から水(H2O)を抜き取り二酸化炭素(CO2)にする酵素です。
私たちは酸素を体内に取り込んで、ミトコンドリアで糖や脂肪を分解してエネルギー(ATP)を産生しています。肺から取り込んだ酸素は血液中に拡散し、赤血球中のヘモグロビンに結合して全身の細胞に運ばれます。
この酸素呼吸の副産物として細胞内で二酸化炭素(CO2)が産生されますが、これは体外に排出する必要があります。この二酸化炭素は細胞外に拡散し、何種類かの方法で血液中を輸送されます。
10%未満は血漿中に溶けて、約20%はヘモグロビンと結合して運搬され、大半は炭酸(H2CO3)に変換されて輸送されます。
赤血球中に炭酸脱水酵素(Carbonic Anhydrase)があって、二酸化炭素が炭酸と重炭酸イオンに変換する作用を助けます。
肺では赤血球の炭酸脱水酵素が重炭酸イオンを二酸化炭素に戻す作用を助け、できた二酸化炭素は拡散して肺から排出されます。
この反応は酵素がなくても自然に起こりますが、炭酸脱水酵素は触媒作用によってこの変換速度を100万倍に加速することができます。
つまり、炭酸脱水酵素は二酸化炭素ガスを血液中に溶解させることによって呼吸によって排出できるようにしています。(下図)
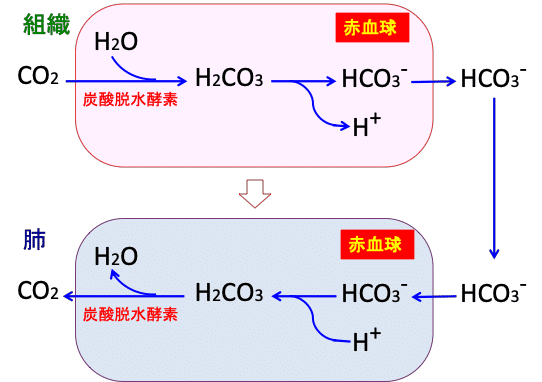
図:体内の組織で産生された二酸化炭素(CO2)は拡散して赤血球内で炭酸脱水酵素で重炭酸イオン(HCO3-)に変換されて血清中に溶け込む。重炭酸イオンは肺で赤血球中の炭酸脱水酵素によって二酸化炭素に変換され、肺から排出される。
炭酸脱水酵素は二酸化炭素と水を炭酸(重炭酸イオン+水素イオン)に変換する酵素で、1933年に牛の赤血球から発見されました。その後、体内の全ての細胞に存在することが明らかになっています。
哺乳類の炭酸脱水酵素は構造や局在の異なる10種類以上のアイソザイムが知られています。
炭酸脱水酵素は重炭酸緩衝系を促進することによって、体液や細胞内の酸塩基平衡の制御に重要な働きを担っています。
つまり、動物において炭酸脱水酵素の主たる機能は、二酸化炭素と炭酸水素イオンとを相互変換することで、血液や他の組織の酸-塩基平衡を維持し、組織から二酸化炭素を運び出す補助をしています。
【野菜や果物は体をアルカリ化し、肉は酸性化する】
体内の酸塩基平衡は食事の影響を受けることが知られています。食品は栄養成分に応じて体に酸性またはアルカリ性の負荷をかけますが、体はこの負荷を緩衝して、安定した血液pHを維持します。
高タンパク食品(肉、魚、乳製品)は有機酸と硫酸の生成を増加させ、酸の負荷を増加させます。野菜や果物のようにクエン酸カリウムやリンゴ酸カリウムなどのカリウム塩が豊富な食品は、重炭酸カリウムに代謝され、体液をアルカリ化する効果があります。
果物や野菜などのアルカリ性食品が少なく、肉や魚や乳製品などの酸性食品を多く含む食事は、血液が酸性に傾いた状態(代謝性アシドーシス)を導き、そのことが様々な病気の発症に影響を与える可能性が指摘されています。
アルカリ食の一般的な概念は、血液をアルカリ性にするというものですが、血液のpHは7.35から7.45のアルカリ性pHで非常に厳密に調整されているため、アルカリ食で体内がアルカリ化するわけではありません。同様に酸性食品で血液のpHが酸性状態に変化することはありません。血液のpH緩衝能は高いので、酸性食を多く摂取しても血液pHが酸性化することはありません。しかし、体内の酸塩基平衡において、酸性に傾いた状態に導きます。
食事の酸塩基バランスを表す指標に潜在的腎臓酸負荷(potential renal acid load : PRAL)があります。PRALは以下の式で算出されます。
PRAL(mEq/d)=0.4888×たんぱく質(g/d)+0.0366×リン(mg/d)-0.0205×カリウム(mg/d)-0.0125×カルシウム(mg/d)-0.0263×マグネシウム(mg/d)
つまり、食事中のタンパク質とリンの量は潜在的腎臓酸負荷(PRAL)を増やし、カリウム、カルシウム、マグネシウムはPRALを減らします。
動物性タンパク質は、イオウ含有アミノ酸であるメチオニンとシステインを多く含み、体内で硫酸と水素イオンを形成するため、食事の酸の最大の供給源です。水素イオンは、食事中のリン酸塩の代謝から食事中に提供されます。動物の肉や卵も、体内で水素イオンを形成する成分を多く含みます。動物性タンパク質、特に肉、卵、チーズは、体内で大量の酸を形成する原因となります。
果物や野菜は、クエン酸塩、リンゴ酸塩、グルコン酸塩などの有機アニオンを多く含み、体内で重炭酸塩に変換されます。重炭酸塩は、酸を中和する塩基です。したがって、動物性食品は正の潜在的腎酸負荷(PRAL)ですが、植物性食品は負のPRALを持っています。さまざまな食品のPRALを下の表に示します。一般的に、肉、魚、乳製品、穀類は食事性酸負荷を高め、野菜と果物と豆類はアルカリ性食品と言えます。油脂類は酸負荷はほとんどありません。

表:様々な食品の可食部100g当たりの潜在的腎臓酸負荷(potential renal acid load:PRAL)を示す。PRALがプラスは酸性食品で、マイナスはアルカリ食品になる。(参考:Nutrient. 2020 Apr; 12(4): 1007)
【アルカリ食は寿命を延ばす】
日頃から摂取する食事の潜在的腎臓酸負荷(potential renal acid load:PRAL)が高いほど死亡のリスクが上昇する傾向が認められてます。国立がん研究センターの多目的コホート研究(JPHC研究)からの報告では、食事のPARLスコアが最も低い群に比べ最も高い群では総死亡のリスクが13%増加していました。
Dietary acid load and mortality among Japanese men and women: the Japan Public Health Center-based Prospective Study.(日本人男性と女性における食事性酸負荷と死亡率:日本公衆衛生センターに基づく前向き研究。)Am J Clin Nutr. 2017 Jul;106(1):146-154.
死因別にみると、循環器疾患および心疾患死亡との間で統計的に有意な関連を認め、食事性酸負荷スコアが最も低い群に比べ最も高い群において死亡リスクはどちらも16%増加していました。
他の研究でも、食事の酸性度が高いほど総死亡及び循環器疾患死亡のリスクが上昇することが報告されています。
酸性に傾いた食事が死亡リスクを高めるメカニズムははっきり分かっていませんが、こうした食事により、体重が増え、インスリン抵抗性が高まり、糖尿病・高血圧・脂質異常症といった疾患が引き起こされ、結果として動脈硬化が進むことが想定されています。
したがって、野菜、果物、豆類といった体内のアルカリ度を高める食品を多く摂取することは循環器疾患の予防により健康寿命を伸ばす効果が示唆されています。
【食事中の酸負荷ががんの発生率を高める】
食事の内容とがんの発生率の関連を疫学的に調査する場合、多くは食事の内容をアンケートで調査しています。この方法だと、正確性に欠ける懸念はあります。
肉といっても、脂肪の多い肉と脂肪の少ない肉では発がん作用の程度が異なり、果物も糖分や抗酸化成分やフラボノイドの量が区別できないと、果物が多いだけでは、がん予防にプラスの場合とマイナスの場合があります。
食事の潜在的腎臓酸負荷を測定してがん発生率との関連を解析した研究もあります。このような研究では、酸性食が発がん率を高めるという結果と、関係ないという結果が報告されており、コンセンサスは得られていません。これは、食事の内容をアンケートで調査している事による疫学研究の限界かもしれません。
以下のような研究報告があります。
Dietary Acid Load and the Risk of Pancreatic Cancer: A Prospective Cohort Study.(食事の酸負荷と膵臓がんのリスク:前向きコホート研究)Cancer Epidemiol Biomarkers Prev. 2021 May;30(5):1009-1019.
【要旨】
背景: 現代の西洋型食生活は酸生成食品が豊富である。人間とin vitroの研究は、食事の酸負荷とがん発生とのリスクとの間に潜在的な関連があることを示唆している。しかし、食事の酸負荷と膵臓がんのリスクとの関連を調査した疫学研究はない。この点を明らかにするために前向きコホート研究を実施した。
方法: 95,708人のアメリカ人成人の人口ベースのコホートが特定された。潜在的腎臓酸負荷(Potential renal acid load :PRAL)と正味内因性酸産生(net endogenous acid production :NEAP)を使用して、各被験者の食事性酸負荷を評価した。数値が大きいほど、食事酸負荷が大きいことを示す。Cox回帰を使用して、膵臓がんの発生率のリスク推定値を推定した。
結果: 848,534.0人年(person-years)の追跡期間中に、合計337件の膵臓がん症例が観察された。PRALスコアは膵臓がんのリスクと正の相関が認められた。PRALの高い上位4分の1の群はPRALの低い下位4分の1の群に比べて膵臓がん発生リスクは1.73(95%信頼区間(95%CI):1.21-2.48)であった。サブグループ分析では、PRALスコアと膵臓がんのリスクとの正の関連性は、65歳以上の被験者よりも65歳未満の被験者でより顕著であった。NEAPスコアについても同様の結果が得られた。
結論: 食事の酸負荷が高いほど、膵臓がんのリスクが高くなる。将来の研究では、他の集団や設定での調査結果を検証する必要がある。
重要性: これは、食事からの酸の負荷を減らすことが膵臓がんの一次予防に役立つ可能性があることを示唆する最初の疫学研究である。
1人を1年間追跡すると 1人年(1 person-year)になり、10人を10年間追跡すると 100人年(100 person-years)になります。この疫学研究では、95,708人のアメリカ人成人を848,534人年(person-years)追跡しているので、平均9年間程度追跡されているコホート研究です。この追跡期間に337人が膵臓がんになり、食事の酸負荷との関連を解析しています。その結果、食事の酸負荷が多いほど、膵臓がんの発症リスクが高くなることが示されました。
食事の酸塩基バランスを表す指標には、潜在的腎臓酸負荷(PRALスコア)と推定内因性酸産生量(NEAPスコア)が使われています。
PRAL(mEq/d)=0.4888×たんぱく質(g/d)+0.0366×リン(mg/d)-0.0205×カリウム(mg/d)-0.0125×カルシウム(mg/d)-0.0263×マグネシウム(mg/d)
NEAP(mEq/d)=[54.5×たんぱく質(g/d)/カリウム(mEq/d)]−10.2
いずれも値が高いほうが食事の酸性度が高いことを意味します。食事中のタンパク質とリンの量は酸負荷を増やし、カリウム、カルシウム、マグネシウムは酸負荷を減らします。
膵臓がんは加齢とともに発生率が増えます。膵臓がんは60歳以上になると増えてきます。65歳以上で急速に増えます。
膵臓がんのリスク要因として飲酒や喫煙や糖尿病や肥満があります。これらの要因があるとより若い時点で膵臓がんになります。高齢者の膵臓がんは加齢(高齢)という要因が最も強くなります。
この研究で、「食事性酸負荷と膵臓がんのリスクとの正の関連性は、65歳以上の被験者よりも65歳未満の被験者でより顕著であった」というのは、食事性酸負荷が加齢とは関係なく膵臓がんの発生率を高める要因であることを意味します。
以下のような報告もあります。
Higher diet-dependent acid load is associated with risk of breast cancer: Findings from the sister study.(より高い食事依存性の酸負荷は乳がんのリスクと関連している:姉妹研究からの発見)Int J Cancer. 2019 Apr 15;144(8):1834-1843.
【要旨】
慢性的な軽度の代謝性アシドーシスに寄与する食事要因は乳がんのリスクに関連しているが、これまでのところ、食事依存性の酸負荷と乳がんを調べた疫学研究は無い。登録時(2003年から2009年)に食物摂取頻度アンケートに回答し、適格基準を満たした43,570人の姉妹研究参加者からのデータを使用した。
潜在的腎臓酸負荷(Potential Renal Acid Load :PRAL)スコアを使用して、食事に依存する酸負荷を推定した。スコアが高いほど、タンパク質とリンの消費量が多く、カリウム、カルシウム、マグネシウムの消費量が少ないことを示している。潜在的腎臓酸負荷(PRAL)と乳がんの関連性は、多変数Cox比例ハザード回帰を使用して評価された。
登録から少なくとも1年後(平均追跡期間、7.6年)に診断された1,614例の浸潤性乳がんを特定した。
PRALが高い上位4分の1の群は、PRALが低い下位4分の1の群と比べて、乳がんの発症リスクが高かった(ハザード比: 1.21; 95%信頼区間:1.04-1.41, p=0.04)。
この関連性は、エストロゲン受容体(ER)陰性(最高対最低四分位数のハザード比:1.67 [95%信頼区間:1.07-2.61]、p= 0.03)およびトリプルネガティブ乳がん(最高対最低四分位数のハザード比:2.20 [95%信頼区間、1.23-3.95]、p= 0.02)で顕著であった。
アルカリ性食品の摂取を表す負(マイナス)のPRALスコアのグループは、PRALスコアが0のグループと比較して、ER陰性およびトリプルネガティブ乳がんのリスク低下と関連していた。
食事依存性の高い酸負荷は乳がんの危険因子である可能性があり、アルカリ性食事は発がんを予防する可能性がある。PRALスコアは肉の消費量と正の相関があり、果物と野菜の摂取量と負の相関があるため、結果は、果物と野菜が多く肉が少ない食事がホルモン受容体陰性乳がんを予防する可能性があることも示唆している。
日本人の女性の乳がんは高齢化とは関係なく、年齢調整罹患率も死亡率も増加しています。出産回数の減少や初潮年齢の低下、閉経年齢の上昇など体内のエストロゲン濃度が高い状態が長く続く状況は、ホルモン感受性の乳がんの発生率は高めます。経口避妊薬の使用や閉経後の女性ホルモン補充療法など、体外からの女性ホルモン追加もホルモン受容体陽性の乳がんの発症リスクを上げます。
つまり、ホルモン受容体陽性の乳がんはエストロゲン過剰という発がん要因の寄与が大きいので、食事の酸負荷の影響は相対的に少なくなります。
しかし、エストロゲン受容体陰性およびトリプルネガティブ乳がんでは、エストロゲン濃度は発がんに寄与していないので、食事性の要因が相対的に高くなると言えます。そのため、食事性酸負荷と乳がんの発症の関連性は、エストロゲン受容体陰性およびトリプルネガティブ乳がんで顕著であったことが理解できます。
いずれにしろ、酸負荷が大きい食事はいろんながんの発生リスクを高める可能性があります。したがって、がんの予防において、アルカリ性食品によって食事性の酸負荷を減らし、血液や体液のアルカリ化能を高めることはメリットがあります。
さらに最近の研究では、食事性酸負荷が動脈硬化や糖尿病など生活習慣に起因する疾患に対して影響を及ぼす可能性が示唆されています。慢性腎臓病の発症および進展に食事性酸負荷が関連しているとする多くの報告が集積されています。がん治療においても、食事性酸負荷を減らすメリットは大きいと言えます。
この記事が気に入ったらサポートをしてみませんか?
