
シンプルで美しい「BZ反応」
その名はベロウソフ・ジャボチンスキー反応。
通称BZ反応と呼ばれます。
まずは以下の動画を見て下さい。
このように、周期的に色が変化します。
さらに、反応液をシャーレのような浅い容器に入れておくと、
色の変化が同心円状に広がっていきます。
このように周期的に変化し、同心円状などのパターンを生成する現象は自然界にも見る事ができます。
BZ反応は酸化還元反応で、以下の図のように酸化還元を繰り返すことで色が変化します。
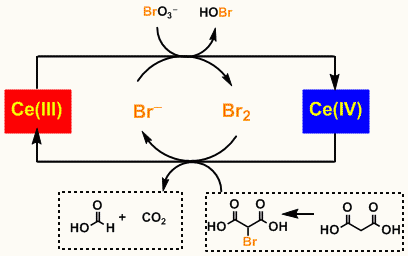
セリウムを用いたBZ反応(https://www.chem-station.com/odos/2009/09/-belousov-zhabotinskybz-reacti.html)
三価のセリウム(赤)が四価のセリウム(青)になる酸化反応 [Ce(III)→Ce(IV)] は、臭化物イオン(Br-)の濃度が高い時に優先的に起きます。要するに、臭化物イオンの量を減らす方向に反応(酸化)が進むわけですね。
一方、四価のセリウム(青)が三価のセリウム(赤)になる還元反応 [Ce(IV)→Ce(III)] は、臭素(Br2)の濃度が高い時に優先的に起きます。臭素の量を減らす方向に反応(還元)が進みます。図に表記している臭素酸イオン(BrO3-)が酸化、マロン酸(HOOC-CH2-COOH)が還元に関わっています。
BZ反応の酸化還元電位を測定してグラフにすると、以下のようになります。

酸化還元を繰り返すことで電位は上下動しますが、次第に振れ幅は小さくなっていき、反応が終わると変化が無くなります。
酸化還元反応に必要な臭素酸塩とマロン酸が消費されてしまうと反応は止まってしまいます。
BZ反応は1951年、ボリス・ベロウーソフがクエン酸回路の研究中に発見しました。ところが、当時、全ての化学反応は安定状態へ収束すると考えられていたため、酸化還元を周期的に繰り返すBZ反応の論文は受け入れられませんでした。

ボリス・ベロウーソフ(https://en.wikipedia.org/wiki/Boris_Pavlovich_Belousov)
それから十年後の1961年、アナトール・ジャボチンスキーは反応を詳しく調べ、セリウム以外の金属塩でも反応が起こることを発見し、発表しました。
ようやく認められたこの反応は、二人の名前を取ってベロウソフ・ジャボチンスキー反応と名付けられました。

アナトール・ジャボチンスキー(https://en.wikipedia.org/wiki/Anatol_Zhabotinsky)
BZ反応は周期的に酸化還元を起こしますが、前述したように媒介となる物質が消費されれば反応は止まります。
......ところが、21世紀になって驚くべき事実が判明します。
2008年、茨城県立水戸第二高等学校で、教師と学生がBZ反応の実験を行いました。反応が停止した後、学生は片づけずにカラオケへ行ってしまいました。週末だったので、反応液は月曜までそのまま放置されました。
そして週明け、反応液を見ると、なんと反応が復活していました!
終了した化学反応が自動的に復活するなんて、普通はあり得ません。
下図は、そのときに行われたBZ反応の結果です。前述した例と同様、縦軸に酸化還元電位、横軸が経過時間になっています。青(上)と赤(下)のグラフは、途中で上下に振れる事がなくなり、反応が終わっているのが分かります。
問題は真ん中のグラフです。一度反応が終わったのに、途中からまた反応が復活しています。
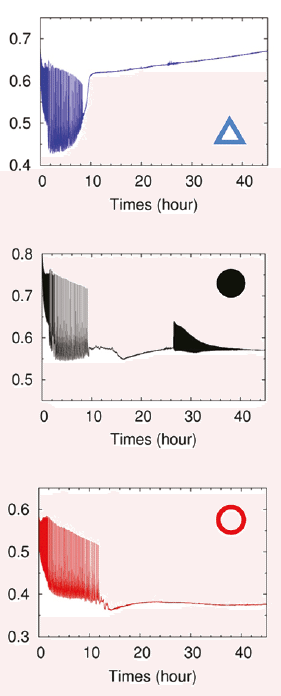
BZ反応の酸化還元電位(https://www.chem-station.com/blog/2011/11/post-314.html)
この真ん中のグラフをよく見ると、下図のように前半と後半を直線で結ぶことが出来ます。
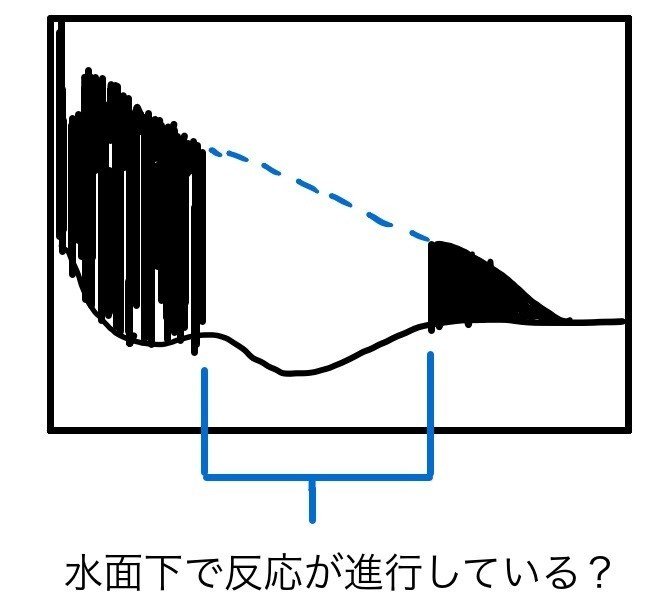
こうして見ると、復活した後半の反応は、前半の続きのように見えます。
そうです、一見、反応は終わったように見えて「実は水面下で反応が進んでいるのではないか」そのように考えられています。もしそうなら、酸化還元電位には表れないという所が興味深いですね。
ちなみに、BZ反応なら必ず反応が復活するわけではありません。ある特定の濃度でのみ起こる現象ということが分かっています。
BZ反応は色の変化で酸化還元反応を確認でき、簡単に実験を行うことが出来るため、演示実験に適しています。
また、一定の模様を周期的に描き、時間経過と共に変化するため、パターン化や散逸構造の研究者からも注目され、コンピュータ科学の視点からも研究されています。
美しく、謎を秘めた化学反応。ベロウソフ・ジャボチンスキー反応には不思議な魅力があります。
いいなと思ったら応援しよう!

