感染症に対するmRNAワクチン、コロナ禍以前の知見。
これが意外と注目されていないというか、こういう視点で語っている人を見たことがないのだが。
コロナ禍以前のmRNAワクチンの実績ってどのくらいあったの?、ってことで調べてみた。
結果、マヂでほとんど真っ当な臨床試験はない。
(("mRNA vaccines") OR ("mRNA vaccine"))
この単語で「Clinical Trial」と「Randomized Controlled Trial」で、2019年以前に限定。
クリックしてみたらわかるけど、たったの4件。そのうちインフルエンザの1件をのぞいてあとは悪性疾患の論文。なので、インフルエンザのを軽く読んでみます。
n数も少なく、H10N8で201名、H7N9で156名。こんだけ年数かけてなんでたった201人とかしか集まらなかったのかは書いてなかったけど。Fig.1とFig.2がどうやって打ったかの方法です(省略)。
で、肝心の結果なんですが、まず検討方法のMaterials and methodsから原文を抜粋しますね。
2.5. Immunogenicity assessments
Immunogenicity was determined by hemagglutination inhibition (HAI) using recombinant, full-length HA proteins for H10N8 (A/Jiangxi-Donghu/346/2013, Medigen) or the A/Shanghai/02/2013XPR8 virus for H7N9 and by microneutralization (MN) assays, using the A/quail/Italy/1117/1965 and the A/Shanghai/02/2013XPR8 viruses for H10N8 and H7N9, respectively, as previously described [18], [19]. Testing for HAI was performed on blood samples collected at days 1, 8, 22, 30, 43, and 84, and testing for microneutralization (MN) assays was performed on blood samples collected at days 1, 22, and 43. Blood samples for HAI persistence testing were collected at approximately 6 and 12 months after the last vaccination. Peripheral blood mononuclear cells (PBMC) were collected at days 1, 6, 22, 30, 43, and 84 and were analyzed by enzyme-linked immunospot (ELISPOT).
Serum antibodies to influenza virus HA proteins (HAI assay) were measured by serial dilution of heat-inactivated sera incubated with the titer reported as the reciprocal of the highest dilution that effectively inhibited agglutination of red blood cells by a specific influenza strain. Serum neutralizing antibodies (MN assay) were measured by serial dilution of heat-inactivated sera incubated with influenza virus and transferred to plates containing Madin-Darby canine kidney (MDCK) cells, with the titer reported as the reciprocal of the highest dilution at which no cytopathic effect was observed. Influenza viruses A/quail/Italy/1117/1965 and A/Shanghai/02/2013XPR8 were used for H10N8 and H7N9 MN assays, respectively [18], [19]. Cell-mediated immune response was assessed by interferon-γ ELISPOT assays of PBMC stimulated with H10N8 and N7N9 HA protein peptide libraries.
結果のFigがこちら。
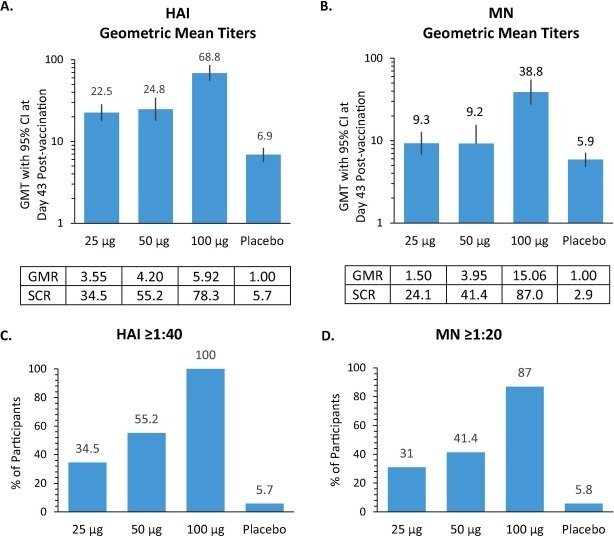
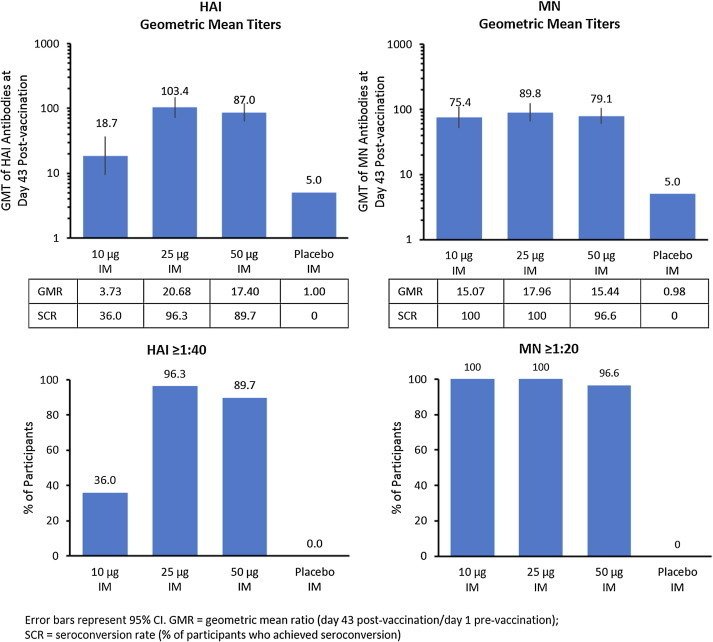

たったこれだけです。感染予防とかの効果はまだです。有害事象についてはたった200人だかを細かい投与方法の違いに分割しちゃっているので1群が少なくなって、検討に耐えるn数じゃありません。
この結果だけでは悪いとは言えません。ただ、以後の引用を見るとこのワクチン自体の進展がなかったことがわかります。
大したオチはありませんが、この程度のものだったということです。
物事は冷静に捉えましょう。
