
がんと自由診療:丸山ワクチン
※ 本記事は有料記事ですが、期間限定無料公開中です。
※ がん自由診療の概略と私の考え方はこちらにまとめています。
※ 最終更新日 2024/8/17 (ver 1.0)
がんと自由診療、第二回。今回は丸山ワクチンについてです。
私はこれまで何人かの患者さんから丸山ワクチンを試したいと要望を受けたことがあります。最初は患者さんの励みになればと協力していましたが、配布元の日本医大の治験状況に疑問を感じてからは対応をやめました。
現在は書類作成や投与を引き受けてくれるかかりつけ医が他にあれば、自由にして下さいとお伝えしています。
丸山ワクチンの大きな問題点は、日本の科学を牽引するはずの大学病院が目的も期間も明かさぬまま、有償治験という謎の制度で効果不明な薬を売り続けている点です。更にこの治験結果は開始から40年以上経過した今でも公表されていません。40万人以上の患者に投与されているにも関わらず、公式HPに載っている臨床試験データは”「基礎と臨床」Vol.17 No1 Jan '83”と示された古い時代のグラフ一つだけ。(2024/7月現在) 通常の医師であれば疑問に思うのは当然でしょう。
治験とは本来いち早くデータを出し、広く患者さんに治療の利益を享受してもらう目的で行われるはずです。しかしこの「有償治験」はどうやらそうではない。延々と有償で薬を配り続ける目的が、科学的根拠の擁立以外にあるとすれば、思い至るのは一つ、お金儲けではないかと私は推測します。
丸山ワクチンは「大学病院が行っている治療」そして「自由診療としては費用が比較的安い」という2点で患者さんに人気があるようです。
しかし大学病院の名を利用して、効果が不明瞭な治療を「医療」として提供していることは大きな問題ですし、ある意味日本における医療への信頼を失墜させかねない行為です。今回は丸山ワクチンに関連するデータお示しし、その問題点と治療に対する考え方についてお伝えしたいと思います。
結論から先に読みたい場合は目次から【5】の考察に飛んで、ご覧ください。
※ 記事内の(*1)などの数字は参考文献です。巻末に一覧を載せています。
【1】丸山ワクチンとは?
丸山ワクチン公式HPに開発の経緯について記載がありますが、簡単にまとめます。
丸山ワクチン(SSM=Specific Substance MARUYAMA)は皮膚結核菌の加熱抽出物で、1944年に皮膚結核の治療薬として開発されました。これを生み出した丸山千里医師が、皮膚結核罹患者にはがん合併が少ない、あるいはがんを患っても進行が遅いという点に着目し、本薬剤ががんにも効くのではと考えたことが開発のきっかけとされています。
丸山ワクチンの成分は主に結核菌由来の糖脂質(ミコール酸・リポアラビノマンナン)とされており、がんに効くメカニズムについては、これらが免疫応答の中心的な役割を担う樹状細胞を活性化し、さらにそれが腫瘍特異的な細胞障害性Tリンパ球やナチュラルキラーT細胞を誘導することによるなどと推測されています。(*1)
免疫的機序でがんを治療するというアイデアは、当時様々な研究がなされました。クレスチン・ピシバニールといった免疫療法の薬剤も承認(その後有効性は否定)された時代に、この丸山ワクチンも効果が期待できる臨床報告が多く発表されたことから、1976年11月にゼリア新薬より抗悪性腫瘍剤として製造承認申請が行われました。結果的に有効性が確認できないと判断され承認には至りませんでしたが、厚生省は引き続き試験・研究を行う必要を認め1982年から特例として丸山ワクチンを有償治験薬とする措置をとりました。
丸山ワクチンはSSM-A, SSM-Bという二つの薬剤からなります。SSM-A, Bの内容物は同一で、Aは1ml中に結核菌体抽出物質 2μg、Bがその1/10濃度である0.2μgを含有しています。最初の3年はA-B-A-Bと隔日で交互に皮下注射し、病変がある間はずっとこのままで継続。術後などで転移・再発がなければ週2回にして5年まで継続。最終的には週1回として適宜終了するとHPには記載されています。薬剤費用は2024年7月現在、A 10本, B 10本 (隔日投与で40日分)で9,000円+消費税です。 (*2)
現在に至るまで丸山ワクチンは抗腫瘍薬としては承認されていません。同内容物で濃度を10倍とした薬品であるアンサー20注 (ゼリア新薬工業開発コード: Z-100)は放射線治療による白血球減少抑制剤として認可されており、ゼリア新薬は同薬の開発を現在も進めているようです。(*3)
【2】丸山ワクチンの効果は?
臨床データを後述しますが、その効果の根拠はほとんどが1970年~80年代に書かれた症例報告が元となっています。以前紹介した高濃度ビタミンC点滴療法が現在でも臨床試験を通じて開発が進んでいるのとは対照的に、現在丸山ワクチンに関する論文は発表されていません。更に日本語の報告がほとんどであることから他国では使用されておらず、まさに昭和の日本で流行したガラパゴス治療の一つと言えるでしょう。
【3】丸山ワクチンの副作用は?
これまでの報告からは、問題となる副作用は報告されていません。微熱や注射部位反応を少数例認めている程度です。しかし後述しますが用量によっては、むしろ害となる可能性がデータから示唆されており注意が必要です。
【4】丸山ワクチンの臨床データ
丸山ワクチンの臨床データを以下に示します。問題点は上述したようにほとんどが症例報告レベルのデータであること、また報告は1980年代に集中しており、それを過ぎるとプッツリと途絶えていることです。
当時とは標準治療も何もかもが変わっているのに「副作用が無い、全てのがんに有効」という宣伝文句だけが独り歩きし、安全性も効果も何もデータが無いまま40年以上前のデータをもとに患者に薬剤が販売・投与されています。
症例報告を読む際に注意していただきたいことは、治療と効果の因果関係です。「3た論法(さんたろんぽう)」というものをご存じでしょうか。医学では「ある薬を使った→病気が治った→だから薬が効いた」という理屈は必ずしも成り立ちません。基本的に病気は体が治しているのであって、薬効とは無関係の場合があります。よって薬効の証明には"比較"が必須であり、比較対象のない症例報告は本当に薬の効果を示しているかわからないのです。
(3た論法についてはこちらのHPが詳しいのでご参照下さい)
各文献には今でもweb上で利用可能なものはリンクを貼ってありますので、ご参照ください。一例報告は多数ありますが、どれも似たりよったりでエビデンスレベルは変わらないので、症例数の多い報告に限定して紹介します。
今回は開発の経緯が分かりやすいよう、時系列にデータを並べました。
① 各種悪性腫瘍に対するSSMの使用経験
島根県立中央病院からの症例報告です。合計20例の患者に丸山ワクチンを投与した経過を紹介しています。臓器内訳は胃 9例, 結腸直腸 4例, 肺 2例, 食道・胆嚢・胆管・乳房・卵巣が各1例の合計20例。治療効果は延命効果とKarnofsky効果基準という抗腫瘍効果の判定基準をベースとして筆者が独自に判断しています。この報告では有効 3例, やや有効 1例, 無効 11例, 判定不能 5例と記載されており、有効 3例とやや有効 1例について、詳細が記載されています。簡単に紹介します。
(有効) 1例目は67歳胃がん症例。肉眼的Stage III胃がんに対し根治切除後、化学療法を行いその後SSMを投与され術後7年4カ月時点で生存維持。
(有効) 2例目は29歳胃がん症例。吐血を主訴に紹介され緊急で胃全摘を施行。リンパ節などに癌は遺残し非治癒切除。術後抗がん剤施行。術後6ヵ月目からSSMを使用し約2年生存している。
(有効) 3例目は52歳胃がん症例。吐血を主訴に受診。根治的胃切除を施行したが断端陽性。抗がん剤施行し術後9ヵ月からSSMを使用。2年9ヵ月生存。
(やや有効) 4例目49歳胃がん症例。StageIV胃がんに対し抗がん剤を施行。3か月後からSSM開始。一時的に自他覚症状の改善あり。1年6ヵ月で死亡。
※※※ 解説 ※※※
上記4症例はいずれも当時としては長生きをしており、2例目について筆者は「臨床医の常識では考えられない延命効果」と評価しています。ただあくまで症例報告であり、たまたま長生きした症例を見たという可能性が否定できず、薬効との因果関係についての言及は難しいと考えます。筆者は最後に「癌免疫療法は過大評価も過小評価も避けるべきであり、基礎的研究成績の多くの出現が待たれる」と結んでいます。
② 頭頸部癌患者に対する結核菌体抽出物質(SSM)の使用経験
大阪回生病院よりSSM投与経験例68例の報告です。内22例は根治術後再発予防を目的として、残りの46例は治癒切除不能・再発の状態に対してSSM単独を用いています。
本報告では結果的に全体として予後の延長は認めず、再発予防効果も不明と結論付けられています。ただ治癒不能症例の内2例 (上咽頭がん・硬口蓋原発悪性黒色腫)に腫瘍縮小を認め約1年数ヶ月の生存を得ました。これについて筆者らは、耳鼻科領域では特異な経過を示すことがある組織型でありSSMの効果については疑問が残るが、一般的な自然退縮の頻度から考慮すると2/46例の確率は高率と考えられることから、治療効果の可能性は残ると説明しています。
※※※ 解説 ※※※
報告内容から、筆者らはどちらかといえばSSMに懐疑的な立場であることが読み取れますが、一部の症例に認めた奏効については治療効果の可能性があると述べています。上咽頭がん・悪性黒色腫は共に免疫原性が比較的高い腫瘍であり免疫療法の効果が出た可能性はあるかも知れません。
③ 共同研究によるSSMの癌免疫療法
CHEMOTHERAPY,28(2), 171-177, 1980
本報告はSSMを100例の患者に投与した症例報告です。100例の内訳は胃がん 47例, 大腸 23例, 他、肝胆膵・食道・肺・乳房・子宮・卵巣 各数例ずつとなっています。SSMは主にB液を隔日4週間以上投与されました。SSM+抗がん剤併用とSSM単独についてそれぞれ効果が報告されています。
抗がん剤併用症例は81例で、マイトマイシンC, 5-FUを含む多剤が併用され客観的改善 18.8%, 主観的改善 23.1%, 1年生存割合 26.1%でした。
SSM単独使用症例は19例で、客観的改善 5.9%, 主観的改善 23.5%, 1年生存割合 5.9%の結果でした。SSMによると考えられる副作用は認めませんでした。
抗がん剤+SSM併用胃がん症例32例と、過去に抗がん剤治療のみを行った66例をカルテから抽出し比較をしたところ、腫瘍縮小を認めた患者割合は21.9% vs 21.2%と差は認めませんでした。しかし生存期間では、生存期間中央値 5.5ヵ月 vs 2.9ヵ月、1年生存割合 28.1% vs 1.5%, 2年生存割合は 9.4% vs 0%とSSM併用患者で良好な傾向を認めました。
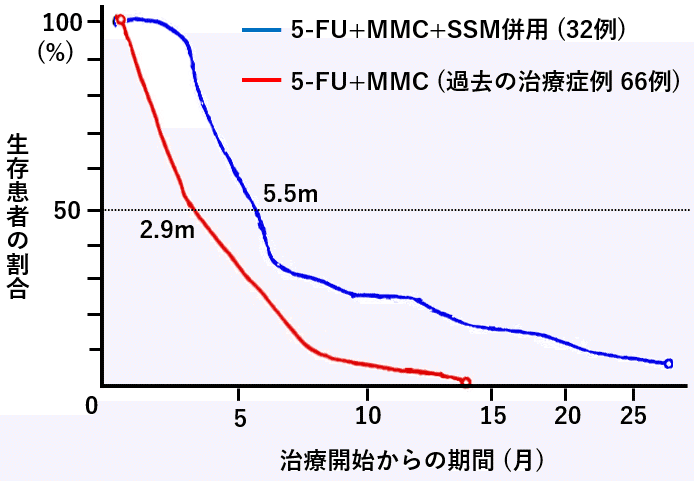
目盛りの不整は元データのまま表現しています。MMC: マイトマイシンC
※※※ 解説 ※※※
比較対象が過去の症例であり、患者背景が同じでないため確定的な判断は下せませんが、SSM併用患者の生存曲線は近年の免疫チェックポイント阻害薬でよく見るtail plateau (テールプラトー)型にも見え、SSMの効果が同様のメカニズムに拠るとすれば、一部の患者には効果を期待できそうな印象は受けます。しかし結論的なデータとは言えず、抜本的にはやはり無作為化比較試験が計画されるべきデータと考えます。
④ 丸山ワクチンを使用し長期生存した転移性肝癌60例
日本医科大学ワクチン療法研究施設からの報告で、昭和54~58年までSSMを3年以上使用した3,800例の内、肝転移を伴っていた60例について報告されています。原発巣は胃26例, 腸 18例, 胆膵 10例, 他に食道・乳房・卵巣・甲状腺が各々1-2例でした。これらの症例には手術や抗がん剤など他の治療も行われており、根治目的の手術を行われた症例も含まれていました。生存年数は3-4年が19例, 4-5年が22例, 5年以上が19例でした。

※※※ 解説 ※※※
上記の表では化学療法・手術との関連性が別々に記載されており、手術と抗がん剤両方を併用された患者も居る中で、何が患者の生存に一番寄与したのかが分かりづらいデータです。ただ進行症例でも長期生存している症例があることは見て取れます。
筆者らは「今回の調査では、化学療法との併用よりむしろSSM単独で長期生存の可能性が大きい結果」という旨の記載しており、末期患者には化学療法剤による不利益があると解釈していますが、これは逆に化学療法が不要な、状態の良い症例が選別されたためにSSM単独の方がより生存期間が長い結果が出た、という可能性も考えられます。この結果から言えるのは「長期生存した患者にSSM使用者が居た」というだけで、SSMが生存期間を延長させたのかどうかは分からないという点では、他の症例報告と本質的には変わりません。
⑤ その他の症例報告
その他にも症例報告は幾つか発表されておりますが、長期に奏効した患者を一部認めた、という点において概ね同様の結論となっていますので割愛します。
・頭頸部悪性腫瘍に対する免疫療法 -丸山ワクチンの使用知験-
(耳鼻咽喉科展望 第21巻, 第2号, 1978年)
・骨悪性腫瘍におけるSSMの治療成績
(日本医事新報 2932, 1980年)
・消化器癌患者に対するヒト型SSM投与の臨床病理学的検討
(癌の臨床 第26巻, 第8号, 1980年)
・進行・再発子宮癌に対するSSMの治験成績
(臨床婦人科産科 第35巻, 第2号, 1981年)
⑥ SSMによる進行癌の免疫化学療法
例数は違えどいずれも症例報告ばかりであったSSMの効果の検証目的に計画された多施設共同二重盲検化比較試験です。東北大学が主体となって実施されました。対象は切除不能あるいは進行再発の胃・大腸・肝胆膵・肺癌患者です。プロトコールに定めた幾つかの化学療法に併用する形で、SSMあるいはプラセボ(生理食塩水)を隔日皮下注射しました。当時CTは一般的でなかったため腫瘍縮小評価はレントゲンあるいは身体所見により計測されました。
363例が登録されましたが、151例が対象外・プロトコール違反で除外・脱落され(ほとんどが食道癌の誤登録) 残ったSSM群105例, プラセボ群 107例が解析対象となりました。最も登録が多かったがん種は胃がん(134例)でその他のがんは数例ずつの登録でした。
結果、抗腫瘍効果は完全奏効 0% vs 0%, 部分奏効 8.7% vs 10.8%, 不変 44.7% vs 35.3%で両群に有意差はありませんでした。生存期間中央値は133日 vs 109日でSSM群に良好な傾向でしたが有意差はありませんでした。胃がん症例に限定した解析も施行されましたが同様の結果でした。食欲・倦怠感・疼痛・体重・PS(全身状態の指標)についても、いずれも有意な差は認められませんでした。SSMによると考えられた副作用は発熱(1例)でした。

※※※ 解説 ※※※
当時としては良く計画された臨床試験であったと考えます。SSM群は中央値で24日生存期間が長い傾向を示しましたが結果として2群に有意差は認めませんでした。SSM群のごく一部に長期生存症例がおり、好意的にとらえれば免疫療法としての効果の可能性も否定できません。ただこれだけのデータでは何とも言えず、試験全体で見れば少なくともほとんどの患者には無効であり「効果は否定的」という解釈になるでしょう。
⑦ 胃癌非治癒切除および切除不能症例に対するSSMの比較試験
こちらは愛知がんセンターを中心とした地域で実施された比較試験です。
非治癒切除あるいは切除不能胃がん症例を、各々化学療法単独群 vs SSM (A液を週2回) 皮下注射併用群とに分け治療効果を比較しました。本試験はプラセボ対照としなかったことから、化学療法単独群に割り当てられた患者の内25%に、患者希望・主治医判断などでSSMが投与されてしまいました。そこでプロトコール違反が無かった症例のみの解析(解析①)と、実際に投与された薬によって患者を分けた解析、すなわち患者希望・主治医判断でSSMが投与された症例も含めた解析(解析②)が施行されました。
結果、解析①では生存期間中央値が単独群 10ヵ月 vs 併用群 14ヵ月と併用群良好であり、特に生存曲線の後半においては統計学的に有意な成績でした。解析②も同様に生存期間中央値は単独群 10ヵ月 vs 併用群 15ヵ月でした。腹膜転移あり、なしでのサブグループ解析も行ったところ生存期間中央値は解析①・②共に単独群 9ヵ月 vs 併用群 12ヵ月の結果で併用群で良好でした。腹膜転移なし症例においても良好な傾向が認められました。

※※※ 解説 ※※※
これが丸山ワクチン公式HPに掲載されている文献です。文献⑤と同じ無作為割付による比較試験ですが、こちらの試験はそれと比べてデータの信頼性が落ちます。理由を以下に述べます。
(1) プラセボ対照としなかったため被験者・評価者が盲検化されておらず、様々なバイアスが入る余地があったこと。
(2) 患者の多数が違反・脱落扱いとなり、その患者を除外して解析したためそもそもランダム化が崩れてしまっていること。患者背景では有意差無しとなっていますが、患者の経済力・家族のサポート力など目に見えないパラメータも無作為割付することがランダム化の目的ですので、この時点で既にランダム化比較とは呼べません。自ら選んでSSMを行った患者を含んだ解析②では解析①より差が開いています。筆者らは薬の効果がはっきり出たと解釈しているようですが、元気で治療に積極的な患者がよりSSM群に流れた結果、SSM群の生存が良くなっただけかも知れません。
(3) ランダム化の方法が封筒法であること。封筒法は担当医が中身を空けて割付を確認出来てしまうため、現在ではランダム化の方法として推奨されていません。
これらの点は筆者らも考察で反省点として述べています。素直に生存曲線を見ればSSM良好な結果と言えますが、このように多数のバイアスを含んだ結果であるという前提でデータを解釈する必要があると思います。
丸山ワクチン公式HPが患者さんに正しい情報を提供しようと考えるのであれば、より信頼性の高いデータである⑤、あるいは⑤と⑥の両方の結果を併記すべきでしょう。しかしそうしていないところに、都合の悪いデータを隠したいという意図が透けて見える気がしてなりません。
⑧ SSMの悪性腫瘍術後症例の生存率に及ぼす効果
本研究は非根治的切除を行ったがんの症例に対し、術後SSMを開始した時期と、その後の生存期間の関係について調査したものです。術後3か月以内に開始した群(早期群)と、7-12ヵ月の間に開始した群(晩期群)に分けて術後24ヵ月時点での生存割合を調査しました。少なくとも1クール(40日間) SSMを使用した患者でのみ評価を行っています。
結果、胃がんにおいては早期群 vs 晩期群:46.63% vs 35.71%。肺がんにおいては 53.66% vs 35.71%。大腸癌については 42.56% vs 18.60%といずれも早期開始群で良好でした。Stage IV症例に限っても、胃がん 35.93% vs 28.57%、肺がん 44.44% vs 33.33%, 大腸癌 38.71% vs 14.29%と早期群良好な結果でした。
※※※ 解説 ※※※
結論として筆者らは、SSMは診断早期から開始すべきとまとめています。早期開始群が生存良好な傾向は見て取れますが、問題は早期群と晩期群の患者背景が同じかという点です。晩期群で何らかの原因(術後の合併症や体調不良等)でSSMの開始時期が遅れた患者が含まれていたのであれば、それはただ治療前の全身状態の差を見ているだけの可能性があります。データの信頼性を担保するため、患者背景まできちんと調査をすべきであったと思います。また3-6ヵ月の間に開始した症例との比較がない理由が不明です。都合が悪かったので意図的に外した可能性は否定できません。
⑨ 非治癒切除胃癌症例へのSSM単独 vs 化学療法併用の効果比較
⑦と同じ筆者からの報告です。本研究では過去のカルテから胃癌に対し非治癒切除を行った症例を抽出し、その後の治療としてSSM単独69例と化学療法を併用した74例について生存期間の比較を行っています。患者の癌の転移状況等の背景は統計学的な偏りはありませんでした。化学療法はFT-207, 5-FU, MFC療法, MF療法など様々な治療が使用されていました。
結果、生存期間中央値はSSM単独群で23ヵ月、化学療法併用群で13ヵ月と、SSM単独で予後良好な結果でした。肝転移例・腹膜転移例・漿膜浸潤例・リンパ節高度転移例いずれにおいてもSSM単独で生存期間は良好な結果を示しました。
※※※ 解説 ※※※
SSM販売元である日本医大からの報告は、基本的にSSMの効果を支持する内容ばかりなので話半分に読む必要があるのですが……。
この報告はSSM単独の方が生存予後が良かったという結果を示しています。今回は患者背景についての言及があり、⑦の報告よりは信憑性が高いと考えられますが、限られたデータであり比較対称性が担保されているかまでは微妙です。切除不能胃癌においては、現在の標準治療ですらようやく生存期間中央値が2年に達するかどうかというところなのですから、多少ステージの低い症例が混じっている可能性があるとはいえ、この時代SSM単独で23ヵ月の生存期間中央値は"良すぎ"です。何らかの患者選別がベースにあるとみるべきでしょう。また本研究では非常に多くの統計学的検定を行っていますが、多重性など統計学的な問題点はないのかが個人的には気になります。
カルテを利用した後ろ向き研究の限界とも言えますが、筆者らが「本調査成績が免疫療法の評価における基礎的資料になりうる」と結語でまとめているように、この結果で効く効かないを判断するのではなく、今後もっとエビデンスレベルの高い研究をするための材料として用いるべき結果です。
⑩ SSM10年以上使用の施行胃癌・大腸癌症例の報告
日本医事新報 第4291号, 67-72, 2006年
日本医事新報 第4314号, 63-68, 2006年
1980年代後半以降丸山ワクチンの臨床報告はプツリと切れ、次はこの2006年の報告となります。これも日本医大からの報告です。主に1980年代~90年代からSSMを開始し10年以上使用している患者について報告したものです。
論文というより半ばエッセイのような内容で詳細は割愛しますが(リンク先で無料で読めます)、これまでの報告同様、長期に使用・生存した症例がいたというだけのものです。考察にはSSMのマイナスイメージが払拭され、もう一度日の目を見ることを切望する筆者らの主張が切々と書かれています。
20年ぶりにデータを出すなら長期生存症例の予後因子探索でもしてくれれば有用なのにと思いますが、恐らくそのようなデータは取れていないのでしょう。何のための治験で、何のためにデータ収集をしているのか改めて疑問を抱かざるをえない内容です。
⑪ IIIB期子宮頸がんに対する放射線療法とZ-100の併用試験
(A) Phase II Jpn J Clin Oncol. 2006;36:570–577.
(B) Phase III Gynecol Oncol. 2006;101:455-63.
近年ゼリア新薬が主体となって開発しているZ-100のデータも紹介します。Z-100はSSM-A液と内容物は同じで10倍の濃度(20μg)を含んだ薬品です。Z-100は放射線治療の白血球減少に対して保険収載されている薬剤ですが、放射線治療の感受性を高める効果が期待され本邦において臨床試験が計画され、適切な投与量を探索するPhase II試験と、治療効果の検証をしたPhase III試験が行われました。
両試験ともStage IIIB期子宮頸がんに対し全骨盤照射+腔内照射を行い、Z-100は週2回皮下注射されるプロトコールです。照射終了後もメンテナンスとしてZ-100は2週間に1度皮下注射され、1年以上継続。放射線治療中は化学療法や免疫療法の併用は許可されませんでした。
Phase IIのランダム化非盲検比較試験(上記文献A)では2μg, 20μg, 40μgの3用量でZ-100の投与が行われました。各々36例, 39例, 35例の患者が割付けられました。結果、投与量が多くなるほど治療終了後の腫瘍の縮小効果は上昇し、放射線治療終了時点での奏効割合は各々72.2% vs 82.1% vs 91.4%でした。特に大きいサイズの病変は用量増加によって縮小割合が増加する傾向にあり、小~中サイズの病変では差は認めませんでした。5年生存割合は各々 59.2% vs 59.6% vs 47.4%と40μg群で低い傾向にありましたが有意差は認めませんでした。
本研究の結論としては40μgが最も強い抗腫瘍効果を認めたため、この用量でPhase III試験において生存期間の検証を行う結果となりました。

この結果を受けてもう一つのPhase III試験(上記文献B)が行われました。放射線治療+Z-100を0.2μg vs 40μgの二群で併用したランダム化二重盲検化比較試験です。(0.2μgはSSM-B液と同じ) 本来比較対象はプラセボであったはずですが、当時の日本においてプラセボ対照は被験者に受け入れられづらいであろうと研究者らが判断し、対照群は0.2μgに設定されました。
221例の子宮頸がん患者を0.2μg群 vs 40μg群に各々110例, 111例割り付け、放射線療法に各々の量のZ-100をPhase IIと同様に併用投与しました。
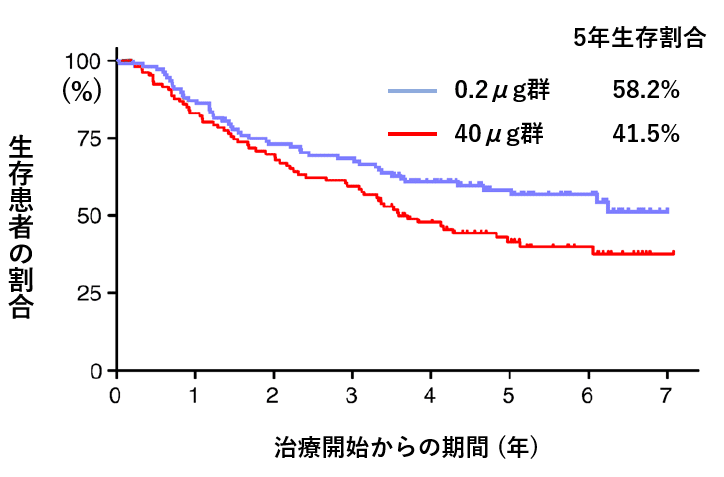
この試験の結果は衝撃的なもので、腫瘍の奏効割合は0.2μg群 vs 40μg群各々93.5% vs 91.5%と差を認めず、さらに5年生存割合は58.2% vs 41.5%でむしろ0.2μg群で有意に良好で、病状が悪化するまでの期間も0.2μg群で良好という結果でした。
※※※ 解説 ※※※
Phase IIIの結果を受けてPhase IIの結果を見直すと、やはり40μg群は生命予後が悪い傾向にあり高用量のZ-100はむしろ患者の生命予後を悪くする可能性が示唆されました。0.2μg群の生存期間は過去の試験からすれば良好な成績と筆者らは考察していますが、比較対象がプラセボではないため本当に良い治療であるのかが判断できません。結果的に本試験においてZ-100の効果は検証できず、将来的にプラセボ対照の試験を再計画する予定となりました。
ちなみに本試験においては発熱、注射部位反応、肝酵素上昇、頭痛、皮疹、関節痛、帯状疱疹などの副作用を少数例に認めましたが重篤なものは観察されませんでした。
⑫ Stage IIB-IVA子宮頸がんへのZ-100プラセボ対照比較試験
上記試験が何とも言えない結果に終わったことを受けて、再度プラセボ対照のPhase III試験が計画されました。本試験では既に標準治療となっていたシスプラチンの放射線治療への上乗せは許容され、Z-100は0.2μgを前述の試験と同様のスケジュールで投与されました。
249例の患者がZ-100群 vs プラセボ群に各々123例 vs 126例割り付けられました。患者の死亡イベント発生が予測より少なかったため、モニタリング委員会より追跡期間5年での結果公表が勧告されました。結果、各群の5年生存割合はZ-100群 vs プラセボ群各々で75.7% vs 65.8%で、Z-100群で良好な成績でしたが統計学的な有意差は認めませんでした。化学療法併用の有無に関わらずZ-100群で良好な傾向を示し、特にStage IIIの患者においては良好な結果でした。
奏効割合は99% vs 99%で差を認めませんでしたが、完全奏効に至った患者数はZ-100群で多い傾向でした。無再発生存期間は両群で差を認めませんでした。有害事象に明らかな差は認めませんでした。

※※※ 解説 ※※※
ゼリア新薬がJGOGという日本の婦人科がん研究グループの協力の下、キチンと効果を検証しようと試みた点は評価できます。結果も統計学的な有意差は無かったもののZ-100群で良好な結果であり、これら対象患者に対しては本薬剤を使用する意義があるかもしれません。(ただし後述するとおり、本試験のあと同様の追試が行われましたが、その結果でも生存の有意差は認められませんでした)
データでは再発率(無再発生存期間)に差が無かった割に生存に差がついた点について、筆者らは理由が不明であると前置きを述べつつ「再発をしても免疫療法の効果で死亡には至らなかった症例がいた可能性がある」と考察しています。
【5】 臨床データからの考察
以上、丸山ワクチンに関連する臨床データをお示ししました。
多くは症例報告で本当に効果があるのか結論づけるのは難しいと考えますが、比較試験も含めて「一部の患者には奏効する可能性がある」という点においては昨今の免疫療法と似た感じを受け、期待したい気持ちはあります。しかし有効な対象患者・がん種は不明瞭であり、むしろデータを素直に解釈すれば「ほとんど効果が無い」とさえ言える結果です。
さらに丸山ワクチンは至適量が未だ不明であり、⑪文献の結果から、増量するとむしろ命を縮める可能性がある点も見逃せません。つまり「ほとんど効果が無い」だけでなく「一部の患者には害をもたらしてる」可能性が否定できないからです。SSM-Aは2μgですが、これが一部の患者にとって多すぎる可能性については検証されているのでしょうか。「副作用が無い」という宣伝文句も観察できる副作用を認めなかっただけで、そのじつ命を縮めているとしたら?症例報告では効いた症例ばかりに目が行きがちですが、有害であった症例が紛れていた可能性にも目を向けるべきだと思います。
現在標準治療に使われている抗がん剤も同様に、一部の患者には害になっているのが現状です。しかし科学的データで効果が望める対象と利益・不利益のバランスを示しているからこそ、医学として信頼のある治療になりえています。
臨床試験を行うには多額の費用がかかります。⑥の文献の生存曲線を見る限り「がん患者」という広いくくりで試験を計画するには、期待できる効果が低すぎて有意差を出せないであろうということは日本医科大学の研究者も認識しているであろうと思います。しかし臨床試験に多額の費用を投じて失敗するよりは、真偽は不確かなまま細々と売れ続けてくれればいいという方針のままでは、まさに私が過去の記事で書いた「効果の真偽がグレーの方が都合が良い」という自由診療の闇そのものになってしまいます。
これまでのエビデンスを総括すると、患者の状態やがんの種類を問わず効果があるという公式HPの記載は誇張を含んだ表現です。根治術後の使用も含めた長期使用者の割合を長期生存例のように見せている点も、医学というより商売を考慮したやり方のように見えます。
がん患者さんは1%の可能性であっても藁をもつかむ思いで自由診療にすがるものです。日本医科大学は今後も丸山ワクチンを有償で配布するつもりであれば、キチンと有効性・安全性を確認する責務があります。それが果たされなければ丸山ワクチンはこの先もずっと信頼に値する治療にはなりえないでしょう。
一方、ゼリア新薬がきちんとデータづくりに取り組んでいる点は評価でき、今後に期待したいと思います。⑫の文献ではプラセボと比較し明らかな有意差はないものの、生存曲線はZ-100が有効である可能性を示唆しており、子宮頸がん患者の放射線治療との併用においては希望が持てる印象です。ただこの結果が出た後ゼリア新薬は、同様の試験をアジア7か国で合計700例規模の患者を集めて追試(NCT02247232)しています。既に2021年には解析が終了しているようですが、主要評価項目の全生存期間の延長を示せなかったと報告されています。(*4)
⑫の文献の差が再現性のある結果であれば、700人規模の臨床試験を行えば恐らく有意差は出るはずです。それなのに出ていないということは、効果が不安定、あるいは効果を望める対象が絞れていないことに起因するのかも知れませんが、試験結果はまだ論文化していないので何とも言えません。
子宮頸がんの化学放射線治療においては近年免疫チェックポイント阻害薬の併用効果が示すデータが出てきています。(*5) このような時代に同じ免疫治療であるZ-100を果たしてどのように使うべきか、そしてZ-100が効果をもたらす適切な対象患者は誰なのか、安全性はどうか、ゼリア新薬には引き続き研究を進めて欲しいと思います。
【6】 まとめ
本記事のまとめは以下の通りです。
丸山ワクチンの有効性を示すデータの多くは症例報告であり、信頼度の高い比較試験では一度も有意な結果は出ていない。
ごく一部の症例において有効である可能性はあるが、効果が期待できる患者像・がん種は不明である。
「どんながんにも効く」と言えるデータは無い。子宮頸がんの放射線療法への併用が有効かもしれないが、大規模な追試においても有効性を示せなかったと報告されており、現時点で推奨は出来ない。
「副作用はない」と宣伝されているが、用量によっては生存期間をむしろ短縮させる可能性が示唆されている。適切な用法・用量は判明しておらず、これまでの報告の中で、投与がむしろ有害であった症例が存在した可能性が否定できない。また近年劇的に変化する治療薬、特に免疫チェックポイント阻害薬との相互作用は不明であり安易な併用は避けるべきであろう。
日本医科大学の有償治験は目的も試験期間も不明であり、一般的な治験とは一線を画すものである。本記事を参考にして丸山ワクチンが価値のある治療か良く考慮された上で、治療を受けるかを検討していただきたい。
以上です。
本治療については新しいデータが出次第、随時更新していく予定です。
この情報が皆様の役に立てば幸いです。
ご質問はX (旧Twitter)までダイレクトメールでお送りください。質問いただいた内容が他の方にも役立つ場合、個人の特定につながる情報を削除した上、このページに追記させていただくことがあります。
無料期間中はどなたでも質問可能ですが、有料化したのちは記事購入者のみの特典となります。ご了承ください。
参考文献
*1 日本医科大学医学界雑誌 2017;13(3) 140-144
*2 丸山ワクチン公式HP
*3 丸山ワクチンとがんを考える会HP
*4 ゼリア新薬第68期株主通信
*5 Lancet. 2024;403:1341-1350.
