
【大学化学への梯】なんで過酸化水素の酸素の酸化数は-1なの?
こんにちは やまたくです
今回紹介する話は大学受験で化学を使う人には是非理解してもらいたい内容になっています。
標題の疑問に答えるためには酸化数とはどのようにして決定されるのかを説明できなくてはなりません。
皆さんは酸化数の定義を正確に言えますか?
実は高校の教科書には正確な定義は書かれていません
酸化数の定義?らしいことと計算方法だけは記されています…
ちなみに日本化学会では
「結合に使われている電子対を電気陰性度の大きいほうの原子に割り当て、原子の酸化状態を表わしたものである」
とされています。
このことを前提に本題に戻ります。
通常、酸素の酸化数は-2ですが、過酸化水素の酸素の酸化数はどうして-1になるんでしょう……
日本化学会の示す酸化数の定義にしたがって説明したものが下記になります。

少しわかりにくいので順々に読み解いていきましょう。
最初のポイントは電気陰性度は酸素の方が水素より大きいということです。
つまり、酸素原子と水素原子が隣り合っているとき、水素原子の電子は酸素原子に引き寄せられる(割り当てられる)ということです。

続いて水分子について見てみましょう。
もともと水素の価電子は1個、酸素の価電子は6個です。しかし、酸素の方が電気陰性度が大きいので、水素の電子は酸素に引き寄せられます。そのため2つの水素原子の電子は酸素に割り当てられ、結果的に酸素の酸化数は–2になります。
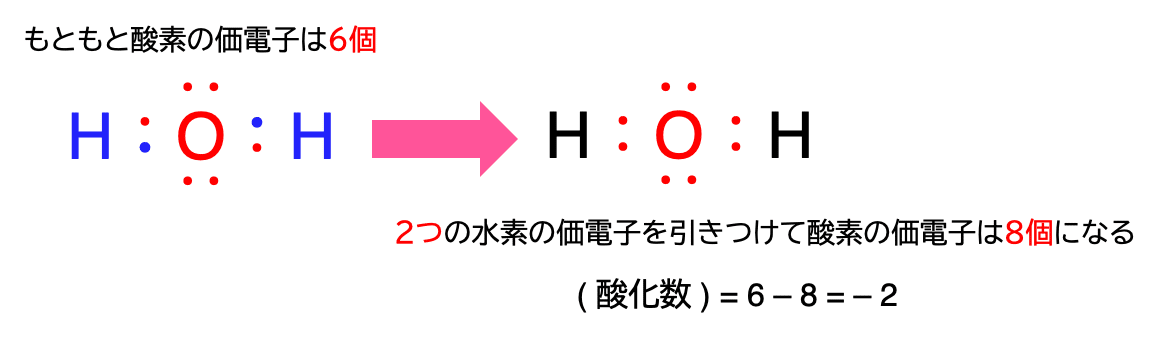
最後に過酸化水素分子についてみてみましょう。
過酸化水素分子と水分子の違いは酸素原子と酸素原子が隣り合って並んでいるということです。この場合、酸素と酸素の間にある電子は、電気陰性度に差がないので、どちらか一方に割り振られるということはありません。そのため1つの水素の電子が酸素に割り当てられ、結果的に過酸化水素の酸化数は–1になります。

結果的には電気陰性度がなんなのか、そして酸素と水素だと電気陰性度はどちらの方が大きいのかがわかっていればそんなに苦労はしません。
また、今回紹介した例は他の化合物でも応用できることなので化学を受験に使う高校生の皆さんは是非理解しておいてもらえると嬉しいです。
長くなりましたが、今日はこれくらいにして…
駄文でしたが最後まで読んでいただいた皆様、本当にありがとうございます。
いいなと思ったら応援しよう!

