
07.遊んでわかる!iPS細胞の研究:超ECO祭2024 訪問記 07
同志社大学 商学部 瓜生原葉子(以下敬称略)研究室(以下瓜生原ゼミ)は、2024年11月09、10日にイオンモールKYOTOで「超ECO祭2024」を催した。なお、私は10日に参加した([1])。
「超ECO祭2024」のブースの1つである「遊んでわかる!iPS細胞の研究」で、京都大学iPS細胞研究所(CiRA)は、人工多能性幹細胞(induced pluripotent stem cells:iPS細胞)の基礎知識を紹介し、iPS細胞を展示した(図07.01,図07.02,図07.03,図07.04,[2],[3])。



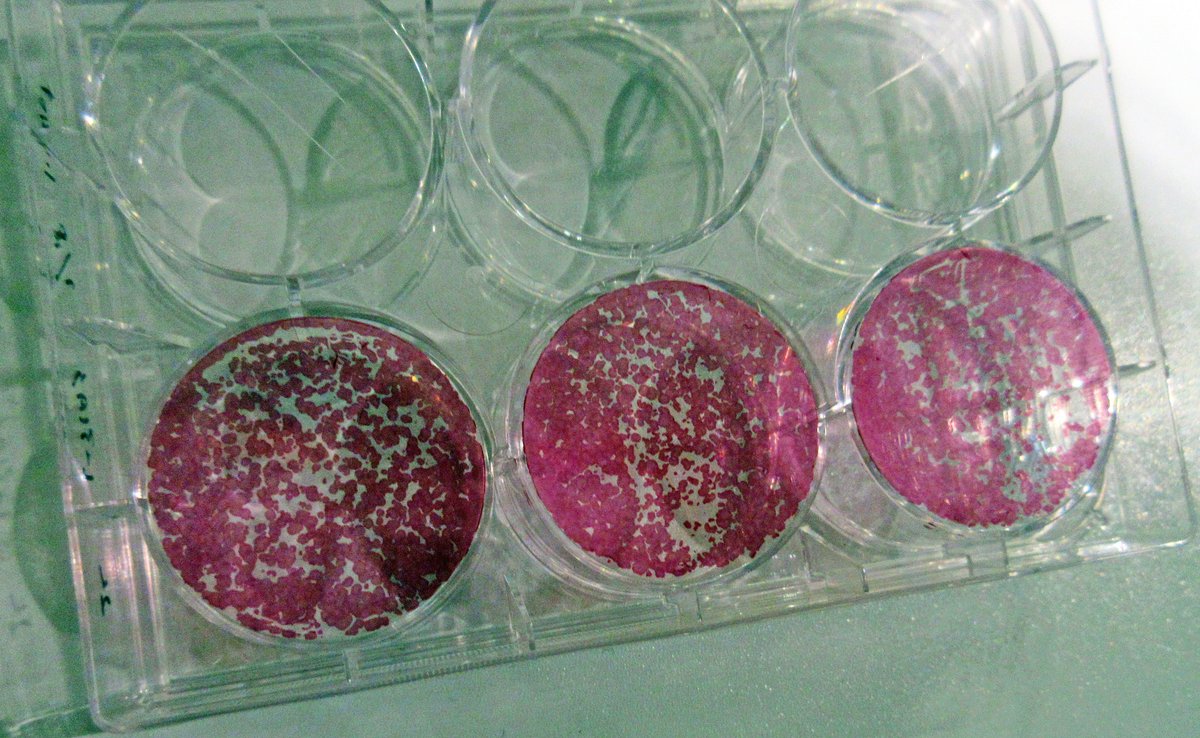
ここで、興味深いiPS細胞関連研究のいくつかを以下に示す。
01.2024年01月24日、高山和雄 講師(CiRA増殖分化機構研究部門)らの研究グループは、横川隆司 教授、藤本和也 助教(共に京都大学大学院工学研究科)、長尾美紀 教授(京都大学大学院医学研究科)らと共同で、三次元的な構造をもった気管支と血管の組織を再現できる生体模倣システム(Microphysiological systems:MPS)を開発し、新型コロナウイルスへの感染によって放出されるインターフェロン分子が血管の構造に影響を与えることを見出したことを発表した。
本研究で、生体内の環境を再現するためにマイクロ流体デバイスを用いた生体模倣システムを活用し、ヒト気管支上皮細胞からなるオルガノイドと三次元的な血管網を共培養する技術を開発した。これにより、気管支上皮細胞あるいは血管網に選択的に新型コロナウイルスを感染させることが可能になった。その結果、ウイルスは気管支上皮細胞に感染するものの血管内皮細胞には感染しにくいこと、そして感染した気管支上皮細胞からのI型インターフェロンが血管構造を壊し、その機能を低下させることが分かった。
このモデルを使うことで、新型コロナウイルスが血管に影響を与える過程をさらに理解することや、将来出現する可能性のある新しい感染症にこの技術を応用し、そのメカニズムを解明するために役立つことが期待できる([4])。
02.2024年09月30日、横井歩希大学院生(CiRA増殖分化機構研究部門)、高山和雄講師(CiRA同部門)らの研究グループは、ヒトiPS細胞から作製した大腸オルガノイドに、炎症性腸疾患(Inflammatory Bowel Disease:IBD)の病態進行と関連が示唆されるサイトカインを作用させることで、IBDのサブタイプの1つである潰瘍性大腸炎(Ulcerative colitis:UC)モデルの開発に成功したことを発表した。
研究グループは、ヒトiPS細胞から作製した大腸オルガノイドにIBD患者の血清中で高い濃度の炎症性サイトカインを作用させることで、IBDの病態再現を試みた。作製した大腸オルガノイドは、大腸上皮細胞だけでなく、間質細胞や血管内皮細胞などの非上皮細胞を含む多様な細胞から構成されていた。炎症性サイトカインの作用により、上皮細胞障害、ならびに、間質細胞や血管内皮細胞における炎症応答が引き起こされた。IBD患者の組織との比較により、本モデルはIBDのサブタイプの1つであるUC患者の大腸と似た特徴を持つことが分かった。本モデルにUCの治療薬を作用させたところ、炎症応答や上皮細胞障害が抑制され、治療効果が確認された。本モデルはUCの発症メカニズムの解明や創薬研究への応用が期待される([5])。
03.2024年10月15日、豊田太郎 講師(CiRA未来生命科学開拓部門、元タケダ-CiRA共同研究プログラム(T-CiRA))、山﨑緑 主任研究員(武田薬品工業株式会社グローバルアドバンストプラットフォーム)らの研究グループは、Axcelead Drug Discovery Partners株式会社およびオリヅルセラピューティクス株式会社との共同研究により、免疫抑制された1型糖尿病モデルのミニブタを作製し、ヒトiPS細胞由来膵島細胞(iPSC-derived Pancreatic Islet Cells:iPIC)の生着を実証したことを発表した。
研究グループは、胸腺および脾臓を摘出したミニブタに膵β細胞を破壊する薬剤のストレプトゾトシンを投与し糖尿病の病態を再現した。さらに、免疫抑制剤を投与することで、ヒト細胞の移植が可能な糖尿病ミニブタを作製した。糖尿病ミニブタへiPICの移植試験を実施したところ、腹部皮下および腹膜前腔への移植において生着が確認された。本研究は、糖尿病のためのヒト細胞を用いた細胞移植治療の開発において、臨床で想定されるサイズの移植物およびその移植手術手技の検討に役立つと期待される([6])。
そして、興味深いiPS細胞関連治験を以下に示す。
01.2024年06月12日、京都大学iPS細胞研究所(CiRA)の井上治久教授、徳島大学病院 脳神経内科 和泉唯信教授、藤田浩司講師、京都大学医学部附属病院 脳神経内科 髙橋良輔前教授、江川斉宏前院内講師、北里大学病院 脳神経内科 西山和利教授、永井真貴子診療准教授、鳥取大学医学部附属病院 脳神経内科 花島律子教授、渡辺保裕准教授、奈良県立医科大学附属病院 脳神経内科 杉江和馬教授、東邦大学医療センター大森病院 脳神経内科 狩野修教授および広島大学病院 脳神経内科 丸山博文教授らの研究チームは、「筋萎縮性側索硬化症(amyotrophic lateral sclerosis:ALS)患者を対象としたボスチニブ第2相試験」(iDReAM試験:iPSC-based Drug Repurposing for ALS Medicine Study)を行い、ボスチニブの有効性と安全性を評価したことを発表した。
2019年から2021年まで実施した第1相試験では、ボスチニブにALS特有の有害事象は認められなかったこと、ボスチニブの投与期間に一部の患者でALSの進行の抑制が認められたこと、その目印となる可能性のある指標があったことが明らかになった。
2022年より、第1相試験よりもボスチニブの投与期間を長くし、参加患者の数を増やして第2相試験を行った。その結果、過去のALS試験の結果に基づき事前に設定した有効性に関する基準(主要評価項目、副次評価項目)において、主要評価項目2つを達成し、副次評価項目の2つのうち1つは満たさなかったものの、1つは達成した。以上より、ボスチニブの有効性が示唆された。また、安全性に関してはALS特有の有害事象は認められなかった([7])。
02.2024年10月02日、京都大学医学部附属病院糖尿病・内分泌・栄養内科の矢部大介教授らは、肝胆膵・移植外科と連携し、膵島移植が適応となる1型糖尿病患者を対象としたiPS由来膵島細胞シートの安全性を確認するための医師主導治験を2025年01月より当院にて開始することを発表した。
将来的に、この治療法は、糖尿病領域における移植医療のドナー不足解消に貢献し、患者の新たな治療選択肢となることを目指すものである([8])。
iPS細胞を用いる研究の進展だけでなく、再生医療やiPS創薬によるドラッグ リポジショニングの普及、即ち、健康保険適用による患者の治癒を私は大いに期待する。
参考文献
[1] 学校法人 同志社 同志社大学 商学部 瓜生原葉子研究室 医療のエコ活動研究会.“超ECO祭2024”.同志社大学 商学部 瓜生原葉子研究室 医療のエコ活動 ホームページ.https://www.medieco.net/%E8%B6%85eco%E7%A5%AD2024,(参照2024年12月16日).
[2] 学校法人 同志社 同志社大学 商学部 瓜生原葉子研究室 医療のエコ活動研究会.“ブース紹介”.同志社大学 商学部 瓜生原葉子研究室 医療のエコ活動 ホームページ.超ECO祭2024.https://www.medieco.net/s-projects-side-by-side,(参照2024年12月16日).
[3] 国立大学法人 京都大学 iPS細胞研究所(CiRA).“iPS細胞とは?”.CiRA ホームページ.もっと知るiPS細胞.よくある質問.https://www.cira.kyoto-u.ac.jp/j/faq/faq_ips.html,(参照2024年12月16日).
[4] 国立大学法人 京都大学 iPS細胞研究所(CiRA).“新型コロナウイルスの気管支への感染が血管の構造と機能を低下させることをチップ上で再現 ~血管床を有するMicrophysiological systems(MPS)を活用したモデル~”.CiRA ホームページ.研究活動.研究成果.2024年01月24日.https://www.cira.kyoto-u.ac.jp/j/research/finding/240124-160000.html,(参照2024年12月17日).
[5] 国立大学法人 京都大学 iPS細胞研究所(CiRA).“ヒトiPS細胞由来大腸オルガノイドを用いた潰瘍性大腸炎モデルの開発と応用”.CiRA ホームページ.研究活動.研究成果.2024年09月30日.https://www.cira.kyoto-u.ac.jp/j/research/finding/240930-100000.html,(参照2024年12月17日).
[6] 国立大学法人 京都大学 iPS細胞研究所(CiRA).“ヒトiPS細胞由来の膵島移植が可能な糖尿病ミニブタの作製”.CiRA ホームページ.研究活動.研究成果.2024年10月15日.https://www.cira.kyoto-u.ac.jp/j/research/finding/241015-100000.html,(参照2024年12月17日).
[7] 国立大学法人 京都大学 iPS細胞研究所(CiRA).“筋萎縮性側索硬化症(ALS)患者さんを対象としたボスチニブ第2相試験 主要評価項目達成(速報)~iPS創薬からALS進行停止を目指すiDReAM Study~”.CiRA ホームページ.ニュース・イベント.ニュース.2024年.研究活動.2024年06月12日.https://www.cira.kyoto-u.ac.jp/j/pressrelease/news/240612-120000.html,(参照2024年12月17日).
[8] 国立大学法人 京都大学医学部附属病院.“「iPS由来膵島細胞シート移植に関する医師主導治験」の開始について”.京都大学医学部附属病院 ホームページ.ニュース.2024年10月02日.https://www.kuhp.kyoto-u.ac.jp/press/20241002.html,(参照2024年12月17日).
