
9. さまざまな滅菌法
医療機関では、多種多様な器材が治療や手術に使用されます。感染のリスクが高い部位で使用される器材は清潔・無菌でなければなりません。蒸気滅菌は、現在ではほとんどの医療機器にとって最も一般的な方法になっていますが、器材はそれぞれが異なる性質を持っていることに注意が必要です。
たとえば、綿製品・ゴム製品は乾熱滅菌にかけると傷んでしまい、一部の光学機器は蒸気の湿りに耐性がありません。医療機器には、熱に弱いプラスチック製部品(非耐熱性素材)を含んでいるものも多くあります。
これらの素材は蒸気滅菌にかけることができないため、それでも滅菌できるよう、被滅菌物に合わせたさまざまな滅菌法が生み出されました。
滅菌工程が安全で適正と認められるには、以下の条件を満たさなければなりません:
• 無菌性保証水準 を達成すること
• 毎回、滅菌後に無菌性を達成すること(滅菌工程には再現性がなくてはならない)
• 滅菌工程のあとも無菌性が保たれること(包装、無菌操作)
この章で説明する滅菌法の中には、作業者への危険や環境への負荷を伴うものもあり、特に毒性のある化学物質・ガスを使った滅菌法には注意を要します。
そのため、より効果的で安全な滅菌法を生み出すための研究が続けられています。また、蒸気滅菌法は現時点で最も安全な滅菌法と考えられるため、蒸気滅菌に対応した器材を導入する事も、滅菌に伴うリスクを減らすことにつながります。
医療機器製造元は、蒸気滅菌が可能な機器の開発に日夜取り組んでおり、例をあげれば近頃では蒸気滅菌対応の内視鏡も販売されています。
9.1 加熱法
古来より、人間は「熱」を滅菌に使ってきました。微生物を加熱すると、その温度により細胞内物質の「酸化」、またはタンパク質の「凝固」のいずれかが起き、微生物は死滅します( 7.4.1参照)。
滅菌の温度や加熱の方法は、滅菌物の材質により決まります。
-9.1.1 直火による滅菌: 火炎滅菌
この方法が、おそらくもっとも古い滅菌法でしょう。
生肉よりも火であぶった肉のほうが食用として安全であることは長年知られてきたことです。

病院内では、火炎滅菌は現在でも研究室で用いられ、器材を一定時間火に当てることで滅菌しています。
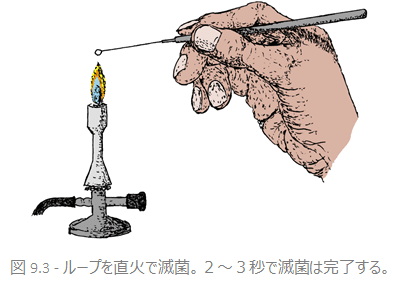
組織標本を採取する際に用いるループなどがその例です。炎の中に2~3秒もあてれば滅菌には充分ですが、ただ火の中に一瞬通すだけでは充分ではありません。
この方法は、金属針、剪刃、ツイーザーなど、直火に耐える道具にしか使うことはできません。この方法で滅菌した場合、たとえ完全に冷めていなくとも、直ちに使用すべきです。というのも、長く放置すると器具の周辺の空気が冷却凝縮し、周囲の(汚染のおそれがある)空気を引き寄せてしまうため、再汚染してしまうのです。

-9.1.2 焼却滅菌
焼却滅菌を用いると、微生物だけでなく機器そのものが破壊されてしまいます。 この方法は、滅菌というよりは破壊と呼ぶのがふさわしいでしょう。
焼却滅菌は、ディスポーザブル(使い捨て)器材に使う場合や、汚染レベルが極めて高く、安全上の理由から器材の廃棄もやむなしとされる場合にのみ用いられる滅菌法です。焼却滅菌はまた、感染性医療廃棄物の処理に用いられます。
医療機器の多くはプラスチックを含むので、焼却時には有毒ガスを発生する可能性もあります。 特に、PVC(ポリ塩化ビニル)のように塩素を含む製品の場合、焼却時に極めて有害な環境危険因子であるダイオキシンを発生します。
医療用に使用されるPVCとしては、チューブ、手袋、静脈内輸液用バッグなどがまず挙げられます。焼却滅菌を正しく行うためには、充分に高い温度で焼却することと、焼却炉が出す有毒ガスを濾過する高性能な濾過機能が必要となります。
医療廃棄物の処理については国際的に議論が続いており、焼却滅菌を廃止し、より環境への負荷の小さい、安全な廃棄物処理の代替方法が検討されています。
-9.1.3 高圧蒸気滅菌
前章までで、微生物を死滅させるのにもっとも効果的な滅菌剤は湿熱であることを学習してきました。この滅菌法では、微生物は細胞内タンパク質の凝固により死滅します。湿熱とは、水・蒸気の両方を指しますが、滅菌用としては通常は高温蒸気が用いられます。この高温蒸気を得るためには蒸気に圧力をかける必要があります。
蒸気には以下のような利点があります:
• 簡単に得ることができる
• 清浄である
• 毒性がなく、無害である
• 腐食を起こさない(水が清浄な場合)
• 熱伝導率が極めて高く、短時間かつ比較的低い温度でも滅菌効果が高い
• 滅菌工程を管理し、バリデーションの有効性を検証するのに極めて適している(14章を参照)
以上のことから下記のことが言えます。
※77
蒸気自体は無毒ですが、正しく取り扱わないとたいへん危険です
➡ 10.5.7 を参照
適応
手術機器、リネン、ゴム製品、ガラス製品など大半の医療器材は蒸気で滅菌されます。
薬品製造においても、たとえば静脈内輸液、目薬など水溶液の滅菌には蒸気が用いられています。
高圧蒸気滅菌器(オートクレーブ)
高温蒸気で微生物を死滅させる滅菌器はオートクレーブと呼ばれます。オートクレーブによる滅菌工程は高圧蒸気滅菌処理と称されます。
ほとんどの病院には、手術中に使う医療機器や衣類の滅菌用にオートクレーブが設置されており、大きな研究室や薬局でも保有している場合があります。オートクレーブは、その目的によって設計が異なります。10~14章では高圧蒸気滅菌そのものからオートクレーブの設計構造までをつぶさに見てゆきます。また滅菌器に対する国際規格についても触れていきます。


-9.1.4 熱水 (100ºC超)
従来の蒸気による液体の滅菌は、容器内の液体が安全な温度(通常約80℃)まで低下するのに時間がかかるため、サイクル時間が長いことで知られています。
最近では、液体バルク用の滅菌器として熱水(100℃を越える水)を滅菌剤として循環させるタイプの滅菌器が開発されてきています。
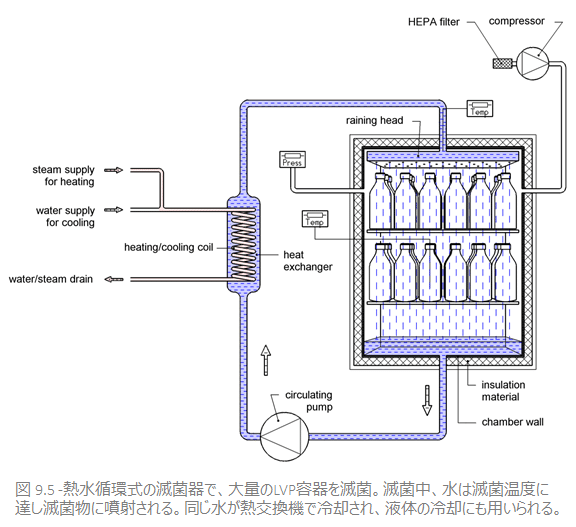
熱水は、滅菌物が入る高圧チャンバーの内部で作られ(表9.5参照)、約121℃の熱水が滅菌物にむらなく噴射されます。
ポイントは、滅菌と滅菌後の冷却で同じ水が使用される点です。
熱交換器内を通る冷却水によって水の温度を下げるので、サイクル時間を遥かに短くできます。
また、冷却用水の循環回路と、無菌水の循環回路は完全に分離されます。チャンバー内で循環する水は滅菌段階に滅菌温度に達するため、温度が下がっても水や滅菌物を再汚染するおそれがありません。こうした熱水循環式のシャワー滅菌器は非常に複雑な装置であり、高度な制御システムが必要となります。
これらは、無菌的な液体(LVP:大容量非経口的栄養剤など)を大量に製造する工程に活用されています。まるでシャワーのように被滅菌物に水が降り注ぐため、「シャワー滅菌器」とも呼ばれます。

-9.1.5 乾熱
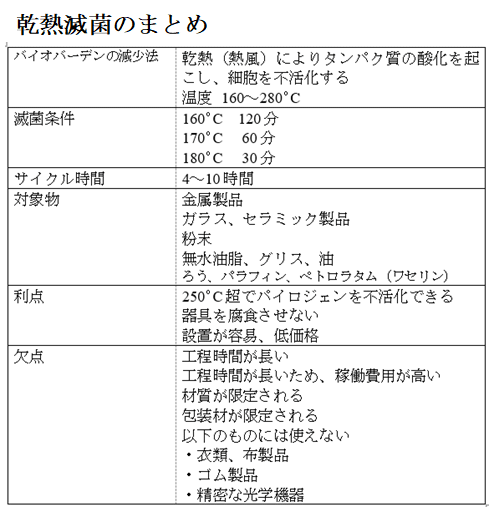
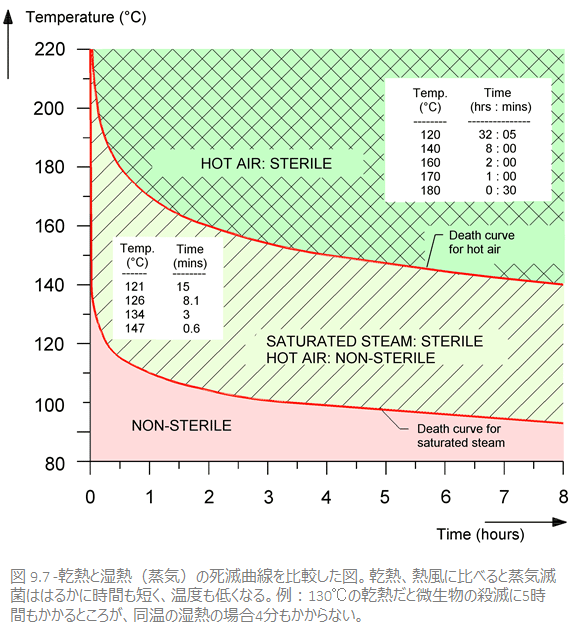
乾熱(熱風)滅菌の一般的な方法ですが、蒸気とは異なったプロセスによって微生物を死滅させます。乾熱では、微生物はいわば「熱傷」により死に至ります(酸化による死滅。7.4.1参照)。
しかし、ここまで見てきたように乾熱は湿熱にくらべて遥かに熱伝導効率が劣ります。
つまり、微生物は蒸気(湿熱)に比べると乾熱に対してはずっと長い時間耐えられるため、乾熱を用いた滅菌工程は湿熱よりも長い時間、高い温度で行わなければなりません(例:160℃ 2時間)。
加熱が済んでから、その後80℃まで温度が下がるにはおよそ10~11時間もかかり、強制冷却しても5時間はかかります。
適応
熱風滅菌は、耐熱性は高いものの蒸気では効率的に滅菌できない素材に用いられます。具体的には、水分や圧力により破損してしまう素材や器材です。
衣類、プラスチック、ゴム製品は高温により破損するおそれがあるため、乾熱滅菌には適していません。しかし、乾熱は湿熱とは異なり、鋭利な器具の腐食も生ぜず、ガラス製の注射器やフラスコなどのガラス球面を摩滅させることもありません。
そのため、乾熱は刃物、針、ガラス製注射器、実験用ガラス器具の滅菌に適しています。
温度が250ºCを越えると、パイロジェン(発熱物質)も不活化します。粉薬は水気を避けるべきなので、蒸気滅菌には適しません。また、油やペトロラタム(ワセリン)などはほとんど水分を含まないため、その性質上、蒸気が内部まで浸透しません。
こうした物質は蒸気に曝露し、結果的に蒸気と同じ温度になっても、水分を含まないため、微生物は死滅しません。以上のことから、こうした物質に蒸気をあてても滅菌はできないので、水分を含まない油脂などには乾熱滅菌を用いるのです。
装置
熱風で菌を殺滅する滅菌器を、乾熱滅菌器(または熱風炉)と呼びます。熱風は、電気的に加熱されたキャビネットまたはオーブンから排出されます。

9.2 ガスや薬品により、微生物を死滅させる
微生物を毒により殺滅するには液体またはガスを用います。もし人間が毒性のあるガスを吸えばたちまち体調を崩し、死亡することもありえます。
微生物にも、ガスや薬品は同様に使用できます。医療機器の中には、熱に弱いものや放射線滅菌に適してないものもあり(後述)、こうした類の機器には化学薬品による滅菌法が考えられます。
-9.2.1 酸化エチレンガス
酸化エチレンガス (EOG)は、微生物を死滅させるのにきわめて効果的であることが立証されており、ガスと微生物間の化学反応により微生物を殺滅します。
ガス滅菌を用いるのは、他の滅菌法が使えない場合に限られるべきです。というのも、微生物にとって有毒であるとともに、作業者にとってもガスは極めて危険な物質だからです。
滅菌物からガスが除去されていないまま患者に使用すると、体内組織にひどい損傷を与え、なくてもよい肉体的な苦痛をもたらします。毒性のあるEOGは、環境危険因子でもあるので、その利用はごく最小限に抑えるべきです。

酸化エチレンは、微生物の細胞タンパク質と核酸を攻撃します。微生物が完全に乾燥しきっていると、EOGは効果を発揮できません。
充分な湿度を確保するため、チャンバー内は滅菌前に相対湿度が適度に保たれた状態にしなければなりません。そのための前処理が、プレコンディショニングと呼ばれる工程です。
滅菌工程
滅菌工程は、大気圧以上あるいは以下いずれでも行われます。 大気圧以下での滅菌の利点は、リークがあった際にも、器内が負圧なためEOGが漏出しない点です。
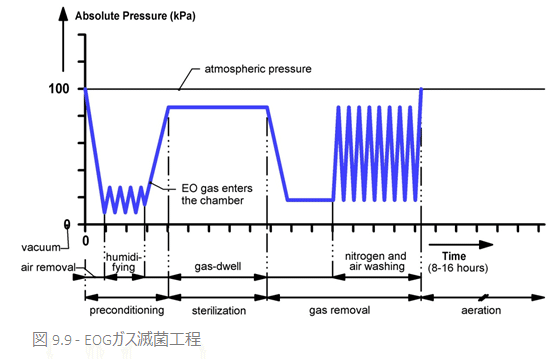
それゆえ、最も望ましい方法と考えられます。工程は、まずガスのもつ不活化効果に理想的な器内環境にするためのプレコンディショニングから始まります。プレコンディショニングには、空気除去工程と、加湿工程とがあります。
空気除去
真空工程中のガスの浸透を助けるため、滅菌物から空気が除去されます。一定の真空度に到達したら、リークがないかのチェックが行われます。
加湿
プレコンディショニングの二段階目では、一定の湿度に達するまで蒸気をチャンバー内に導入させます。
滅菌
滅菌の直前、ガスがチャンバー内に侵入し、圧力は上昇します。工程中の圧力が大気圧以上であるか以下であるかは、ガスの種類によって異なりますが、大気圧以上の工程ではガスが漏出する危険があるため、現在ではこの方法は用いられていません。
また、混合ガス中のEOG濃度を一定に保つことはできず、それはEOGの純度が100%の場合のみ可能となります。近年、大気圧以下での濃度100%のEOG工程のみが用いられているのは、この2つの理由のためです。滅菌中の温度は、滅菌物の種類にもよりますが、40~55℃です。
ガスの除去
滅菌工程の最終段階では、チャンバーから排気するとともに、無菌空気を供給し、残留したEOGをチャンバーから取り除きます。さらに安全を担保するために、多くの場合、窒素ガスを供給することでEOGを不活化させ、反応を止めます。
エアレーション (強制脱気)
プラスチックやゴムのような素材は、滅菌中にガスを吸着してしまいます。滅菌後、残留したガスは近くのものに移ってしまい、患者に用いると、ガスの毒が患者の組織を傷害する恐れがあります。
そのため、滅菌物からは残留ガスを除去しなければなりません。
これは、チャンバー内に充分な時間クリーンエアを導入する段階で、エアレーションと呼ばれます。エアレーションは、独立したエアレーションチャンバーや専用区域で行うこともあります。
温度は30~50℃で、無論、清浄な空気を使用しなければなりません。そこで、チャンバー内に入る空気は、高性能エアフィルター(HEPAフィルター)を通すことが必須となります。作業員を保護するため、エアレーションからの排気は作業場の通常の排気システムとは完全に分離されなければなりません。
温度が高ければ高いほど、エアレーションによるガス除去効果は高くなります。器材からのガス除去所要時間は、EOGの供給される空気への再吸着速度によって変動します。脱気のレベルは計測され、残留ガスのレベルは、機器のクラスごとの最大残留基準値と比較されます。
通常、エアレーション段階は、被滅菌物の材質や形状によって24時間から数週間かかります。EOGガス滅菌法は、非常に危険であるため、他に代わる方法がない場合に限り用いられるべきだと結論づけられます。
多くの国では、もはやEOG滅菌法は医療施設内ではなかなか用いられてなくなっており、専門業者が行うことがふつうです。こうした業界では、一般に大型の滅菌器で大量の被滅菌物を扱います(図9.8も参照)

-9.2.2 ホルムアルデヒドと蒸気の組み合わせ
ホルムアルデヒドは、生体内に極めて少量存在する天然のガスです。
多くの生物にとって代謝の副産物であり、大気中や雨水、またリンゴ、コーヒーなどの食物にも含まれます。
しかし、凝縮すれば滅菌剤として非常に高い効果を発揮します。ホルムアルデヒドは、極めて高い親水性をもつため、水に非常によく溶けます。
加えて、ホルムアルデヒドの不活化力は、湿度の存在により大幅に向上します。そのため、ホルムアルデヒド水溶液は消毒薬や防腐剤の活性剤として活用されます。
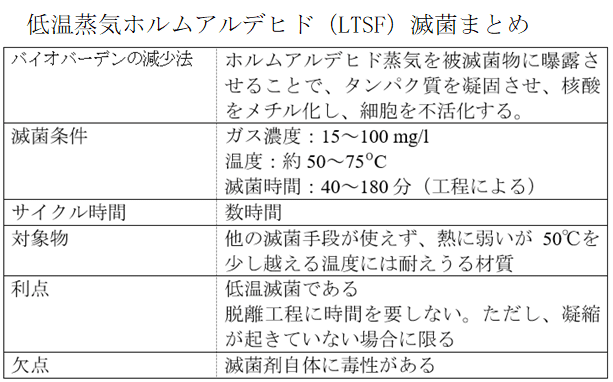
50~75℃でホルムアルデヒドは滅菌剤となりますが、その不活化力を高めるために蒸気と混合して用いられ、低温蒸気ホルムアルデヒド(LTSF)滅菌法として利用されます。比較的低温の滅菌であるため、熱に弱く従来の蒸気滅菌に適さない器具にも使用することが可能です。
ホルムアルデヒドの注入と脱気のパルス、その後の蒸気・空気注入という工程により、長い管腔構造を有した機器にも適しているとされます。適正に管理された工程下で用いれば、ホルムアルデヒドの濃度は、作業環境の許容値(労働衛生許容濃度=MAC値 )を上回ることはなく、滅菌した器材を患者に使用しても問題ないレベルです。
ほとんどの被滅菌物は、滅菌後すぐの払出が可能であるため、サイクル時間は比較的短く、EOG滅菌に比べると、高価な機器を短時間で回転させることができます。
しかし、ドレーン(凝縮水)が残らないよう、またドレーンがホルムアルデヒドやパラホルムアルデヒド(毒性あり)の残留につながらないよう特別な注意も払わなければなりません。特に温度分布や工程の脱気レベルなど、工程管理には厳格な必要条件があります。
メモ:低温蒸気ホルムアルデヒド(LTSF)の効果については、国ごと、また専門家ごとに長い間見解がわかれてきました。英国、ドイツ、スウェーデン、デンマーク、ノルウェーなどにおいては、LTSFが日常的に用いられ、LTSF滅菌器につき国内規制があります。一方で、オランダなどいくつかの国では、ホルムアルデヒドは滅菌剤としては推奨されておらず、米国ではこの滅菌法自体あまり知られていません。近年では LTSFの欧州基準 が生まれ(2003)、それによりこの滅菌法が公式に認められました。 LTSFの運用については、関係当局にお問い合わせください。

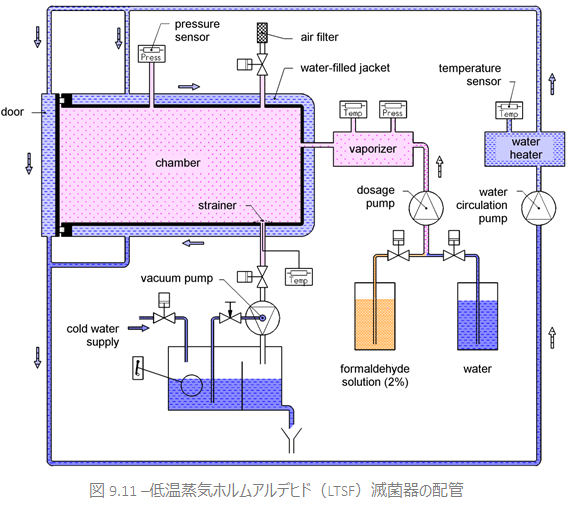
滅菌器の設計
低温蒸気ホルムアルデヒド(LTSF)滅菌器は、大気圧以下で稼働するよう設計されています。正しく稼働するには、チャンバー内・滅菌物内部のいずれの箇所でも温度が等しいことが大切です。
チャンバーを取り包む外缶が、蒸気、水、あるいはオイルで熱せられて実現します。電気加熱マントルも使われることがあります。
外缶の温度は念入りに制御され、チャンバー内部は適切な温度内に正確に保たれます。水循環ポンプは空気除去と脱気に必要な真空状態を作り出し、蒸気は蒸気発生器で生成されます。
滅菌剤は、低濃度ホルムアルデヒド溶液(2%など)であり、蒸気発生器で蒸気と混合され、蒸散します。自動計量システムと入念に制御された蒸気発生器が、ホルムアルデヒド濃度を正確に調整します。
滅菌工程
LTSF滅菌工程では、ホルムアルデヒドが滅菌剤ですが、被滅菌物の全表面へのホルムアルデヒド浸透を促し、さらに不活化力を促進するのは蒸気の力です。
蒸気の物理的作用にホルムアルデヒドの化学的作用が加わるため、この滅菌工程はいわば物理・化学的工程と見做されます。LTSF滅菌は、滅菌器の設計によってその工程はさまざまです。
図9.12は、図9.11で示した滅菌器のサイクルです。サイクルは以下の段階に従って進行します。
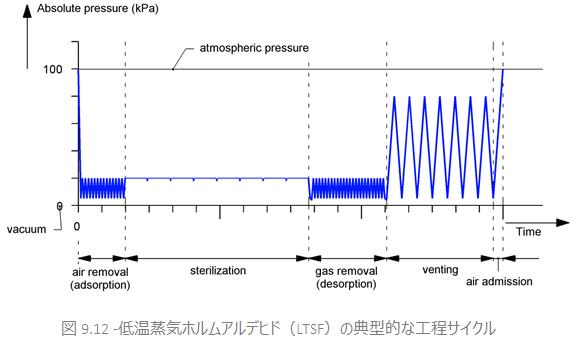
パルスマチックプレバキュームによる空気除去とホルムアルデヒド吸着
ホルムアルデヒドと蒸気の混合気は、被滅菌物の全表面に到達する必要があります。これは、一般的な蒸気滅菌器と同様に、パルスマチックプレバキューム(反復脱気)と蒸気の供給により可能になります。
機種によっては、ホルムアルデヒド蒸気が反復脱気中に供給され、被滅菌物への浸透を促進します。このような工程は管腔構造を有した器具にも適しています。
滅菌
反復脱気が終わると、ホルムアルデヒド蒸気が供給され、設定温度・時間内で滅菌物に曝露します。正確に管理することによって混合気は適正な温度・濃度に保たれ、ドレーンは真空ポンプで定期的に排出されます。
脱離(脱気)
蒸気とホルムアルデヒドの混合気は、蒸気の供給と真空引きの反復サイクルにより排出されます。パルスごとに新鮮な蒸気が供給され、ホルムアルデヒドの排出を促進し、その濃度は安全レベルまで下がります。
換気/乾燥
滅菌物は、続いてフィルター(HEPAフィルター)で濾過した無菌空気の供給と排出を繰り返されて、乾燥されます。
給気
サイクルの最後に、無菌空気がチャンバー内に供給され、圧力は大気圧まで戻ります。この段階でドアは開放可能となり、払出が可能となります。
-9.2.3 グルタルアルデヒド
熱耐性がない被滅菌物の多くは、化学薬品や放射線による滅菌ができます。
ただし日常実務でこれらの滅菌方法を使おうとするととても長い時間がかかります。
膀胱鏡や内視鏡のような、高価でかつ集中的・頻繁に使用される機器は、滅菌の頻度もそれだけ多いため、これらの滅菌法は適切ではありません。またこうした器材に適した滅菌器、特に放射線滅菌器はたいへん高価です。
そこで、化学薬品のグルタルアルデヒド滅菌が活用されます。
しかし、これが本当に滅菌法と呼べるかどうかについては議論があります。なぜならば、使用時まで無菌性を保つことができないからです。
まず滅菌物が包装されておらず、さらにすすぎが必要なので再汚染の可能性があるからです。そのため、グルタルアルデヒドに浸漬することは滅菌というよりも、高水準の消毒法と見做されています。
また充分な水ですすがないと、グルタルアルデヒドは患者の組織を傷害するおそれがあることに注意しなければなりません。その毒性から、作業者の保護対策は必須であり、換気が行われる部屋でのみ取り扱うべきです。グルタルアルデヒドは、熱、ガス、放射線でも滅菌できないもの・器材への非常手段ととらえるのが妥当です。
また、グルタルアルデヒドは、プリオン汚染が疑われる機器の消毒には適していません。

9.3 放射線滅菌
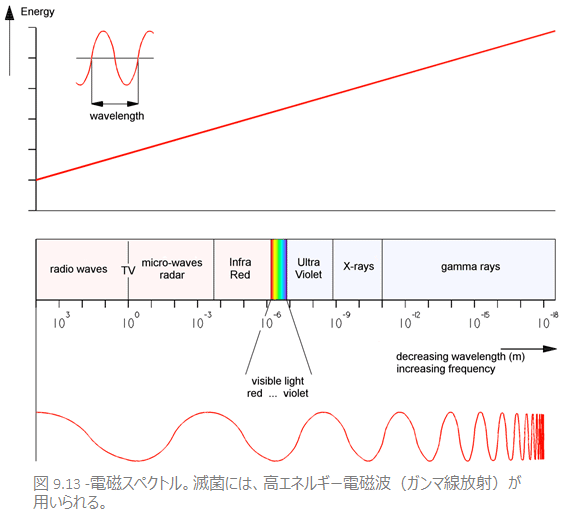
放射線は「線」として放出されるエネルギーの一種です。これらの線は、磁力や電気特性を持ち、波のような動きをするので「電磁波」と呼ばれます。
水による波と同様、電磁波は特定の波長があり、その波長は数百キロにもおよぶ非常に長いものから、フェムトメートル 単位の非常に短いものまで存在します。
波長の範囲は周波数帯(=バンド)と呼ばれ、周波数帯ごとに特徴を持ち、その全帯域を合わせて電磁スペクトルといいます。
電磁波は面白い特徴を持ち、たとえばラジオ、テレビ、レーザー、レーダーなどの形で我々の生活の身近な所にあふれています。
電磁放射はさまざまな形で体験できますが、そのもっとも身近な形態が「熱」です。太陽や火から感じる熱は、その典型です。目に見えないこの放射線は、赤外線(IR)と呼ばれ、長い波長を持ちます。
放射線の形態は、カラースペクトルと呼ばれ、人間の目にも見えます。このスペクトルは波長順に赤色から青色までわかれ、その中に虹の全色が含まれます。赤から青に近づくに従って波長は短くなり、逆にエネルギーは増大しますが、青色を超えるとその放射線は人間の眼には見えなくなり、紫外線(UV)と呼ばれます。この紫外線は非常に強力な放射線であり、皮膚に熱傷を与え、UVよりも波長が短い放射線になれば、原子や分子を電離します。
この電離を「イオン化」と呼び、原子や分子を電離できる放射を「電離放射線」といいます。これは非常に短い波長と高いエネルギーを有し、生物に重大な被害をもたらします。
電離放射線は原子が崩壊するときに発生します。そうした放射線を自ら発する物質は「放射性物質」と呼ばれ、
電離放射線には以下の3つのタイプがあります:
1. アルファ線
比較的大きい正荷電粒子(ヘリウム元素の原子核
に似た、2個の陽子、2個の中性子からなる原子核 )からできています。
2. ベータ線
小さな負荷電粒子(電子)からできています
3. ガンマ線
電磁放射線
アルファ線、ベータ線は粒子からなり、一方ガンマ線は質量を持たない純粋な電磁放射線からなります。そのため、ガンマ線はベータ放射線にくらべて高い透過性をもちます。
しかし、物質との衝突のため、ガンマ放射線のエネルギーは徐々に減衰してしまいます。またベータ放射線は大部分が物質に吸収されます。これらすべての放射線はいずれも、照射した物質を放射性物質に変えることはありません。
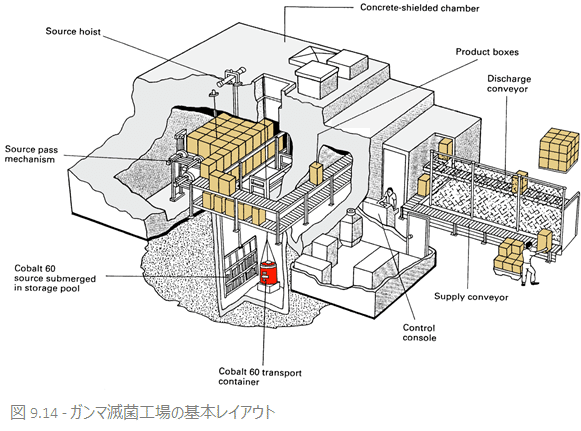
ガンマ放射線は放射性物質である燃料棒の線源から放出されます。ガンマ線放射に使われるもっとも一般的な物質がコバルト元素で、コバルト60とも呼ばれます。
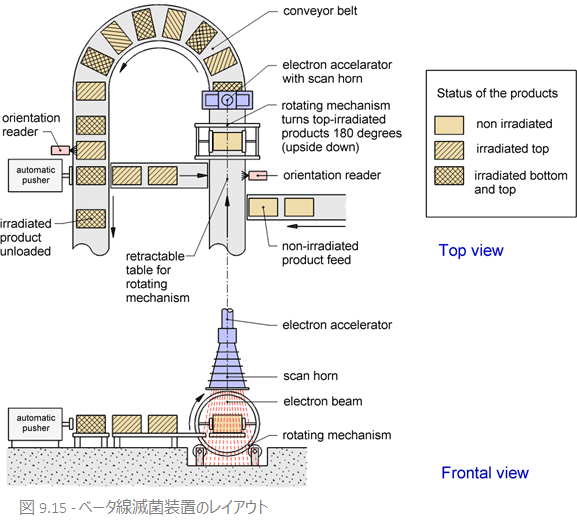
ベータ放射線は電子加速器で電子を加速させて作り出します。医療においては、ベータ線とガンマ線の両方が用いられ、治療、診断、滅菌に役立てられています。
滅菌剤としての放射線
1945年に広島と長崎に投下された原子爆弾や、1986年のチェルノブイリ(現ウクライナ)原子力発電所事故によって、放射線が人類に与える致命的な影響は、充分に裏付けされてきました。高いエネルギーの放射能には強い殺傷力があるので、つまり強い殺菌力があるということは明白です。
厳密な工程管理のもと、電離放射線が滅菌に活用されています。放射線は、生物の細胞膜や遺伝子にダメージを与えます。
ガンマ線滅菌のためには、被滅菌物を照射室に運び入れ、放射線源を周回させる必要があります。この工程は、滅菌物が全方向から均等に照射されるようにセットされ、照射は継続的に行われます。
線源(燃料棒)は、使われない間は水槽に浸漬されますが、このとき放射線は水に吸収され、水槽は美しく「青い光」を放ちます。
ベータ線は、テレビのブラウン管に似た電子加速器で作り出します。加速器から放射線が放たれ、照射チューブを通り、その下にセットされた被滅菌物を透過します。ベータ線滅菌器では、被滅菌物は照射チューブ内で複数回照射されます。照射により被滅菌物が放射性物質となることはありません。ガンマ線、ベータ線いずれの方法でも、照射室を出てしまえば、被滅菌物は安全です。
適応
放射線滅菌は、主に滅菌物の材質や包装が熱や薬品滅菌に対して耐性がない場合に使用されます。多種多様な製品を大量生産する場面では、放射線滅菌が急速に広まっています。医療機器の他、薬品、食品、農産物にも用いられる滅菌法です。
▼放射線滅菌のまとめ

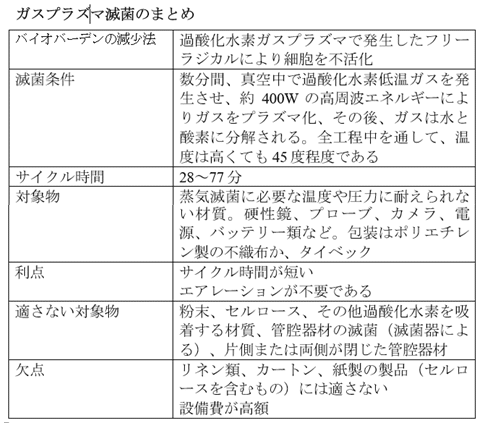
9.4 過酸化水素ガスプラズマ滅菌
市場には、これまでにないほど、低温滅菌が必要な医療機器が出現しています。しかし、環境と健康への配慮から、有毒な薬品を用いた滅菌法は次第に減少する傾向にあり、放射線滅菌はその高いコストから大規模な工場でしか用いられません。
そして、ポリプロピレンや電子部品を含む多くの医療機器は、放射線への耐性がありません。これらのことから、過酸化水素低温ガスプラズマ滅菌により微生物を不活化させる方法が開発されてきました。
機種にもよりますが、この工程ではわずか45℃で、28~77分で滅菌ができます。
プラズマ:物質の「4番目の」状態
実はプラズマはごく一般的な物質状態で、固体、液体、気体に続く、物質の第4形態といわれています。星や星間空間のプラズマは目に見える宇宙の99%以上を占め、見えない宇宙のほとんどもプラズマだと考えられています。
プラズマは、自由電子と自由イオン、電離した原子から構成されていて、プラズマを生成するには原子から電子を電離するためのエネルギーが必要です。エネルギーには熱、電気、光(紫外線、可視光レーザー)などさまざまな形態があります。充分なエネルギーを維持できないと、プラズマは中性ガスに戻ってしまいます。
プラズマは、強力な電磁場があれば低温(50℃以下)状態で作ることができます。プラズマは電磁場によって加速、誘導することできるため、その管理や低温滅菌への応用が可能です。

滅菌剤としての過酸化水素ガスプラズマ
プラズマ状態で発生する自由電子や自由イオンは、化学的に極めて活性が高く、フリーラジカルと呼ばれます。これらのフリーラジカルが、微生物の細胞壁を破壊し、細胞を不活化します。
過酸化水素低温ガスプラズマ滅菌器では、過酸化水素水がプラズマ化し滅菌剤として用いられます。プラズマが作られる温度は50~60℃と低いままです。
過酸化水素水は、1890年から多くの細菌の芽胞を不活化できる消毒薬として広く知られてきました。過酸化水素水を気体(ガス)にすると非常に滅菌効果が高くなり、さまざまな器材の滅菌に適したものになります。過酸化水素ガスに高周波エネルギーを放射すると、ガスはプラズマ化します。
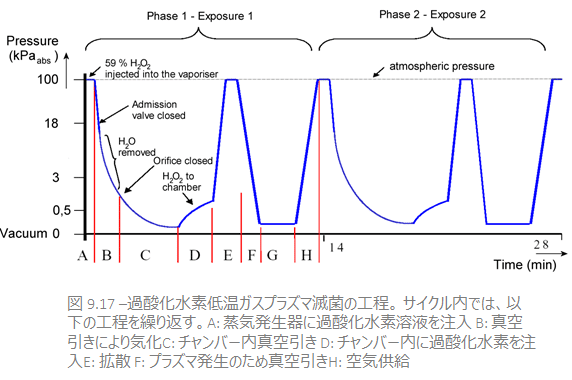
滅菌工程
まず、滅菌チャンバー内で真空引きをします。真空引きは一定時間継続し、この間に被滅菌物を乾燥させ、40~45度まで温めます。
次に、過酸化水素溶液を注入します。真空度が高い状態のため、溶液は蒸発して過酸化水素ガスとなります。フィルターにかけた空気を供給し、大気圧まで戻すと、過酸化水素蒸気が生まれ、包装を透過し、被滅菌物の全表面に到達します。
拡散が終わったら、蒸気をチャンバーから排出し、高周波エネルギーにより残りの混合気をプラズマ化させます。このプラズマ工程中、高周波エネルギーを止めると水素原子と酸素原子は分解し、水と酸素が形成されます。 この注入・拡散・プラズマ工程が繰り返され、全工程は終了します。
工程は、滅菌器の種類にもよりますが、28~77分程度です。被滅菌物はタイベックかポリエチレンで包装し、チャンバー内に積みつけます。滅菌工程中、温度は45度を超えません。希望に応じてすべての工程パラメータを参照することも可能です。
プラズマ滅菌法は、蒸気滅菌の温度や圧力に耐えられない素材に使用されます。たとえば、硬性鏡、プローブ、カメラ、電源・バッテリー類などです。多く普及している軟性鏡も、プラズマ滅菌に適しています。
長年、過酸化水素/プラズマ滅菌器は、ある製造元が単独で生産しており、この本の初版の時点では3機種が販売されていました。すべてFDAの承認とクラス2a医療機器のCEマークとを得ています。
また、ISOEN14937にも適合しています。その後、他の製造元も、過酸化水素/プラズマ滅菌器を市場に送り出しました。
9.5 濾過滅菌
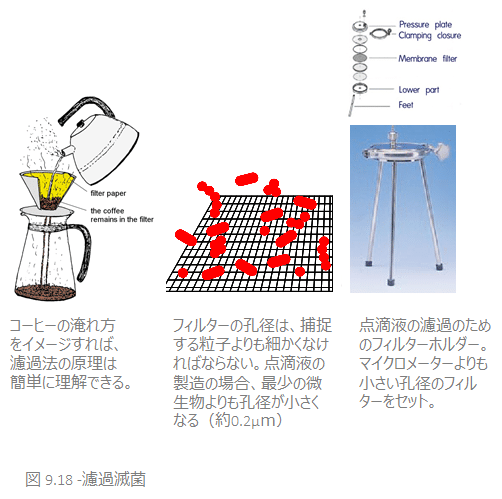
濾過滅菌は、これまでに述べたあらゆる滅菌法とは明らかに異なります。微生物を死滅させるのではなく、それを被滅菌物から取り除くのが目的です。
濾過とは、「こし器(濾紙)」の目よりも大きな素材や物質をふるいにかける方法です。 コーヒーの淹れ方をイメージすれば理解がしやすいはずです。フィルター上のコーヒーにお湯を注ぐと、お湯はフィルターを通じてポットに落ち、挽いたコーヒー豆がフィルターに残ります。
濾過をして微生物を除去できるのは、液体と気体だけです。コーヒーフィルターのように、微生物の除去は単に溶液を濾紙にかけることで可能となります。この濾紙はあらゆる微生物が通過できないようでなければなりませんが、ウイルス(0.01~0.3µm)は小さすぎて、現存する濾紙では濾過できません。 そのため、濾過滅菌は現実的な滅菌方法とは考えられていません。
ガスの濾過
滅菌工程中、粒子が浮遊していない無菌空気が必要となる場合があります。たとえば蒸気滅菌器では、滅菌工程後、チャンバー内の乾燥のために蒸気を排出する必要があります。このとき、真空状態を脱するために、無菌空気を供給する必要があります。
また、たとえば無菌の溶液を容器に注入するなど、工程が無菌状態で行われなければならないような時には、空気もまた無菌的でなければなりません。これは通常ラミナエアフロー(LAF)と呼ばれる、空気をフィルターにかける機械の設置された、室内で行われます。
この目的で、空気はHEPAフィルターを通して濾過されます。
液体の濾過
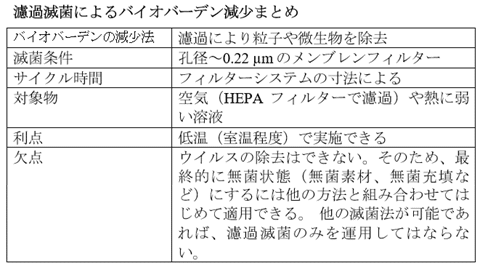
オートクレーブの熱では充分な安定が得られない溶液には、濾過法の使用が考えられます。無菌状態の溶液、液体の製造時には、孔径0.22 µm以下の無菌済みメンブレンフィルター(逆浸透膜フィルター)か、他の同レベルの菌補足性をもつフィルターが用いられます。
フィルターからの汚染がないよう、適切な手順をとる必要があります。濾過のあとは、溶液はあらかじめ滅菌された容器に入れて無菌状態で分別し、微生物の混入を防ぐために密封しなければなりません。
また、滅菌フィルターの品質は使用前に必ずチェックし、使用後も使われたフィルターごとに精密濾過膜の完全性試験の一種、拡散流量試験であるバブルポイント試験、圧力保持試験、)を実施し菌補足性能の検証を行います。
使用中、フィルターは捕捉した菌で目詰まりを起こすため、液体の流れが悪くなります。これは、汚れた水をフィルターに通すことを考えるとわかりやすいでしょう。
最初のうち、水は澱みなく流れますが、次第にフィルターが目詰まりをし、流れが悪くなり、しまいには流れなくなってしまいます。
そのため、フィルターは定期的に交換しなければなりません。
濾過法で液体から細菌や粒子を取り除けますが、ウイルスは除去できません。つまり、濾過法を使えるのは液体中にウイルスがいないと確証できる場合だけです。
他の方法と組み合わせた場合に限り、濾過法で滅菌物を作り出すことができるのです。
要するに、濾過は滅菌物を作り出す工程の1つに過ぎず、保証も限定されるので、他の滅菌方法が使える場合には認められません。
9.6 非耐熱性材質のより良い滅菌法を求めて
手術の技術やプロセス(手順)はますます複雑化しており、プラスチックを含む器材の割合も増えてきています。これらプラスチックの多くは乾熱や蒸気滅菌の熱への耐性がありません。
環境への関心の高まりや、薬品・放射能を用いた滅菌法がもつリスクへの懸念から、より安全な他の滅菌法を求める声は大きくなっていると感じられます。
最近運用が進んでいる滅菌法の一部が、過酸化水素ガスプラズマ、過酢酸、オゾンなどによる滅菌法などです。超臨界流体による滅菌法は、議論の的となっている新たな滅菌技術です。
医療現場では、蒸気を用いる方法のみが主流です。
ですから、蒸気滅菌に適さない器材や材質のものは、他処の滅菌会社で滅菌されたディスポーザブル製品に代替されるようになってきています。
こうした、すべての滅菌法の発展および新しい滅菌法は、滅菌に関わるあらゆる人々の強い関心から生み出されているのです。
===
お問い合わせは、株式会社名優まで。

