
国内のガイドラインに絡むCOIがヤバい件について:後編
こんにちは、にゃんでもにゃ医です😇😇
今回は皆さんお待ちかねの後編です😇😇
前編をまだ読んでない方はぜひお読みください😇
ついに各ガイドラインに切り込みます!
いよいよ各ガイドラインの推奨とCOIについてみていきたいと思います。選考基準としては基本的に自分が読んでこの推奨はどうなんだろう…とワイが思っていたものをピックアップしています😇そして次のステップとしてCOIを確認してみる、という流れになっています😇
5つのガイドライン(提言などもあります)を取り上げていますが、どのガイドラインも基本的には以下のような流れでやっていきます😇
①ガイドラインの推奨の紹介
②海外のガイドラインの紹介
③ガイドラインの引用文献などを確認
④COIの確認
肺炎のガイドラインは有料なので読んでいなかったですが、TwitterにてCOIがヤバいという話を複数いただいたので取り上げています😇ガイドライン全体の質についてはまったく評価しておらず、推奨そのものにフォーカスしています。取り上げているガイドラインも重要な役割を果たしてきたと思うんだけど、とか言われても知りません😇😇😇
基本的にワイが1人でレビューしているので、間違っている箇所もあるかと思います😇指摘していただけると大変ありがたいです😇
あと今回は2万字近い大作になってしまっているので、全部読むと疲れます😇
気になるものから読んでいってもらったらと思います😇
それと個人名の記載は諸事情により控えさせていただきました😇
まあちょっと確認すればわかりますが😇
それではよろしくお願いします😇😇
成人肺炎診療ガイドライン2024(日本呼吸器学会)
こちらは有料ガイドラインですね😇なので全然読んでなかったのですが、フォロワーの方からある薬剤が怪しいというコメントを複数いただいたので買って読んでみました😇
その薬剤とはラスクフロキサシンですね😇😇
市中肺炎のscopeのところに以下の記載があります😇
…mutant prevention concentrationを超える面積が大きいほど耐性菌は誘導されにくいとされている。この理論に則って開発された薬剤はガレノキサシンとラスクフロキサシンである。
ほーほうほう、キノロンならその2剤がおすすめなのね😇😇😇
ワイはキノロンだとレボフロキサシン、シプロフロキサシン、モキシフロキサシン以外はすべてアレだと思っていたんですが😇😇
…その後、PK/PD等の科学的根拠に基づき、耐性菌を誘導しにくいレスピラトリーキノロンの存在が明らかとなり、「成人肺炎診療ガイドライン2017」からはレスピラトリーキノロンを第一選択薬の一つに位置付けている。
(;゚д゚)(つд⊂)ゴシゴシ(;゚Д゚)…?!
んんんん⁉️⁉️
困惑しながらも市中肺炎のエンピリック治療薬がまとまった図をみてみると、なんとラスクフロキサシンの文字がたくさん並んでいるではありませんか😇😇
まず市中肺炎の第一選択薬にキノロンはいろいろよろしくないのではというツッコミが😇😇
自分でも1ページ前に書いてるじゃないですか、結核もカバーしてしまうから、キノロンが本当に必要かどうか考慮する必要があると😇😇なのに第一選択薬てどういうことですか、自分で書いたのを忘れちゃったんですか😇😇
最近出たJAMAからの市中肺炎のレビューでも、もろもろ良くないことがあるから、キノロンはβラクタムアレルギーがあるときにだけ使うことを考慮するように書いてますね😇
良くないことの一つに大動脈解離・大動脈瘤リスクの増加があり、米国FDAも高血圧の患者や高齢患者などには他の選択肢がある状況でキノロンを使うべきではないと警告していますね😇
フォロワーさんに教えてもらうまで知らなかったんですが、キノロンの添付文書には重要な基本的注意のところに「大動脈瘤、大動脈解離を引き起こすことがあるので、観察を十分に行うとともに、腹部、胸部又は背部に痛み等の症状があ らわれた場合には直ちに医師の診察を受けるよう患者に指導す ること。」という記載があるんですね😇皆さんはちゃんと指導されていますでしょうか😇😇
あとはキノロンを選ぶとしてもなぜそこでラスクフロキサシンなのかという話ですね😇
2020年に承認された薬剤で圧倒的にデータが少ないですね😇臨床データについてガイドラインではなにも引用されていません😇
耐性菌のリスクが低いとのことですが、ラスクフロキサシンについてその根拠となる文献は何も提示されていません😇😇 in vitroのデータでもあるんでしょうかね、良くわかりませんが😇
どうですか、これは漂ってきませんか、COIの匂いが😇😇😇
そこでラスクフロキサシンを製造販売している杏林製薬とのCOIを確認してみました😇
ガイドライン作成に関わっている52人のうち、杏林製薬とのCOIを報告しているのは9人で、そのうち8人が委員長・委員です(委員長・委員は計19人)😇
杏林製薬のホームページで確認しましたが、2022年における委員長・委員に支払われた金額(講師謝金と原稿執筆料)は合計約1200万円で、そのうち委員長に支払われたのは約430万円です😇うーんなるほど😇
とりあえずラスクフロキサシンのインタビューフォームみてみました😇
https://www.kyorin-pharm.co.jp/prodinfo/medicine/pdf/i_lasvic.pdf
そこにある市中肺炎患者における ラスクフロキサシンと レボフロキサシンの第 III 相二重盲検比較試験を読んでみたのですが、筆頭著者がガイドラインの委員の1人で、その他の著者のなかに委員長ともう1人の委員も含まれているではありませんか😇😇
https://www.chemotherapy.or.jp/journal/jjc/068S1/068S10041.pdf
これはもはやアレですね、このガイドラインの狙いはラスクフロキサシンを売りこmうわなにをするやめくぁw背drftgyふじこlp
…ということでまず一つ目はここで終わりです😇
このノリでどんどんいってみましょう😇😇
急性・慢性心不全診療ガイドライン2017年改訂版 (日本循環器学会 / 日本心不全学会)
続いてはこちらですね😇
https://www.j-circ.or.jp/cms/wp-content/uploads/2017/06/JCS2017_tsutsui_h.pdf
こちらで気になったのがトルバプタンとカルペリチドです😇😇
まずトルバプタンからいきますね。急性心不全に対して、ループ利尿薬をはじめとする 他の利尿薬で効果不十分な場合の体液貯留に対しての投与について推奨クラスⅡa, エビデンスレベルAとなっています😇エビデンスレベルAということはさぞかし強いエビデンスがあるんやろなあと思いながら本文を読んでみると…
EVEREST 試験とわが国における多施設共同非盲検ランダム化比較試 験では,短期的には自覚症状や体重を改善したが,投与後の生命予後を改善するには至らなかった.近年行われたTACTICS-HF試験,SECRET-CHF試験にお いても体液貯留改善効果は認められたものの,症状軽減効果は限定的であった. よって,利尿薬抵抗性のため 強いうっ血症状を呈する心不全患者の体液管理には有効と考えられるが,必要最小限の投与にとどめるべきである.
ぬぬぬ⁉️ちなみにレベルAのエビデンスとは「複数の無作為介入臨床試験,またはメタ解析で実証されたもの.」とのことです😇
ということは体重減少や体液貯留の改善といった代用のアウトカムについてレベルA ということなんですかね😇😇ちなみにHFrEFに対する推奨はⅡaBとなってますね😇こちらにも長期予後を改善するエビデンスはないと書かれてますね😇
ここで諸外国のガイドラインも見てみましょう😇
まずは2022年に出た米国3学会合同の心不全ガイドライン😇
うっ血性心不全の治療のところに、「低ナトリウムを伴う心不全において、パソプレシン受容体拮抗薬は役立つかもしれない」という記述で終わっています😇😇
続きまして2021年のヨーロッパの心不全ガイドライン😇
こちらも同様で、低ナトリウム血症を伴う心不全にはパソプレシン受容体拮抗薬を考慮するという記載ですね😇
どちらのガイドラインにも他の利尿薬で効果不十分なときに使うという記載はありません😇ESCガイドラインでは急性心不全でループ利尿薬の効果が不十分な場合はサイアザイド、メトラゾン、アセタゾラミドの追加を考慮するとの記載はあります😇
UpToDate, DynaMedも確認しましたが同様のスタンスです😇
代用のアウトカムを改善したというエビデンスは色々あるようですね😇
こちらはフロセミド単独と比べてサムスカを併用すると3rd スペースから水を引いて血管内脱水になりにくいという報告😇
こちらはトルバプタンはフロセミドと比べて腎機能が悪化しにくく、血圧も下がらなかったという報告😇
CKDのある心不全患者において、フロセミドにサムスカを足したほうが腎機能の悪化が少なかったという報告😇
ということで日本は海外と比べて代用のアウトカムも重要視しているということなんでしょうかね😇😇
循環器系の本を読んでも、トルバプタンは基本肯定的に書かれてますし、実際に循環器の先生とお話ししても、トルバプタンは心不全管理がしやすくなるというお話を聞きます。自分は使用経験が少ないですが、玄人向けのよい薬剤なんだと思います😇
ただ、ジェネリックが出たとはいえ高い薬でもありますし、慢性心不全に対してもずっと使われる薬でもあるので、やっぱりちょっとモヤりますね😇
今後game changerになるような、海外のガイドラインでもガンガン取り上げられるような日本発の研究に期待したいです😇
一応COIも確認しておきましょう😇
2022年までは先発品のサムスカしかありませんでしたね😇
サムスカを製造販売しているのは大塚製薬ですね😇大塚製薬とCOIがあるのはガイドライン作成に関わった58名のうち20名です😇
ガイドラインの班長はガイドラインが出た2017年に大塚製薬から約110万円受け取っています😇ちなみに2021年は約260万円です😇
まあこんなもんじゃないですかね😇
全員を調べるのは諦めました😇
続きましてカルペリチドに行ってみましょう😇😇
ガイドラインでは非代償性心不全患者での 肺うっ血に対する投与において、推奨クラスⅡa, エビデンスレベルBとなっています😇
まずこちらの小規模のオープンラベルRCTで18ヶ月の観察期間において、カルペリチド群は死亡や再入院が少なかったという文献が引用されています😇
一方で、カルペリチドの使用が院内死亡率の増加と関連を認めたとする観察研究も引用されています😇😇
そして最後はこのように締めくくられています😇
以上より,急性心不全におけるカルペリチド投与については,他の血管拡張薬と同様,予後改善効果は確立されておらず,今後有効な患者の選択が重要であると考えられる.
ふーむ、これで推奨クラスⅡaでエビデンスBなのか…と思っちゃったんですが、どうなんでしょう😇😇
上述の海外のガイドラインではまったく触れられていません😇それもそのはず、海外(特に米国?)ではもともと同種薬のNesiritideが使われていたのですが、2018年に製造中止になっています😇
2011年のNEJMのRCTでは、Nesiritideは死亡や再入院を減らしも増やしもしないという結果だったようです😇そして有意差はないが呼吸苦を減らし、腎機能の悪化とは関連がなかったが、低血圧とは関連がみられたと😇
上述のトルバプタンとは違い、色々な書籍でも厳し目のコメントが並んでいますね😇
こちらは10年以上前に出版されたINTENSIVISTの急性心不全にあるコラムです😇
ATTEND registry で示されたように, 本邦ではADHF 患者の約70%にカルペリチドが使用されているという数字は,多くの施設でカルペリチドがルーチンに使用されていることを意味する。これはすなわち,製薬会社にとっての素晴らしい成功を意味するが,患者にとって,また出資者である国民にとっても素晴らしい成功なのだろうか。
果たしてカルペリチドは,血管拡張薬かつまたは利尿薬という標準治療と比較して,臨床的な効果が勝り,押しも押されもせぬ“ルーチン使用薬”なのだろうか。
… “ルーチン使用薬”たる安全性が担保されているのだろうか。もし,カルペリチドと標準治療(例えば,ニトログリセリン+フロセミド)の効果と安全性が同等だとすれば,費用で2 倍以上の差のある治療法をルーチンで使用する妥当性をどこに見いだせばよいのか。さらに質の高い比較試験と健全な科学的議論のうえに白黒はっきりつけたいと考えるのは,それほど不自然なことではないと思うのだが。
こちらは現自治医科大学附属さいたま医療センターの麻酔科教授である讃井將満先生のコラムですが、なかなか厳しい言葉が並んでいますね😇こちらの本が出版されてから10年以上経ちましたが、急性心不全を対象としたカルペリチドのRCTは新たに出たんでしたっけ😇😇
続きまして、循環器ジャーナル71巻1号「ここが変わった!循環器診療 最新スタンダード」にある急性心不全のところの記述です😇
一方でANPアナログであるカルペリチドは使用可能であり,わが国での使用例も多いこともあり,わが国のガイドラインではclass IIa となっている.カルペリチドにおいては,後ろ向きの検討ではあるが,カルペリチ ド投与群のほうが硝酸薬よりも院内死亡率が高く,また入院期間も長期化し,入院コストも高かったと報告されており,まだエビデンスとしては不十分の状態で,血圧低下も来しやすいことから使用時の注意が必要である.
うーん、上述の文献を引用しながら、なかなか渋い記述になってますね😇
そして最後はU40心不全ネットワークの方々が執筆された「心不全治療薬の考え方、使い方」ですね😇
そして、もう一つ重要な点は「カルペリチドは急性心不全に対して安全で有効な薬剤なのか?」という問いに対して明確な答えが示されていないことである。米国において一時的に広く使用されていたネシリチド(BNP製剤)も同様に、腎機能悪化や短期予後の悪化が市販後のいくつかの後ろ向き研究によって示唆されていたが、ASCEND-HF試験にそのようなネガティブな結果は否定された(ただ、明確な予後改善効果も示されなかった)。この点に関しても、カルペリチドでは大規模な臨床試験による検証がなされないため答えは不明である。
あれ、なんかINTENSIVISTとほぼ同じ内容な気がするんですが😇
10年以上経ってもカルペリチドのエビデンスは微妙なままなんですね😇
ワイのお気持ちとしては、カルペリチドだけでなくエビデンスは微妙だけど日本で売れている薬ははっきりさせるためのRCTは行われない印象があるんですが、その辺どうなんでしょうね😇😇例えば○○○○ーフとか😇他にも色々あると思いますが😇
さてどうなんでしょう、カルペリチドに関してガイドラインもCOIが絡んでいるんでしょうか😇
ハンプを製造販売しているのは第一三共です。ガイドライン作成に関わった58名のうち、第一三共とCOIがあるのは22名です😇
班長は講師謝金等で2017年に約280万円受け取ってますね😇
んん、やっぱり班長はそんなにもらってないなーと思っていたとろ…
例の製薬マネーデータベースで2017年の第一三共からの報酬トップ20を確認したところ、見事班員の1人がトップに輝いているではないですか😇😇その額約1320万円😇😇あとふたりの班員もトップ20にランクインしており、それぞれ約950万円と580万円😇😇
気になる方はこちらをご覧ください😇
https://yenfordocs.jp/company/2017/146
この第一三共のランキングなんですが、2018年もお三方がランクインしているものの、2019年にはお一人のみのランクインとなってしまいました😇そして2020年には全員がランク外に😇😇ところが2021年は2017年にトップだった先生が3位に返り咲いています、おめでとうございます😇😇
ちなみに2016年は班長の先生も含めて4名がランクインされています😇😇
最後に前編で紹介したMurayama先生が執筆された、日本循環器学会とCOIについての論文を確認しておきましょう😇
こちらは日本循環器学会(JCS)の診療ガイドラインの作成者と製薬企業とのCOIを評価したもので、2016年から2020年の5年間にわたり、ガイドラインの作成に関与した著者に対する製薬企業からの報酬が分析されています😇
ガイドライン著者の94.4%にあたる877人が、総額約7100万USドルの報酬を受け取っている。
著者1人あたりの平均報酬額は約7万6千USドル、全報酬の85.2%は講演料、10.5%はコンサルティング料だった。
ガイドラインの委員長または副委員長を務めた44人全員が製薬企業から報酬を受け取っていた。これらの委員長に対する報酬の中央値は約42000米ドルで、他の著者に対する報酬の中央値(約1万9千USドル)よりも有意に高かった。
対象となった37のJCSガイドラインの著者の80%以上が、2016年から2020年の間に製薬企業から報酬を受け取っていた。特に「安定冠動脈疾患の血行再建術に関するガイドライン」の著者は、最高の中央値として約23万5千USドルを受け取っており、他のガイドラインと比較しても高額であった。
なるほど、循環器学会はホクホクしている学会なんですね😇
それでは次にいってみましょう😇
2型糖尿病の薬物療法のアルゴリズム第2版 (日本糖尿病学会)
https://www.jds.or.jp/uploads/files/article/tonyobyo/66_715.pdf
こちらはガイドラインではなくコンセンサスステートメントという位置付けですね😇
糖尿病はガイドラインも最近改訂されましたが、あちらは特定の薬剤を推奨するという感じではないのでこちらを選択しました😇
こちらでの目玉はやはり薬剤選択のアルゴリズムですよね😇
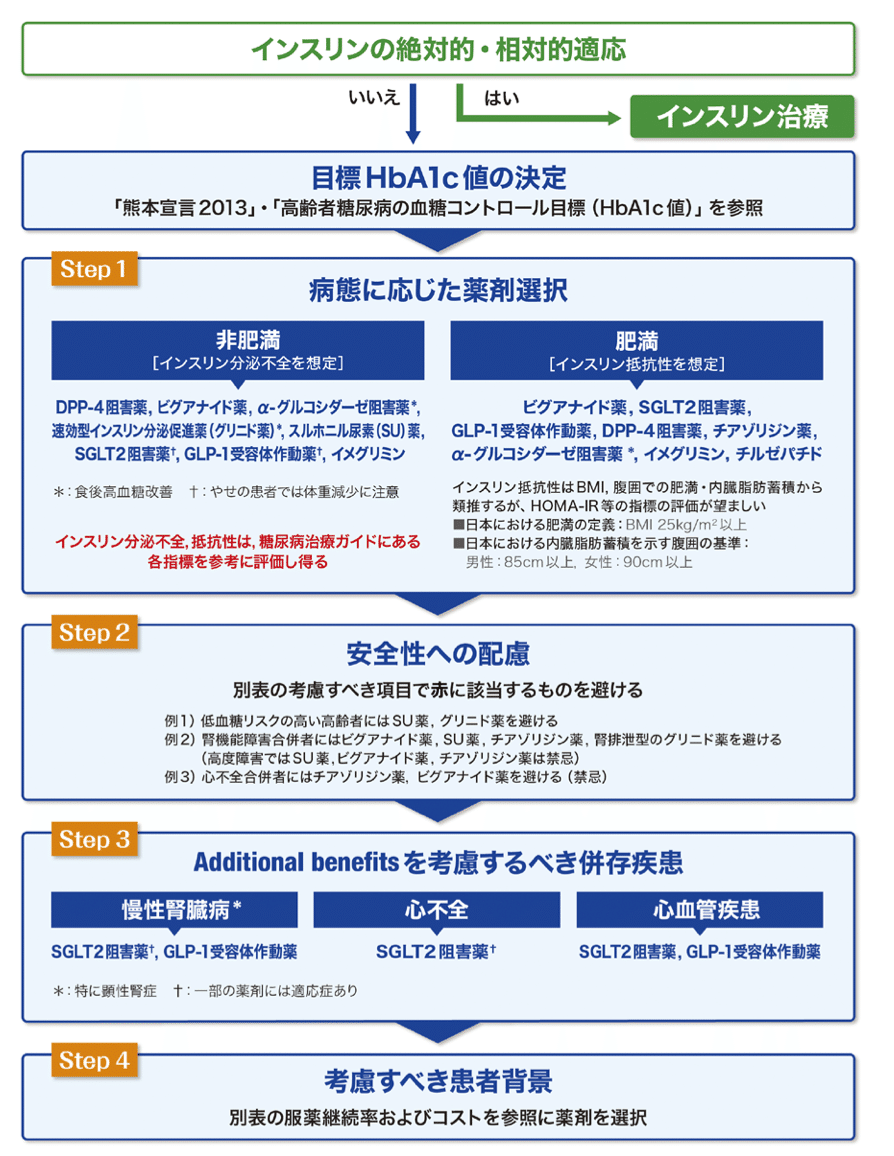
ほうほう、非肥満と肥満で分けろと😇
非肥満だとDPP-4の優先順位が高いのね😇
そしてアルゴリズム作成のコンセプトを確認すると…
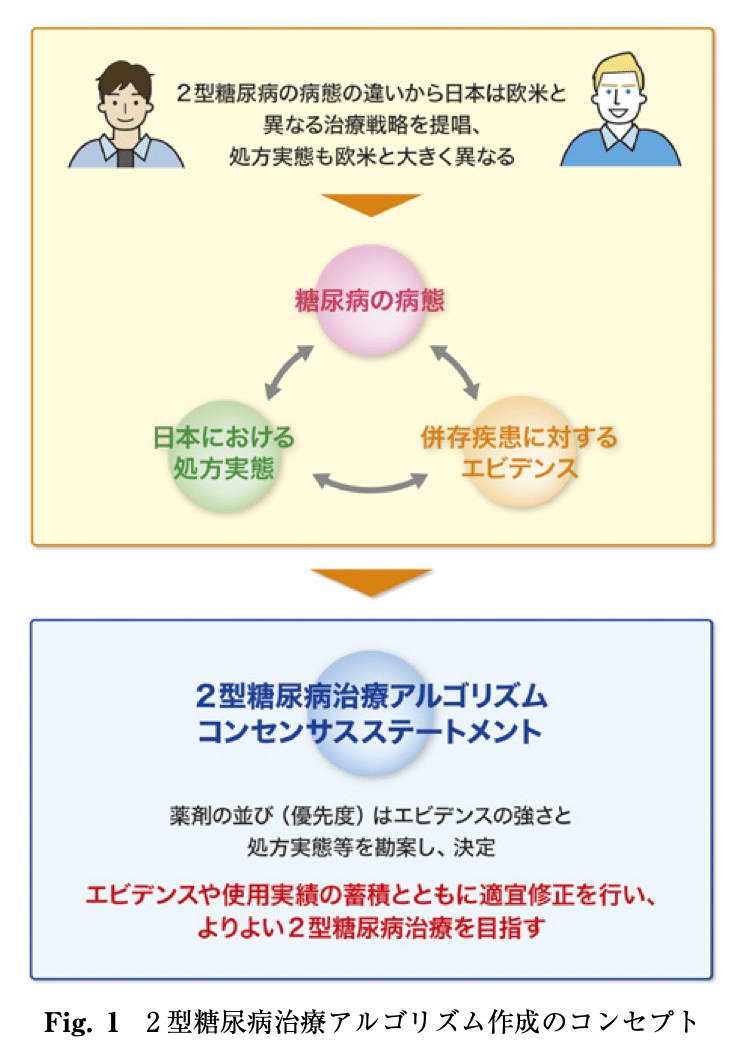
「薬剤の並び(優先度)はエビデンスの強さと処方実態等を勘案し、決定」
(;゚д゚)(つд⊂)ゴシゴシ(;゚Д゚)…?!
んんん⁉️薬剤の優先度はエビデンスの強さを勘案するのはわかるけど、処方実態⁉️
そこで本文を読んでみると…
匿名レセプト情報・匿名特定健診等情報データベース(NDB) に 2014 年度下半期から 2017 年度に登録された 100 万 人以上の 2 型糖尿病患者において,最も処方された糖尿病治療薬は,欧米とは異なり,DPP-4阻害薬であり…
ということは「日本では DPP-4が一番処方されているからアルゴリズムで優先順位を上げといたよ!」ってことかな⁉️
日本人を含めたアジア人の2 型糖尿病は欧米の2型糖尿病とその病態が異なることから,JDS は欧米とは異なる2型糖尿病の治療戦略を長きにわたって提唱してきた.実際に,我が国の2 型糖尿病に対する初回処方の選択も欧米と大きく異なることが明らかになったが,この事実は日本糖尿病学会の提唱する治療戦略が専門医に限らず実地医家にも広く浸透していることを示唆する.
ふむふむふむ…ふむ⁉️
すなわち、①学会が欧米とは異なる2型糖尿病の治療薬(DPP-4i)を提唱してきた→②我が国の処方はDPP-4iがシェアのトップに→③日本では DPP-4iが一番処方されているから今回のアルゴリズムでも優先順位を上げといたよ!
…あれ、なんか循環してる⁉️⁉️
そもそも多く処方されているからアルゴリズムの優先順位を上げるっていう論理もよくわからないんですが😇
ワイの頭がおかしいのかよくわからなくなってきました😇
とりあえず気を取り直して海外のガイドラインを覗いてみましょう😇
まずは米国糖尿病学会のガイドラインから😇
こちらは薬物治療のところですが、以下のアルゴリズムが有名ですね😇

大きくは心血管リスクを下げるための治療選択と、血糖と体重をコントロールするための薬物選択の二軸に別れてますね🧐
このアルゴリズムを含め、こちらのガイドラインではDPP-4iはあまり推されてはないようですね😇
続きまして米国内科学会(ACP)のガイドラインです😇
衝撃の推奨2はこちらですね😇
「ACPは血糖コントロールが不十分な成人の2型糖尿病患者に対して、合併症や死亡を減らすためにメトホルミンと非薬物療法にDPP-4iを加えないことを推奨する(強い推奨、高い確実性のあるエビデンス)」
これはなかなか強いものいいですね😇
そのあとに説明されてますが、DPP-4iを加えても死亡や心血管イベントを減らさないという強固なエビデンスがあるからですね😇
GLP1-RAやSGLT-2iと比べて死亡や心血管イベントを増やすかもしれないという話もありますね😇
うーん、日本の推奨と全然違う…
いや待てよ、日本人と欧米人では糖尿病の病態が異なるんだったな😇😇
コンセンサスステートメントから再び引用します😇
上述したように欧米の 2 型糖尿病の多くが肥満・インスリン抵抗性を主たる病態とするのに対し,日本人 2 型糖尿病はインスリン抵抗性とインスリン分泌不全 の寄与度が症例によって異なることが特徴である.
非肥満の2 型糖尿病の多くは,インスリン分泌不全 が病態の主体であるため,インスリン分泌促進系薬剤 を中心に薬剤選択を行う.DPP-4阻害薬は本邦の2型糖尿病の初回処方として最も多く選択されており,中でも高齢者での処方割合は極めて高く,DPP-4 阻害薬の高齢者における安全性への期待の大きさが示唆される.
ふむふむ😇
そして以下の論文を引用しながら、DPP-4iはアジア人には血糖降下作用が強いとしています😇😇
なになに、アジア人が50%を超える研究では50%以下の研究に比べてHbA1cが0.26%低かったと😇 BMIが低いとDPP-4iの効果が高かったと😇なるほどなるほど😇
結局非肥満の患者に対してDPP-4iがいいっているのは、病態生理的に合っているということと、血糖の下がりがよいという理由ですね😇
でも他の薬剤よりいいかどうかは他の薬剤と比べないとわからないですよね😇
病態整理だけで決めていいんでしょうか😇本当にメトホルミンやGLP1-RA, SGLT-2iより優先して出すべきなんでしょうか😇
それをはっきりさせるためには日本人の非肥満患者を対象にRCTをするしかないですね😇でもそれが行われているという話は聞いたことがないですね😇
なんか心不全のところでも似たような話がありましたね😇😇😇
もちろん自分もDPP-4iを処方しますよ、しかし積極的に選ぶ薬だとは自分は思わないです😇これは皆さんのご意見を待ちましょう😇
ということで、個人的にはCOIのかほりを感じるので、ちょっと調べてみましょう😇
こちらのステートメント作成に関わったのは12名、COIについて書かれているのはそのうち8名です😇残りの4名はCOIなしということなんですかね😇
DPP-4iは複数の製薬会社が製造販売しているので、会社ごとのCOIあり人数をまとめてみました😇
三和化学研究所 1
武田薬品 2
帝人ファーマ 1
日本ベーリンガーインゲルハイム 5
MSD 3
キッセイ薬品 2
協和キリン 2
小野薬品 4
アステラス製薬 2
田辺三菱製薬 4
第一三共 1
ノバルティスファーマ 1
住友ファーマ 8
DPP-4iでのシェアは小野薬品のグラクティブ、MSDのジャヌビア、トラゼンタの日本ベーリンガーインゲルハイム(日本BI)が3強なんですかね😇
3つの製薬会社COIを調べてみましたが、2022年だと小野薬品は4人とも50万円以下ですね😇MSDは3人とも50万から100万の間です😇日本BIは2023年だと1名は10万程度、3名は50-100万、1名は130万でした😇
どうなんでしょう、循環器と比べたら可愛いもんなんですかね😇😇
最後は恒例のMurayama先生の論文で締めましょう😇
この研究は、糖尿病診療ガイドライン2019の著者と製薬企業とのCOIを2016年から2020年の5年間で調べたものですね😇
ガイドラインの著者135人のうち、129人(95.6%)が製薬企業から少なくとも1回の報酬を受け取っていた。総額は約2300万USドルに達し、個々の著者に対する報酬の中央値は約9万USドルであった。
著者のうち74.1%(100人)が1万ドル以上、60.7%(82人)が5万ドル以上、47.4%(64人)が10万ドル以上の報酬を5年間で受け取っていた。特に、ガイドライン委員長は約20万ドルの報酬を受け取っていた。
著者135人のうち、80人(59.3%)は2016年から2018年にかけてCOIを自己申告していたが、日本糖尿病学会の規則により、年間500,000円(約4,683米ドル)未満の報酬は申告の対象外とされていた。このため、COIを申告していない55人の著者のうち、48人(87.2%)が実際には製薬企業から報酬を受け取っていたことが判明した。
うーんどうなんでしょうね😇循環器のほうが強いんですかね😇50万円以下は報告しないっていうのは多くの学会がそのようですね😇
それでは次にいってみましょう😇
DIC診療ガイドライン2024(案) (日本血栓止血学会)
こちらのガイドライン案ですが、やはり驚きの推奨はこちらですね😇😇
「敗血症に伴うDICに対してリコンビナントトロンボモジュリン製剤を投与することを強く推奨する(強い推奨/中の確実性のエビデンス:GRADE1B)
リコモジュリンを強く推奨すると😇😇
いやー、ワイはリコモジュリン使ったことがないもんで、ちょっとした衝撃でした😇あ、そんなガンガン敗血症みているわけではないですが😇ということで例によって海外のガイドラインであるSurviving Sepsis Campaign Guidelines 2021を確認しておきましょう😇
…あれ、リコミジュリンについて触れられてない⁉️
SSCG2016までは記載があったようですが、それがなくなってしまったようですね😇
そして忘れちゃいけない日本版敗血症診療ガイドライン2024(J-SSCG2024)もチェックしておきましょう😇
「敗血症DICに対して、リコンビナント・トロンボモジュリンの投与を行うことを弱く推奨する」
おお、こちらは弱いながらも推奨しているんですね😇しかし日本のガイドラインで推奨の強さが異なっているとな😇
まず、どうしてSSCG2021でリコモジュリンの記載が消え去ったのか、UpToDateを彷徨っていたところ、「Investigational and ineffective pharmacologic therapies for sepsis」で記載を見つけました😇😇
どうもこちらのRCTをもってリコモジュリンは意味なしと結論づけられたようでした😇
しかし、このSCARLET試験をもってリコモジュリンは意味なしとするのは違うのではという話があるようです😇😇
カチコむなんて話は聞いてはないですが、SSCGメンバーはDICをあまり分かってない可能性はあります。実はSCARLET試験は、全体ではDICを対象とした試験でないので、評価できないんですよ。あれはProf. Vincentが悪いです。 pic.twitter.com/ISxAXtb1Rb
— EARLの医学ツイート (@EARL_med_tw) September 14, 2024
JSSCG2024でも、そういったことを踏まえて系統的レビューを行ったようです😇
そして以下のような記載があります😇
4編のRCTの解析において, 死亡は1000 人あたり 39 人の減少(75 人減少~3 人増加)であり、3 編の RCT8-10)の解析において, DICからの離脱は 1000 人あたり 120 人の増加(4 人~274 人増加)であった。一方, 望ましくない効果は出血合併症であり, 4 編の RCT6,8-10)の解析において 1000 人あたり 12 人の増加(6人減少〜41人増加)であった。それぞれのアウトカムの相対的価値を考慮すると, 望ましい効果は「大きい」, 望ましくない効果は「わずか」と判断した。
ほうほうほう😇ちなみにこのシステマティックレビューにはさきほどのSCARLET試験に加えて、同じ著者のRCT,そしてあとの二つは日本からのRCTが含まれています😇😇
ワイが不勉強だったのですが、GRADEでは有意差のあるなしはでは考えず、効果量および95%信頼区間を踏まえて判断するようです😇作成者のひとりであるEARL先生から教えていただきました😇😇
作成メンバーとして補足しておくと、GRADEは有意差有無だけで判断するものではなく、数値的には効果量に加えて95%CIの上限と下限の絶対数がものを言います。p値慣習に染まってしまうと解釈の邪魔になってしまうので、トレーニングが必要な方法論です。
— EARLの医学ツイート (@EARL_med_tw) September 14, 2024
しかしこの辺の推奨はやはり過去に作成メンバーで議論があったことをEARL先生が明かされています😇
このあたりの解釈は実は2016年版作成時にDIC治療の項目でけっこうガイドラインメンバー内でもめた経緯があって、GRADE的には正しい、MINDs的には正しくない、で作成中に推奨が二転三転しました。
— EARLの医学ツイート (@EARL_med_tw) September 14, 2024
またEARL先生や他の先生から教わりましたが、ARDSのガイドラインなども含めて、集中治療医学会が作成に関わっているガイドラインはかなり厳密に作られているようです😇😇
ちなみにですが、敗血症ガイドラインでは作成に関わった158人のうちリコモジュリンの旭化成フォーマとCOIがあるのが5人だけ、しかしその中に委員・担当理事21人のうちの4人が含まれていて、そのうち2人は委員長と副委員長でした😇
— にゃんでもにゃ医 (@lE9BrvyUwLLVZIE) September 14, 2024
この推奨にCOIは関わっているのだろうかと考えていました😇
敗血症ガイドラインは、コアメンバー、ワーキンググループ、監視役のアカデミック班が三権分立状態で作成にあたってるため、COIを有する医師がいても変なことできないようになってます。
— EARLの医学ツイート (@EARL_med_tw) September 14, 2024
ガイドラインにも以下の記載があり、中立性の高いガイドラインのようです😇
日本医療機能評価機構の EBM 医療情報部が推奨する診療ガイドライン作成のための組織構成は、診療ガイドライン統括委員会、作成グループ、系統的レビューチームの 3 つである 。J-SSCG独自の取り組みとして、J-SSCG2020と同様にアカデミックガイドライン推進班を編成し、中立的な立場から診療ガイドライン作成を支援している。
ということでDICガイドラインに戻りましょう😇
…あれ、J-SSCG2024のリコモジュリンの推奨のところとまったく同じRCT4つでメタ解析されている⁉️なのに推奨が異なっている⁉️これはJ-SSCG2024かDICガイドラインのどちらかがアレということ⁉️
…気を取り直して読み込んでみましょう😇
4RCT 1527 症例を解析対象とした。全原因死亡について rTM 投与により小さな効果が見込まれる(1000 人当たり 39 人の減少)。出血性合併症は悪化せず、DIC 離脱については増加する可能性が高い。以上より、すべてのアウトカムにおいて rTM 投与により有益効果が期待される。
んーーん⁉️出血性合併症は悪化せず⁉️
まとめられているGRADEエビデンスプロファイルを確認しましょう😇

当然効果量と95%信頼区間はJ-SSCG2024と同じですよね、同じRCTを解析してるんだから😇
出血性合併症の効果量と95%信頼区間は12 more per 1,000(6 fewer to 41 more)でJ-SSCGと同じですね😇
ところが出血性合併症は悪化せずと断言しちゃってます😇上述のように、GRADEでは有意差の有無では語らないのでしたね😇仮に一貫性を持たせるとしたら、死亡も減らないと断言しないとですね、39 fewer per 1,000(75 fewer to 3 more)なんだから😇😇
うーん、これはちょっと漂ってきますね、アレのかほりが😇
と思って勇んで調べてみましたが、金額としては大したことはなさそうですね😇😇
委員長の先生が2021年に旭化成ファーマからの報酬トップ20にランクインされていますが、約150万円でかわいいものですね😇そもそも旭化成ファーマは今まで登場した製薬会社より医師に支払っている金額が少なそうです😇
https://yenfordocs.jp/company/2021/41
敗血症の章の作成委員の先生は4名ですが、旭化成ファーマからの報酬は多くても年間100万ちょっとなので、やはりかわいいもんですね😇
しかしなんか気になるなと思い、もう一つのCOIを確認してみました😇そう、アカデミックCOIですね😇
アカデミックCOIに関してはMindsの診療ガイドライン作成マニュアルにまとまっています😇
https://minds.jcqhc.or.jp/docs/materials/minds/old-minds-manual/2017/manual_2_2017.pdf

そしてなんと4名ともゴリゴリの(敗血症)DICの専門家・研究者ですね😇もちろんご自身の診療(医局?)でもリコモジュリンを使われているのでしょう😇
ガイドラインの中立性を保つためには、リコモジュリン何それおいしいのな先生も作成委員に含めるべきなんじゃないですかね、しりませんけど😇
まあでも学会としてもリコモジュリンが有用ということにしといたほうが学会のプレゼンスを高めることにもなるでしょうし、こうなるのも仕方ないんですかね、しりませんけど😇😇
他のガイドラインでは調べませんでしたが、どのガイドラインでもアカデミックCOIの影響はそれなりにあるのかもしれませんね😇😇
さてさて、残るは一つですね😇
ゾフルーザの使用についての新たな提言(日本感染症学会)
さてさて、大トリを飾るのはこちらですね😇
https://www.kansensho.or.jp/uploads/files/guidelines/teigen_231130_nashi.pdf
まず12歳以上の小児、および成人の外来治療、および重症患者の治療のところの結論を見てみましょう😇
これらを総合的に勘案し、12 歳〜19 歳および成人のインフルエンザに対し、バロキサビルはオセルタミビルと同等の推奨度で治療薬として位置付けることが可能と考えます。
内服薬の薬力学・薬効動態が不安定となる患者(血液透析患者、ショック、等)を除き、バロキサビルを重症患者の治療に単独で投与することは可能と考えます。
ぬぬぬ⁉️
当方ゾフルーザを使ったことがなくて驚きました😇
まずは海外の推奨をみてみましょう😇
まず2022年のWHOのガイドラインですね😇
https://iris.who.int/bitstream/handle/10665/352453/9789240040816-eng.pdf?sequence=1
もちろんバロキサビルのバの字もありませんが、これはWHOなのでしゃーないですね😇😇
そもそも発売が2018年3月ですし😇
タミフルのエビデンスのまとめは見やすくていいですね😇
続きましてIDSAのガイドラインですが、ノイラミニダーゼ阻害薬しか記載がないですね😇出たのが2018年12月で、まだ米国でも市場に出てなかったでしょうし、しゃーないですね😇
続きまして、2023年12月に出たCDCのまとめですね😇
ついにバロキサビルの文字が😇😇
これはすこし詳しく読んでみましょう😇
まず入院患者や重症患者にはオセルタミビルを推奨となってますね😇今回の提言は使ってもいいという記載でしたが😇
あとリスクのある患者もオセルタミビル推しですね😇提言では明言はされていない気もしますが、リスクがあってもオセルタミビルと同等に推奨ということだと思います😇すくなくともリスクがあればオセルタミビルという記載はないですね😇
免疫抑制患者にはバロキサビルは推奨しないとなってますね😇提言では使ってもいいかも的なノリですが😇
そしてついに、健康な外来患者では他の抗ウイルス薬に加えてバロキサビルも使ってもよいと😇あと、インフルBにはバロキサビルがいいかもという記載もあります😇
根拠になっているのはこの論文ですね、提言でももちろん引用されています😇ちなみに塩野義製薬がスポンサーです😇
ということでCDCのまとめではバロキサビルの立ち位置は提言とはだいぶ異なっていますね😇
最後に2023年のカナダのガイドラインです。
2020年にバロキサビルが承認されたがまだ市場に出ていないと😇残念😇
ということで海外のガイドラインとはだいぶ異なっているようですね😇あまりゾフルーザが出回ってない感もありますが😇
さて、提言で引用されている論文を舐めるようにみていきたいのですが、もう息切れ気味なので一つだけとりあげます😇
最近,わが国から報告されたシステミックレビューとメタ解析では、外来患者を対象とした 2 つの RCT において、バロキサビルはオセルタミビルと比較して、有意にウイルスのtiterとRNA 量の低下、有害事象の減少を認め、罹病期間が短い傾向にあったとしています
上記で引用されている論文がこちらですね😇
バロキサビルの効果をみたシステマティックレビュー・メタ解析ですが、2つのRCTと2つの後ろ向き研究が解析されています😇
アブストの結果は以下のようになっています😇
Among inpatients, BXM reduced mortality (p = 0.06) and significantly shortened hospitalization period (p = 0.01) compared to oseltamivir. In outpatients, BXM had a significantly lower incidence of adverse events (p = 0.03), reductions in influenza virus titers (p < 00.001) and viral RNA loads (p < 00.001), and a tendency to be a shorter illness duration compared with that of oseltamivir (p = 0.27).
ほーほー😇そして"Our findings support the use of BXM in the initial treatment of patients with influenza virus infection”で締め括られています😇ほーほー😇
この論文について我らが山本先生と岩田先生がご意見されています😇
こちらの山本先生のご意見はレターとして取り上げられていますね😇
バロキサビルとオセルタミビルを比べたメタアナリシスにレターを書きました。
— Shungo Y (@bizarreID) March 4, 2024
Caution when incorporating observational studies into a meta-analysis https://t.co/InfetmTfxP
そしてこちらがイワケン先生のコメントです😇登録すれば読めると思います😇
岩田先生もレターを書かれたそうですが、「それってあなたの憶測ですよね」といわれてリジェクトされた話は笑ってしまいました😇😇
妥当な考察だと思いましたが😇
ワイも雑な考察を試みています😇
これを持ってタミフルじゃなくてゾフルーザを第一選択にすべきって結論はヤバすぎでしょ😇
— にゃんでもにゃ医 (@lE9BrvyUwLLVZIE) October 29, 2023
4つの研究のうち2つは後ろ向きコホートやで😇その後ろ向き2つは死亡率をみてるけど、統合しても優位差ないし😇RCTのうち一つは症状持続時間をみていて優位差なし、もう一つのRCTはprimaryは https://t.co/XRblDOkTcb pic.twitter.com/fAUbNGVwQU
さらにですよ、問題はやはりCOIですよ😇😇
None of the authors has any financial relationships with any commercial entity with an interest in the subject of this manuscript.
None of the authors have financial and non-financial competing interests.
ほんまかいな😇😇
と思いながら著者を確認すると、ラストオーサーのお名前に見覚えが😇😇
今回の提言の著者でもありますね😇😇
感染症学会でご高名な先生ですね😇😇
塩野義製薬のホームページで確認すると講師謝金だけで2022年は約93万円、2023年は約220万円もらっているようです😇😇
これは記載しなくていいんでしょうか😇
Journal of Infection and Chemotherapyは感染症学会の学会誌なので、感染症学会のCOI規定を確認しておきましょう😇
企業・組織や団体から、会議の出席(発表、助言など)に対し、研究者を拘束した時間・労力に対して支払われた日当(講演料など)については、一つの企業・団体からの年間の講演料が合計50万円以上とする。
んー、やっぱりCOIありとして記載すべきなんじゃないですかね😇
学会のお偉いさんだからその辺はオッケーなんですかね😇😇
ということで今回の提言のCOIを確認していきましょう😇
2023年は著者12人のうち10人が塩野義製薬から講師謝金等を受け取っています😇
その中でも一際目を引くのが約890万円を受け取っている先生ですね😇
講師謝金の件数が86となっているんですが、これは講演を86回したということなんでしょうか😇週1以上で講演していることになっちゃうのでさすがに違うんですかね😇
ちなみに2位が約350万円の先生で、3位が先ほどの約220万円の先生と続いています😇
著者たちが受け取っている謝金等を合わせると約2千万円となります😇😇
ちなみに著者たちに対する2022年の謝金等は合計約600万円でした😇2023年は額が跳ね上がっているのはこの提言にむけて講演会パルスをしたんでしょうか、わかりませんが😇😇
ちなみに前編で日本感染症学会のCOIについての論文を取り上げているのでご確認いただけたらと思います😇
最後に
いかがだったでしょうか😇
日本のガイドラインはCOIの影響を受けているのでしょうか😇
調べた限りでは少なくとも影響がないとは言えないという感じでしょうか😇
前編では2019年当時のガイドラインの質が低いという論文を取り上げましたが、それ以降のガイドラインは質が高くなっているのでしょうか😇
もしかしたらまだ道のりは遠いのかもしれませんね😇
先日ガイドラインがCOIの影響を受けてしまう一因らしきものを発見しました😇
そりゃCOIも必要になりますわ😇😇
— にゃんでもにゃ医 (@lE9BrvyUwLLVZIE) September 24, 2024
ガイドラインの質を高めるには教授のお給料を何倍かにしないと😇😇 https://t.co/OaedYs8FUg
いやもう教授の給料低すぎでしょ😇これは由々しき問題ですよ😇
そりゃ製薬会社からお金をもらわないとやっていけませんよ😇
最低でもこれの4倍は必要でしょう😇
といっても大学の給与体系が変わる兆しもないですし、ここはどうしようもないですね😇
ここ以外で日本のガイドラインの質を高めるにはどうしたらよいのでしょうか😇ガイドラインの実態を多くの方に知ってもらうことも重要だと思い、このnoteを書いたというのもあります😇
集中治療医学会のように、昔はアレだったけど、近年は質の高いガイドラインを量産している学会もあります😇
一方でそうではない学会もあるようです😇😇
この違いはなんなんでしょうね。結局は学会上層部がアレかどうかなんでしょうか😇学会上層部が新しい風を受け入れれるかどうかにかかっているんでしょうか😇集中治療医学会はなぜその辺で成功しているのか、ご存知の方は教えてください😇
ガイドラインの質を高める方策についてお考えのある方もぜひ教えてください😇
最後になりましたが、今回のnoteは何人かの先生に内容についてご相談させていただきました😇大炎上は避けたかったですし😇色々なことを教えていただく機会にもなりました、本当にありがとうございました!
今回もどしどしご感想ご批判をお寄せください😇😇
最後までお読みいただきありがとうございました!
