
松廼屋|論点解説 薬剤師国家試験対策ノート問106-100【物理】論点:吸着・脱着 / ラングミュアの吸着等温式
第106回薬剤師国家試験|薬学理論問題 /
問100
一般問題(薬学理論問題)【物理】
問106-100
Q. 以下の図と文章は、化学吸着における単分子層形成を表すラングミュアの吸着等温式(式1)の誘導についてのものである。文章中の[ア]及び[イ]にあてはまる式の正しい組合せはどれか。1つ選べ。

Γ=Γ∞*KC/(1+KC) ・・・式1
吸着質の濃度をC、吸着媒の吸着サイトの全数をΓ∞、吸着質が占有している吸着サイトの数をΓとする。
上図では、Γ∞=10、C=5の場合を示す。
吸着媒に対する吸着質の吸着過程の速度定数をk1、脱着過程の速度定数をk-1とし、吸着平衡が成立していれば、吸着速度と脱着速度は等しいから、[ア]の関係が成り立つ。[ア]を変形すると、式1が得られる。
ただし、K= [イ]であり、この値は吸着質と吸着媒の親和性を表し、大きいほど親和性が高い。
ア|イ
選択肢|
1. k1C = k-1Γ|k1 / k-1
2. k1C = k-1Γ|k-1 / k1
3. k1C = k-1(Γ∞ - Γ)|k1 / k-1
4. k1C = k-1(Γ∞ - Γ)|k-1 / k1
5. k1C(Γ∞ - Γ) = k-1Γ|k-1 / k1
6. k1C(Γ∞ - Γ) = k-1Γ|k1 / k-1
こんにちは!薬学生の皆さん。
Mats & BLNtです。
matsunoya_note から、薬剤師国家試験の論点解説をお届けします。
苦手意識がある人も、この機会に、薬学理論問題【物理】を一緒に完全攻略しよう!
今回は、第106回薬剤師国家試験|薬学理論問題 / 問100、論点:吸着・脱着 / ラングミュアの吸着等温式 を徹底解説します。
薬剤師国家試験対策ノート NOTE ver.
matsunoya_note|note https://note.com/matsunoya_note
Here; https://note.com/matsunoya_note/n/ncf1cf2b5f59f
松廼屋|論点解説 薬剤師国家試験対策ノート問106-100【物理】論点:吸着・脱着 / ラングミュアの吸着等温式
薬剤師国家試験対策には、松廼屋の eラーニング
「薬剤師国家試験対策ノート」
マガジン|薬剤師国家試験対策ノート on note
👉マガジンをお気に入りに登録しよう!
このコンテンツの制作者|
滝沢 幸穂 Yukiho Takizawa, PhD
https://www.facebook.com/Yukiho.Takizawa
お友達や知り合いに、matsunota_note で学習したeラーニングを勧めてみたい方は、いいね!、口コミ、おススメなど、よろしくお願いします!
設問へのアプローチ|

第106回薬剤師国家試験の問100(問106-100)では、吸着・脱着 / ラングミュアの吸着等温式 に関する知識を問われました。
第106回薬剤師国家試験 薬学理論問題【物理】のラスト問題です。
ABCDアイウエオ構文🤢🤮…キタ…選択肢6…😭🤣⏱️
👽👾ヒヒッ。。
でも、ここで焦ってはいけません。
大丈夫です。
論点を整理しておきましょう。
今回、GPT4o にお願いして、論点をまとめてもらいました。
※ラングミュアの吸着等温式詳細については、あらためてLectureで徹底解説します。
完全攻略を目指せ!
■■GPT4o
総合的な論点
1.吸着速度と脱着速度の関係式の選定
問題文の [ア] に該当する式を正しく選定する。
2.吸着平衡定数Kの式の選定
問題文の [イ] に該当する吸着平衡定数Kを正しく選定する。
3.ラングミュアの吸着等温式の誘導
吸着速度と脱着速度から、ラングミュアの吸着等温式を導出する。
Γ=Γ∞*KC/(1+KC)
4.吸着質と吸着媒の親和性の解釈
平衡定数Kの値が吸着質と吸着媒の親和性を示すことを、定数の物理的意味とともに解釈する。
各論点に関する解法へのアプローチ方法
吸着速度と脱着速度の関係式
吸着速度と脱着速度の平衡を考えると、吸着質が吸着サイトに吸着する速度(吸着速度)と、吸着サイトから脱着する速度(脱着速度)が等しい状態が成立します。
これを数式で表すと、吸着速度k1Cと脱着速度k-1Γが等しいという関係が成り立ちます。
したがって、基本形として考えられる関係式は次のようになります。
k1C=k-1Γ
ここでΓは吸着サイトに吸着している吸着質の量、Cは吸着質の濃度です。吸着平衡の条件を元に、この基本式を変形していくと、[ア] に該当する式を特定できます。
吸着平衡定数Kの式
吸着平衡定数Kは、吸着質と吸着媒の親和性を表す定数です。
一般的に、吸着平衡定数Kは次のように定義されます。
K=k1/k-1

この式は、吸着速度定数k1と脱着速度定数k-1の比であり、吸着媒に対する親和性が高いほど、Kの値は大きくなります。
[イ] に該当する式はこの関係式を反映している必要があります。
ラングミュアの吸着等温式の誘導
吸着速度と脱着速度の関係を基に、ラングミュアの吸着等温式を導きます。
吸着が進むと、吸着サイトの限界値Γ∞が存在し、吸着していないサイトの数はΓ∞ -Γとなります。

これを考慮した吸着速度と脱着速度の関係式は次式であらわされます。
k1C(Γ∞ -Γ) =k-1Γ
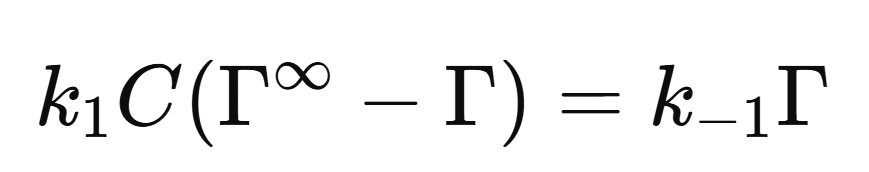
この式は、吸着サイトの限界数Γ∞を考慮したもので、吸着と脱着が平衡に達している時の関係を表しています。
この式を整理して、Γについて解くと、ラングミュアの吸着等温式に対応する次の式が得られます。
(k1/k-1)C(Γ∞ -Γ) =Γ
KC(Γ∞ -Γ) =Γ
KCΓ∞-KCΓ =Γ
Γ + KCΓ = Γ∞*KC
Γ(1 + KC) = Γ∞*KC
Γ =Γ∞*KC/(1+KC)

ここで、K=k1/k-1です。
これにより、吸着の平衡状態における吸着質の量が吸着媒に対してどのように分布するかが表されます。
吸着質と吸着媒の親和性の解釈
吸着平衡定数Kの値は、吸着質と吸着媒の親和性を示します。
Kの定義は以下の通りです。
K=k1/k-1
この値が大きいということは、吸着速度定数k1が脱着速度定数K-1よりも大きい、すなわち吸着質が吸着媒に強く結びつきやすいことを意味します。
逆に、Kが小さい場合は、脱着速度が速く、吸着媒に対する親和性が低いことを示します。
したがって、Kの大きさによって吸着質が吸着媒にどれだけ強く吸着されるか、また吸着がどれだけ安定しているかがわかります。
吸着平衡定数Kは吸着現象における重要な指標です。
特に工業的な吸着プロセスでは重要な設計パラメータとなります。
詳細は、Lectureで後述します。(抜粋)
■■GPT4o

論点解説 ラングミュア吸着等温式 概論
どうですか?
じわじわ来てますか🖐️😎🖐️
🖐️😎🖐️
楽勝です!
はじめましょう。
薬剤師国家試験の薬学理論問題【物理】から吸着・脱着 / ラングミュアの吸着等温式 を論点とした問題です。
なお、以下の解説は、著者(Yukiho Takizawa, PhD)がプロンプトを作成して、その対話に応答する形でGPT4o & Copilot 、Gemini 1.5 Pro、またはGrok 2 (beta) が出力した文章であって、著者がすべての出力を校閲しています。
生成AIの製造元がはっきりと宣言しているように、生成AIは、その自然言語能力および取得している情報の現在の限界やプラットフォーム上のインターフェースのレイト制限などに起因して、間違った文章を作成してしまう場合があります。
疑問点に関しては、必要に応じて、ご自身でご確認をするようにしてください。
松廼屋|論点解説 薬剤師国家試験対策ノート問106-100【物理】論点:吸着・脱着 / ラングミュアの吸着等温式|matsunoya (note.com)
Here we go.
第106回薬剤師国家試験|薬学理論問題 /
問100
一般問題(薬学理論問題)【物理】
問106-100
Q. 以下の図と文章は、化学吸着における単分子層形成を表すラングミュアの吸着等温式(式1)の誘導についてのものである。文章中の[ア]及び[イ]にあてはまる式の正しい組合せはどれか。1つ選べ。

Γ=Γ∞*KC/(1+KC) ・・・式1
吸着質の濃度をC、吸着媒の吸着サイトの全数をΓ∞、吸着質が占有している吸着サイトの数をΓとする。
上図では、Γ∞=10、C=5の場合を示す。
吸着媒に対する吸着質の吸着過程の速度定数をk1、脱着過程の速度定数をk-1とし、吸着平衡が成立していれば、吸着速度と脱着速度は等しいから、[ア]の関係が成り立つ。[ア]を変形すると、式1が得られる。
ただし、K= [イ]であり、この値は吸着質と吸着媒の親和性を表し、大きいほど親和性が高い。
ア|イ
選択肢|
1. k1C = k-1Γ|k1 / k-1
2. k1C = k-1Γ|k-1 / k1
3. k1C = k-1(Γ∞ - Γ)|k1 / k-1
4. k1C = k-1(Γ∞ - Γ)|k-1 / k1
5. k1C(Γ∞ - Γ) = k-1Γ|k-1 / k1
6. k1C(Γ∞ - Γ) = k-1Γ|k1 / k-1
■■GPT4o
物理|問 106-100
■論点|吸着・脱着 / ラングミュアの吸着等温式
この問題の論点は、ラングミュアの吸着等温式を導出する際の吸着速度と脱着速度の関係、および吸着平衡定数Kの表現を特定することです。
■解説1|
吸着速度と脱着速度の関係 (アの選択肢について)
吸着が進行する際、吸着媒の表面に吸着する吸着質の濃度を C、吸着質が占有している吸着サイトの数をΓ、全吸着サイトの数をΓ∞とします。
吸着速度はk1C(Γ∞ -Γ) で表されます。
ここでΓ∞ -Γは、吸着されていないサイトの数です。脱着速度はk-1Γで表されます。これは、吸着されたサイトから吸着質が離れる速度です。
吸着と脱着が平衡状態にあるとき、これらの速度は等しくなり、次の関係が成り立ちます。
k1C(Γ∞ - Γ) =k-1Γ
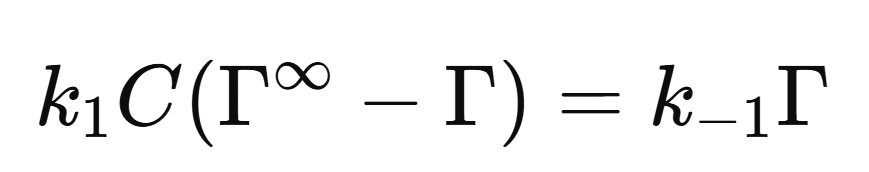
この式を変形すると、ラングミュアの吸着等式 が得られます。
Γ=Γ∞*KC/(1 + KC)

■解説2|吸着平衡定数Kの定義 (イの選択肢について)
吸着平衡定数Kは、吸着と脱着の速度定数k1およびk-1を用いて次のように定義されます。
K=k1/k-1
この平衡定数Kは、吸着質と吸着媒の親和性を示し、Kが大きいほど吸着質が吸着媒に強く結びつき、脱着しにくいことを意味します。逆に、Kが小さい場合は脱着しやすく、吸着質が吸着媒に対する親和性が低いことを示します。
したがって、[イ] に当てはまるのは「K=k1/k-1」です。
■結論|
[ア] の正答は5. k1C(Γ∞ - Γ) = k-1Γ です。
[イ] の正答は4. K= k1/k-1 です。
選択肢5が正答です。
■補足|
ラングミュア吸着等温式の物理的意味
吸着速度k1C(Γ∞ -Γ) は、吸着サイトが満たされるほど小さくなり、脱着速度k-1Γは吸着サイトが多く占有されるほど大きくなります。
吸着と脱着が平衡状態にあるとき、これらの速度は等しくなり、次の関係が成り立ちます。
k1C(Γ∞ - Γ) =k-1Γ
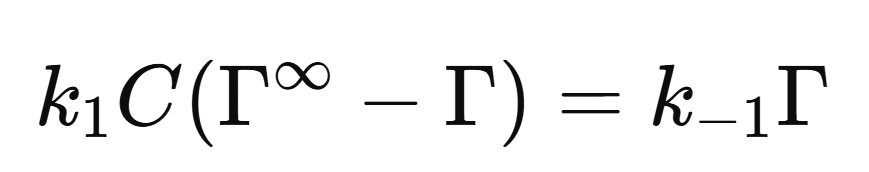

■Lecture
■■GPT4o
論点解説 ラングミュア吸着等温式 概論
1. ラングミュア吸着等温式とは
1.1 背景と歴史
ラングミュア吸着等温式は、1916年にアーヴィング・ラングミュア(Irving Langmuir)によって提唱された吸着理論です。
彼は、吸着現象を単分子層(モノレイヤー)としてモデル化し、吸着サイトに吸着質が均一に吸着する仮定に基づいています。この理論は、表面化学の分野で画期的な発見とされ、特に化学吸着(化学的な相互作用を伴う吸着)の研究において重要な役割を果たしました。
ラングミュアの功績と受賞歴
ラングミュアは、物理化学の分野での貢献により、1932年にノーベル化学賞を受賞しました。
科学的背景
ラングミュア吸着等温式は、固体表面にガスや液体が吸着される現象を数式化することで、吸着平衡の理解を深めることを目的として開発されました。この理論は、吸着質が固体の表面に単分子層として吸着する際の平衡状態を表し、化学吸着の基本的なモデルとして現在でも広く使用されています。
吸着とは何か:吸着現象の概要
吸着の定義
吸着とは、気体または液体の分子が固体または液体の表面に引き寄せられ、表面に蓄積する現象を指します。この現象は、物理的な力(ファンデルワールス力)または化学的な相互作用(化学結合)に基づいて起こります。
吸着の逆プロセスを脱着と呼びます。
吸着の種類
吸着には、以下の2つの主要な種類があります。
物理吸着(ファンデルワールス吸着)
特徴:吸着質と吸着媒の間に弱いファンデルワールス力が働く。一般的に低温で起こり、可逆的(脱着が容易に行われる)です。
例:ガス分子が固体表面に弱く吸着する際など。
化学吸着(ケミソプション)
特徴:吸着質が吸着媒と強い化学結合を形成するため、より高いエネルギーが関与し、不可逆的な場合もあります。触媒反応やガスセンサーの働きに関連しています。
例:金属表面に酸素が吸着する現象。
吸着の具体的な例
ガス吸着:石炭や活性炭が有害ガスを吸着することで浄化するプロセス。
活性炭は表面積が大きく、多数の吸着サイトを持つため、有効な吸着剤として使用されます。液体吸着:液体の溶質が固体表面に吸着されるプロセス。
例として、水中の有害化学物質が活性炭によって除去されることが挙げられます。
吸着の重要性
吸着は多くの産業で応用されており、以下のような領域で重要な役割を果たします。
触媒反応:触媒の表面に反応物が吸着する。で、反応を促進します。
環境保護:大気中の汚染物質を除去するための吸着プロセスが使用されます(例:ガスマスクや空気清浄機)。
ガス分離技術:特定のガス分子のみを吸着する材料を使って、ガスの分離や精製が行われます。
1.3 吸着と脱着の基礎概念
吸着と脱着のプロセス
吸着と脱着は、分子が固体表面に結合したり、そこから離れる現象です。このプロセスは以下のように進行します。
吸着:
気体や液体の分子(吸着質)が固体表面(吸着媒)の特定のサイトに結合する現象。
吸着が進むと、吸着サイトが埋まっていき、最終的には飽和状態に達します。吸着速度は、吸着質の濃度と吸着サイトの空き具合に依存します。脱着:
吸着された分子が固体表面から離れるプロセス。脱着が進むと、表面の吸着サイトが再び利用可能になります。
脱着は温度の上昇や表面の状態変化により促進されることがあります。
吸着平衡
吸着と脱着は逆向きのプロセスであり、ある条件下では両者の速度が等しくなり、吸着平衡に達します。
この平衡状態では、吸着される分子の数と脱着される分子の数が等しく、システムは安定します。
吸着速度:
吸着質が吸着媒に結合する速度は、吸着質の濃度と吸着媒の表面サイトの空き具合に依存します。吸着速度は、通常「吸着定数 k1 」で表されます。脱着速度:
脱着プロセスは、温度や吸着サイトに存在する吸着質の状態に影響されます。脱着速度は「脱着定数 k-1 」で表されます。

吸着平衡の成立条件
吸着と脱着が同じ速度で進行する場合、吸着平衡が成立します。吸着平衡では、次のような関係式が成り立ちます。
k1C=k-1Γ
ここで
k1は吸着速度定数
Cは吸着質の濃度
k-1は脱着速度定数
この関係は、吸着平衡における吸着質の濃度や吸着サイトの状態を理解するための基本となります。
ラングミュア吸着等温式への接続
吸着と脱着の平衡状態を基に、吸着サイトに吸着された分子の数を吸着質の濃度と吸着平衡定数Kによって表すことができます。これがラングミュア吸着等温式の基礎であり、次のステップで詳しく説明します。
2. ラングミュア吸着等温式の導出
2.1 単分子層吸着の仮定
単分子層吸着とは
ラングミュア吸着等温式の導出において、最も重要な仮定の一つが「単分子層吸着」の概念です。これは、吸着が固体表面において1層の吸着質分子で完全にカバーされることを意味します。
単分子層:
吸着媒の表面には一定数の吸着サイトがあり、各吸着サイトには最大1つの吸着質分子が結合できると仮定されます。つまり、各サイトには1つの分子しか吸着できないので、吸着は多層ではなく単層で進行します。均一な表面:
吸着媒の表面は均一であり、すべての吸着サイトは同じ性質を持っていると仮定されます。すなわち、どのサイトも同じ吸着エネルギーを持つため、吸着はどの部位でも同じ条件下で進行します。
仮定の意義
この単分子層吸着の仮定により、ラングミュア吸着等温式は非常に簡潔な形式で表現されます。この仮定は、以下の特徴を持つシステムに適用可能です。
ガス吸着:
気体分子が固体表面に吸着する際、吸着される分子は単分子層を形成する場合が多い。触媒反応:
触媒の表面に反応物が吸着して反応を開始する場合も、単分子層吸着が起こります。
仮定の限界
この仮定は、現実の多くの吸着現象に対して単純化されすぎている場合があります。例えば、多層吸着や吸着サイトごとにエネルギーが異なる場合には、このモデルでは正確な説明が困難です。そのため、ラングミュア吸着等温式は、特に単分子層吸着が支配的な条件下で使用されます。
2.2 吸着速度と脱着速度の定式化
吸着速度と脱着速度の考え方
ラングミュア吸着等温式は、吸着と脱着が時間経過に伴って進行する速度を基にしています。吸着と脱着の速度をそれぞれ数式で表すことで、吸着平衡に達する条件を導きます。
吸着速度
吸着速度は、吸着質が吸着媒の表面に結合する速度です。吸着速度は吸着質の濃度と表面に空いている吸着サイトの数に比例します。以下の式で表されます。
吸着速度 = k1C(Γ∞ -Γ)
ここで
k1は吸着速度定数
Cは吸着質の濃度
Γ∞は吸着媒の全吸着サイトの数
この式は、吸着質が吸着媒の表面に吸着する際の速度が、吸着質の濃度と吸着サイトの空き具合(Γ∞ -Γ)に依存することを示しています。
脱着速度
脱着速度は、吸着された分子が吸着媒の表面から離れる速度です。脱着速度は、占有されている吸着サイトの数に比例します。以下の式で表されます。
脱着速度 =k-1Γ
ここで
k-1は脱着速度定数
Γは占有されている吸着サイトの数に比例します。以下の式で表されます。
この式は、脱着が進む速度が吸着サイトに吸着された分子の数(Γ)に依存することを示しています。
吸着平衡
吸着速度と脱着速度が等しいとき、吸着平衡が成立します。吸着平衡では、以下の関係が成り立ちます。
k1C(Γ∞ -Γ) =k-1Γ
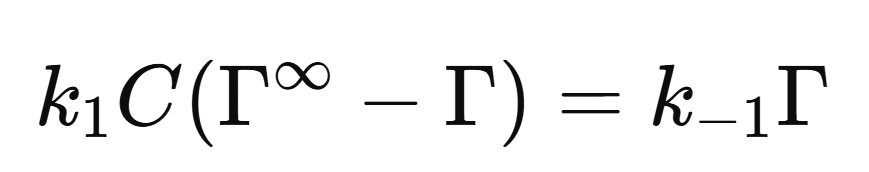
この式は、吸着平衡において吸着と脱着がどのようにバランスしているかを定量的に示す重要な関係式です。この平衡式を変形することで、ラングミュア吸着等温式が導出されます。
2.3 ラングミュア吸着等温式の導出
ラングミュア吸着等温式は、前述の吸着速度と脱着速度の平衡から導き出されます。この式は、吸着質の濃度Cと、吸着媒の表面に吸着されている吸着質の割合を定量的に表すものです。
平衡式の再掲
前のステップで示した吸着と脱着の速度の平衡式は次の通りです:
k1C(Γ∞ -Γ) =k-1Γ
この式を用いて、吸着質の数Γを求めます。
平衡定数Kの定義
吸着と脱着の速度定数を用いて、吸着平衡定数Kを次のように定義します。
K= k1 / k-1
これは、吸着が起こる傾向と脱着が起こる傾向の比を表し、吸着質と吸着媒の親和性を示します。値が大きいほど、吸着質が吸着媒に強く引き寄せられることを意味します。
等温式の導出
平衡定数Kを用いて平衡式を整理します。
KC (Γ∞ -Γ) =Γ
次に、式をΓについて解きます。
Γ∞KC – ΓKC = Γ
Γ+ΓKC = Γ∞KC
Γ(1+KC) = Γ∞KC
Γ =Γ∞*KC/(1+KC)
これがラングミュア吸着等温式です。

式の意味
この式は、吸着平衡において、吸着される物質の量が吸着媒の特性や吸着質の濃度にどのように依存するかを示します。
グラフの形状
吸着質の濃度Cを増やすと、初めはΓが急激に増加しますが、やがてΓ∞に近づき、飽和に達します。これは、すべての吸着サイトが埋まり、これ以上の吸着が起こらない状態を表します。
2.4 ラングミュア吸着等温式の応用
ラングミュア吸着等温式は、様々な分野で応用されています。特に、物理化学や表面科学において、固体表面への気体や溶液中の物質の吸着現象を理解するための基本モデルとして使用されます。
1. 触媒作用における応用
触媒の表面における反応では、反応物が触媒表面に吸着され、その後化学反応が進行します。ラングミュア吸着等温式を使用することで、反応物の濃度と触媒表面に吸着される反応物の割合を予測できます。この情報は、触媒の効率や反応速度を解析する上で重要です。
工業触媒: アンモニア合成やガソリン精製など、多くの工業プロセスで触媒が使用されます。これらの反応では、吸着が反応速度に大きく影響を与えるため、ラングミュアのモデルが役立ちます。
2. 表面科学における応用
固体表面の特性を理解するために、吸着等温式は欠かせません。固体表面へのガス分子の吸着は、表面の性質や構造を調べるための手段として利用されます。
表面解析: ラングミュア吸着等温式を用いて、表面の吸着サイトの数や表面エネルギーを推定できます。これにより、材料の表面性質を明らかにし、材料設計や改良に活用されます。
3. バイオセンサーにおける応用
バイオセンサーの多くは、検出対象物(例:抗原、抗体、DNA)がセンサーの表面に吸着することで動作します。ラングミュア吸着等温式を使って、吸着の動力学を予測することで、センサーの感度や応答速度を最適化することが可能です。
DNAマイクロアレイ: ラングミュア吸着等温式は、DNAやタンパク質が固体表面にどのように吸着し、どの程度の濃度で飽和に達するかを解析するのに役立ちます。
4. ガス吸着における応用
ガスの貯蔵や分離、浄化プロセスにおいて、ラングミュア吸着等温式は広く使われています。特に、ゼオライトや活性炭などの多孔質材料へのガス吸着を解析するための基本モデルです。
ガス分離技術: ラングミュア吸着等温式を用いることで、特定のガスを選択的に吸着する材料を設計し、二酸化炭素や水素の分離・貯蔵に応用できます。
まとめ
ラングミュア吸着等温式は、固体表面における吸着現象の理解において基本的なツールです。その単純さと広範な応用可能性から、工業プロセスや環境科学、バイオ技術など、さまざまな分野で重要な役割を果たしています。
2.5 ラングミュア吸着等温式の限界と修正モデル
ラングミュア吸着等温式は多くの吸着現象を理解するための基本的なモデルですが、現実の吸着現象にはいくつかの側面で限界があります。このセクションでは、その限界と、それを補うために開発された修正モデルについて説明します。
1. ラングミュア吸着等温式の限界
多層吸着:
ラングミュアのモデルは単分子層吸着を仮定しており、吸着質が1層のみ吸着する場合に適しています。しかし、現実の多くのシステムでは、吸着質が複数層にわたって吸着することがあり、これは多層吸着と呼ばれます。この現象はラングミュアモデルでは説明できません。不均一な表面:
ラングミュアモデルは、吸着媒の表面が均一であり、すべての吸着サイトが同じエネルギーを持つと仮定しています。しかし、現実の固体表面は必ずしも均一ではなく、吸着サイトによって吸着エネルギーが異なることがよくあります。このような場合、ラングミュア等温式は適用が難しくなります。
吸着質間の相互作用:
ラングミュアの仮定では、吸着質分子間には相互作用がないとされています。しかし、現実には吸着質分子同士が引き合ったり、反発したりする場合があります。このような相互作用が無視できない場合、ラングミュア吸着等温式では正確な記述が困難です。
2. 修正モデル
a. BET等温式(Brunauer-Emmett-Teller 等温式)
ラングミュア吸着等温式を多層吸着に対応させたモデルがBET等温式です。これは、特に高圧下での気体の多層吸着に適用されます。BETモデルでは、第一層の吸着後も追加の分子が吸着することを考慮しており、ラングミュアモデルの拡張版ともいえます。
C /(Γ(1 - C/Γ∞)) = 1 /(K_BETΓ∞) + C/Γ∞
ここで、K_BET は多層吸着における平衡定数です。この式は、多層にわたる吸着を扱うため、表面積測定や多層吸着プロセスの分析に使われます。
b. フロイントリッヒ等温式
フロイントリッヒ等温式は、不均一な表面や吸着質間の相互作用を考慮に入れるモデルです。このモデルは経験的で、特に低濃度域での吸着挙動に適しています。次の式で表されます。
Γ =KC^(1/n)
ここで、Kは吸着容量に関する定数、 n は表面の不均一性を表す指数です。この式は、ラングミュア等温式が適用できないシステムにも適用可能です。
3. まとめ
ラングミュア吸着等温式は、特に単分子層吸着を仮定するシステムで有効ですが、多層吸着や不均一な表面などの条件下では適用が難しいです。こうした限界を補うため、BET等温式やフロイントリッヒ等温式といった修正モデルが開発され、より複雑な吸着現象に対応しています。
2.6 ラングミュア吸着等温式の数学的解析
ラングミュア吸着等温式は、吸着現象を定量的に表すための強力なツールです。このセクションでは、ラングミュア吸着等温式の数学的解析について説明します。特に、式の形状やその重要な特性を数学的に理解するための解析手法を紹介します。
1. 式の形状解析
ラングミュア吸着等温式は次のように表されます。
Γ=Γ∞*KC / (1+KC)
ここで
Γ:吸着された吸着質の量
Γ∞:吸着媒が最大限吸着できる吸着サイトの数
C:吸着質の濃度
K:吸着平衡定数
この式は、吸着質の濃度 Cが増加するにつれて、吸着量Γがどのように変化するかを示しています。
低濃度領域での解析
吸着質の濃度 Cが非常に小さい場合(C → 0 )、式は次のように近似できます。
Γ ≒Γ∞KC
この近似式は、低濃度領域において吸着量が濃度に比例することを示しています。したがって、吸着質の濃度が低い場合、ラングミュア等温式は線形な振る舞いを示します。この線形性は、吸着がまだ飽和していない段階を意味します。
高濃度領域での解析
逆に、吸着質の濃度 Cが非常に大きい場合(C → ∞)、式は次のように近似できます。
Γ ≒Γ∞
この式は、吸着量が吸着媒の最大吸着量Γ∞に近づくことを示します。この状況は、すべての吸着サイトが占有され、吸着が飽和している状態です。したがって、吸着質の濃度が十分に高くなると、それ以上の吸着は起こらず、Γは一定になります。
2. 平衡定数Kの役割
平衡定数Kは、吸着質と吸着媒の親和性を表す重要なパラメータです。大きなKは、吸着質が吸着媒に強く吸着することを意味します。数学的に見ると、Kが大きい場合、吸着は低濃度でも急速に進行し、飽和に達するのが早くなります。
一方、Kが小さい場合、吸着が進行するためには高濃度が必要となり、飽和に達するのが遅くなります。
3. グラフでの挙動
ラングミュア吸着等温式のグラフは、典型的にはシグモイド曲線の形状をしています。吸着質の濃度が増えるに従って、吸着量が急激に増加し、その後緩やかになり、最終的に飽和に達します。
低濃度領域: 直線的に増加。
中濃度領域: 急激な増加。
高濃度領域: 飽和に向かって緩やかに増加。
4. 微分による吸着速度の解析
吸着量Γに対する濃度 Cの変化率(吸着速度)を解析するために、ラングミュア吸着等温式の微分を考えます。
dΓdC =Γ∞K(1 +KC)2
この微分式は、吸着速度が吸着質の濃度 Cにどう依存するかを示しています。特に、吸着速度は中濃度領域で最大となり、低濃度および高濃度では遅くなります。
5. 応用
この数学的解析により、実際の吸着現象をより詳細に理解することができます。例えば、産業における触媒反応や、ガスの分離技術、バイオセンサーの設計などで、この解析結果を応用することで、吸着プロセスの最適化が可能です。
2.7 ラングミュア吸着等温式の実験的確認
ラングミュア吸着等温式の正確性を確認するためには、実験的なデータが必要です。このセクションでは、実験によってどのようにラングミュア吸着等温式を検証するか、実験方法や実験データの解析について説明します。
1. 実験の概要
ラングミュア吸着等温式を確認するための典型的な実験は、固体表面に対する気体または溶液中の吸着質の吸着量を測定するものです。実験の主なステップは以下の通りです。
吸着質と吸着媒の選定: 実験では、吸着質として選ばれる物質(例えば気体分子やイオンなど)と、それに対する固体表面である吸着媒が選定されます。例えば、活性炭やシリカゲルのような多孔質材料がよく用いられます。
濃度の調整: 吸着質の濃度を変化させ、さまざまな濃度の下で吸着量を測定します。一般的には、低濃度から高濃度まで段階的に吸着質の濃度を増加させます。
吸着量の測定: 吸着媒に吸着された吸着質の量を測定します。これは、重量変化を測定したり、吸着されなかった気体や溶液中の吸着質濃度の変化を測定したりすることで行います。
2. 実験データの解析
実験データから得られた吸着量と吸着質の濃度の関係を、ラングミュア吸着等温式にフィッティングさせることで、モデルが実験結果をどの程度よく説明できるかを確認します。
ラングミュア吸着等温式に従う場合、以下のようなプロセスでデータ解析が行われます。
直線化: ラングミュア吸着等温式を直線化して解析する方法が一般的です。式を変形して次のようにします。
CΓ = 1KΓ∞ + CΓ∞
この式において、 C/Γ を縦軸に、Cを横軸にプロットすると、実験データが直線になるはずです。この直線の傾きと切片から、平衡定数Kと最大吸着量Γ∞を求めることができます。
パラメータの推定: 実験データに基づいて、吸着平衡定数Kと最大吸着量Γ∞を推定します。これにより、吸着媒の表面特性や吸着質との親和性についての重要な情報が得られます。
3. 実験における注意点
吸着媒の性質: 吸着媒の表面が均一であることが、ラングミュアモデルの前提となります。多孔質材料や不均一な表面を持つ材料では、ラングミュアモデルが正確に適用できない可能性があるため、実験結果を慎重に解析する必要があります。
温度の影響: 吸着は温度に依存するプロセスです。温度が上がると、吸着質の運動エネルギーが増加し、脱着が促進されるため、吸着量が減少する傾向があります。したがって、温度を一定に保つことが重要です。
平衡状態の確認: 吸着と脱着の速度が等しい平衡状態に達していることを確認する必要があります。平衡に達していない状態でデータを取得すると、正確な結果が得られません。
4. 実際のデータ例
ある実験で、気体の窒素 (N₂) がシリカゲルに吸着される過程を観察したとします。濃度 Cと吸着量Γのデータを以下のように得たとします。
| 濃度 C(mol/L) | 吸着量Γ(mol/g) |
| 0.1 | 0.02 |
| 0.2 | 0.035 |
| 0.5 | 0.065 |
| 1.0 | 0.1 |
| 2.0 | 0.14 |
このデータをラングミュア吸着等温式にフィッティングすることで、平衡定数Kと最大吸着量Γ∞を推定します。解析の結果、K= 0.5 L/mol、Γ∞= 0.15 mol/g となった場合、この結果を使ってさらに吸着特性を考察できます。
5. まとめ
実験的に得られた吸着データをラングミュア吸着等温式に当てはめることで、固体表面における吸着現象をモデル化し、吸着平衡定数や吸着容量を推定することができます。このプロセスを通じて、実験結果が理論モデルとどの程度一致するか、そして吸着質と吸着媒の間の相互作用の理解を深めることができます。
2.8 ラングミュア吸着等温式の応用例
ラングミュア吸着等温式は、単分子層吸着現象を記述するための基礎理論として、多くの応用分野で利用されています。このセクションでは、ラングミュア吸着等温式の代表的な応用例について説明します。
1. 触媒反応における応用
触媒表面での反応において、ラングミュア吸着等温式は反応物の吸着過程を記述するために広く使用されます。例えば、ヘテロ触媒反応では、反応物が触媒表面に吸着してから反応が進行します。以下はその典型的な応用例です。
アンモニア合成反応: 窒素と水素が触媒表面に吸着し、そこで反応してアンモニアが生成されます。このプロセスで、ラングミュア吸着等温式を用いることで、反応物の吸着量や反応速度をモデル化できます。
自動車の排気ガス浄化触媒: 排気ガス中の有害物質を除去するための触媒表面での吸着反応が、このモデルで記述できます。たとえば、一酸化炭素(CO)や窒素酸化物(NOx)の吸着と分解反応がラングミュアのモデルで説明されます。
2. ガスの吸着と分離技術
ガスの分離技術において、ラングミュア吸着等温式は、さまざまな気体が吸着媒にどの程度吸着されるかを予測するために用いられます。特に、吸着が重要な分離プロセスにおいて、その予測精度が重要です。
二酸化炭素の分離: 産業プロセスや発電所から排出される二酸化炭素(CO₂)を除去するための吸着技術が開発されています。吸着材として多孔質材料が使用され、CO₂の吸着量をラングミュア吸着等温式でモデル化することで、効率的な分離プロセスを設計できます。
メタンガスの貯蔵: 天然ガスの主要成分であるメタン(CH₄)の貯蔵において、吸着材の性能評価にラングミュア吸着等温式が使用されます。特定の圧力下でメタンがどの程度吸着されるかを予測できるため、安全で効率的な貯蔵技術を開発することが可能です。
3. バイオセンサーにおける応用
ラングミュア吸着等温式は、バイオセンサーにおいても重要な役割を果たします。バイオセンサーは、特定の分子がセンサー表面に吸着することを利用して、その分子の濃度を検出するための装置です。
DNAチップ: DNAチップは、特定のDNA配列がセンサー表面に結合(吸着)することで、その存在を検出します。このプロセスをラングミュア吸着等温式でモデル化することで、検出精度を高めることができます。
抗体-抗原反応センサー: 医療分野で使用される抗体と抗原の結合反応においても、ラングミュア吸着等温式が適用されます。抗体がセンサー表面に固定され、抗原が吸着される過程を解析するためのモデルとして使用されます。
4. 水処理技術
水処理においても、ラングミュア吸着等温式は、吸着による有害物質の除去プロセスを記述するために使用されます。以下のような技術での応用が見られます。
重金属イオンの除去: 水中の鉛やカドミウムなどの重金属イオンを、吸着材を使って除去するプロセスがラングミュア吸着等温式で説明されます。このモデルを用いることで、吸着材の性能を評価し、最適な吸着材の選定が可能です。
有機汚染物質の除去: 水中の有機化合物や薬物汚染物質を吸着材で除去する際にも、このモデルが適用されます。ラングミュア吸着等温式を用いることで、汚染物質の吸着効率を高めるための条件を設定することができます。
5. バイオロジカルプロセスでの応用
生物学的な現象にもラングミュア吸着等温式は適用されます。特に、タンパク質や酵素が表面に吸着する現象をモデル化するために使用されます。
酵素吸着: 固定化酵素の技術において、酵素が固体表面にどのように吸着されるかを理解するために、ラングミュア吸着等温式が役立ちます。酵素の吸着量と基質濃度の関係を定量的に把握できます。
細胞吸着: 生体材料に対する細胞の吸着プロセスにも、この等温式が応用されます。例えば、再生医療や組織工学において、細胞がどの程度材料表面に付着するかを解析するために使われます。
ラングミュア吸着等温式の応用範囲は広く、科学技術の多くの分野で重要な役割を果たしています。これらの応用例を通して、単分子層吸着の基礎理論が、実際の問題解決にどのように貢献しているかが明らかになります。
これでラングミュア吸着等温式に関する概論は終了します。
ラングミュア吸着等温式の総括
ラングミュア吸着等温式は、単分子層吸着現象をモデル化するための基礎理論であり、物理化学の分野で広く利用されています。この理論は、固体表面における吸着と脱着のバランスを数式化し、吸着過程を平衡定数や最大吸着量を通じて定量的に説明します。
背景と基礎理論
ラングミュア吸着等温式は、吸着が単一層で行われ、すべての吸着サイトが均一であるという理想条件に基づいています。これにより、吸着平衡定数Kや最大吸着量Γ∞を用いて、吸着質の濃度と吸着量の関係を表すことができます。基礎的な方程式は次の通りです:
Γ =Γ∞*KC/(1+KC)
ここで、吸着質の濃度 C、最大吸着量Γ∞ 、および平衡定数Kが相互に関係しています。この等温式は、吸着と脱着の速度が平衡に達するという前提の下で導かれました。
実験的検証と解析
ラングミュア吸着等温式の妥当性を確認するためには、吸着実験によるデータの収集が重要です。実験的に得られた吸着量と吸着質の濃度のデータは、ラングミュアモデルにフィッティングさせ、直線化手法などを用いて吸着平衡定数や最大吸着量を推定します。これにより、吸着プロセスの性質や、吸着材と吸着質の親和性を解析することができます。
応用例
ラングミュア吸着等温式は、多くの応用分野で実用されています。特に、触媒反応やガスの分離技術、水処理、バイオセンサーなど、多様なプロセスにおける吸着現象をモデル化し、効率的な設計や性能の最適化に利用されています。例えば、排気ガスの浄化や二酸化炭素の分離技術では、吸着の特性を正確にモデル化することで、実際のプロセスにおける効果を高めることが可能です。また、生物学的現象にも応用され、酵素や細胞の吸着現象の解析にも利用されています。
まとめ
ラングミュア吸着等温式は、物理化学の理論と実験が密接に結びついたモデルであり、科学技術における多くの分野でその重要性が増しています。単分子層吸着という理想的な前提の下で、実際の吸着現象を理解し、応用するための基本的な理論を提供します。特に吸着平衡の理解や、実験データをもとにした理論の実証が、産業や環境技術において価値ある成果をもたらしています。
必須問題【物理】の解説はこちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 必須問題 物理 第106回-第109回 全20問 powered by Gemini 1.5 Pro, Google AI Studio & GPT4, Copilo|matsunoya (note.com)
薬学理論問題【物理】(1) の解説はこちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 薬学理論問題 物理(1)・化学(1) 第106回-第109回 30問 powered by Gemini 1.5 Pro, Google AI Studio & GP|matsunoya (note.com)
お疲れ様でした。
🍰☕🍊
では、問題を解いてみましょう!
すっきり、はっきりわかったら、合格です。
第106回薬剤師国家試験|薬学理論問題 /
問100
一般問題(薬学理論問題)【物理】
問106-100
Q. 以下の図と文章は、化学吸着における単分子層形成を表すラングミュアの吸着等温式(式1)の誘導についてのものである。文章中の[ア]及び[イ]にあてはまる式の正しい組合せはどれか。1つ選べ。

Γ=Γ∞*KC/(1+KC) ・・・式1
吸着質の濃度をC、吸着媒の吸着サイトの全数をΓ∞、吸着質が占有している吸着サイトの数をΓとする。
上図では、Γ∞=10、C=5の場合を示す。
吸着媒に対する吸着質の吸着過程の速度定数をk1、脱着過程の速度定数をk-1とし、吸着平衡が成立していれば、吸着速度と脱着速度は等しいから、[ア]の関係が成り立つ。[ア]を変形すると、式1が得られる。
ただし、K= [イ]であり、この値は吸着質と吸着媒の親和性を表し、大きいほど親和性が高い。
ア|イ
選択肢|
1. k1C = k-1Γ|k1 / k-1
2. k1C = k-1Γ|k-1 / k1
3. k1C = k-1(Γ∞ - Γ)|k1 / k-1
4. k1C = k-1(Γ∞ - Γ)|k-1 / k1
5. k1C(Γ∞ - Γ) = k-1Γ|k-1 / k1
6. k1C(Γ∞ - Γ) = k-1Γ|k1 / k-1
楽しく!驚くほど効率的に。
https://note.com/matsunoya_note
お疲れ様でした。
🍰☕🍊
またのご利用をお待ちしております。
ご意見ご感想などお寄せくださると励みになりうれしいです。
note からのサポート、感謝します。
今日はこの辺で、
それではまた
お会いしましょう。
Your best friend
Mats & BLNt
このコンテンツ
松廼屋|論点解説 薬剤師国家試験対策ノート問106-100【物理】論点:吸着・脱着 / ラングミュアの吸着等温式|matsunoya (note.com)
Here; https://note.com/matsunoya_note/n/ncf1cf2b5f59f
よろしければこちらもどうぞ
このコンテンツの制作者|
滝沢幸穂(Yukiho.Takizawa)phD
■Facebook プロフィール
https://www.facebook.com/Yukiho.Takizawa
■X (Former Twitter) プロフィール 🔒
https://twitter.com/YukihoTakizawa
CONTACT|
mail: info_01.matsunoya@vesta.ocn.ne.jp (Matsunoya Client Support)
tel: 029-872-9676
日々の更新情報など、Twitter @Mats_blnt_pharm から発信しています!
🔒 🐤💕 https://twitter.com/Mats_blnt_pharm
https://note.com/matsunoya_note
note.com 右上の🔍で
( matsunoya_note 🔍 )
松廼屋 Mats.theBASE
https://matsunoya.thebase.in/
サポート感謝します👍
最後までお読みいただきましてありがとうございました。
Here; https://note.com/matsunoya_note/n/ncf1cf2b5f59f
松廼屋|論点解説 薬剤師国家試験対策ノート問106-100【物理】論点:吸着・脱着 / ラングミュアの吸着等温式|matsunoya (note.com)
ここから先は
¥ 1,000
医療、健康分野のリカレント教育における「最強コンテンツ」を note で誰でもいつでも学習できる、 https://note.com/matsunoya_note はそんな場にしたい。あなたのサポートがあれば、それは可能です。サポート感謝します!松廼屋 matsunoya
