
松廼屋|論点解説 薬剤師国家試験対策ノート問109-115【生物】論点:酵素反応 / 速度論的解析 / ミカエリス・メンテン式
第109回薬剤師国家試験|薬学理論問題 /
問115
一般問題(薬学理論問題)【生物】
問109-115
Q. ペニシリン耐性の黄色ブドウ球菌が発現するβ-ラクタマーゼを精製し、反応速度論的解析を行った。β-ラクタマーゼの反応は以下のミカエリス・メンテン式に従うものとする。
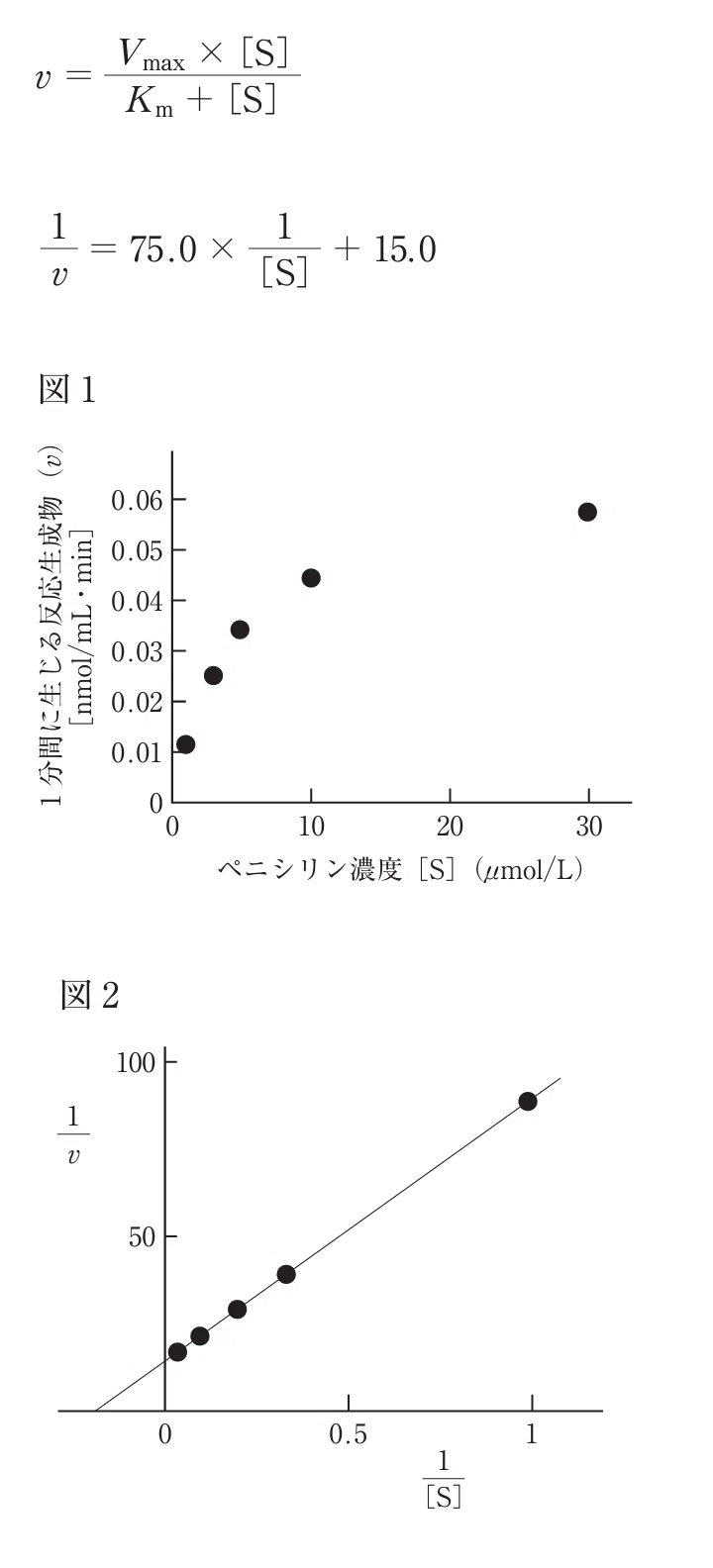
v=Vmax×[S]/(Km+[S])
異なる濃度のペニシリンを含む10mLの反応液中に1ngのβ-ラクタマーゼを加え、反応生成物の量を測定したところ、ペニシリン濃度([S])と1分間に生じる反応生成物の量(v)の関係は図1のようになった。また、ペニシリン濃度の逆数(1/[S])と1分間に生じた反応生成物量の逆数(1/v)をプロットしたところ、図2のようになり、回帰直線の式は1/v=75.0×1/[S]+15.0であった。
以下の記述のうち、正しいのはどれか。2つ選べ。なお、測定中のペニシリン濃度の低下は無視できるものとする。
図1: 縦軸は、1 分間に生じる反応生成物(v)[nmol/mL・min]、横軸は、ペニシリン濃度[S](μmol/L)
図2: 縦軸は、1/v、横軸は、1/[S]
選択肢|
1. β-ラクタマーゼは、酸化還元酵素である。
2. 反応液中のβ-ラクタマーゼを2ngにしても、単位時間あたりの反応生成物量は変わらない。
3. この酵素のVmaxの値は0.067nmol/mL・min(有効数字2桁)である。
4. この反応系に競合阻害薬を加えて実験した場合、見かけ上のKmは5.0nmol/Lより大きくなる。
5. この反応系に非競合阻害薬を加えて実験した場合、図2の回帰直線の傾きは小さくなる。
こんにちは!薬学生の皆さん。
Mats & BLNtです。
matsunoya_note から、薬剤師国家試験の論点解説をお届けします。
苦手意識がある人も、この機会に、薬学理論問題【生物】を一緒に完全攻略しよう!
今回は、第109回薬剤師国家試験|薬学理論問題 / 問115、論点:酵素反応 / 速度論的解析 / ミカエリス・メンテン式を徹底解説します。
薬剤師国家試験対策ノート NOTE ver.
matsunoya_note|note https://note.com/matsunoya_note
Here; https://note.com/matsunoya_note/n/n1dfaf4e538e8
松廼屋|論点解説 薬剤師国家試験対策ノート問109-115【生物】論点:酵素反応 / 速度論的解析 / ミカエリス・メンテン式
薬剤師国家試験対策には、松廼屋の eラーニング
「薬剤師国家試験対策ノート」
マガジン|薬剤師国家試験対策ノート on note
👉マガジンをお気に入りに登録しよう!
このコンテンツの制作者|
滝沢 幸穂 Yukiho Takizawa, PhD
https://www.facebook.com/Yukiho.Takizawa
お友達や知り合いに、matsunota_note で学習したeラーニングを勧めてみたい方は、いいね!、口コミ、おススメなど、よろしくお願いします!
設問へのアプローチ|

第109回薬剤師国家試験の問115(問109-115)では、酵素反応 / 速度論的解析 / ミカエリス・メンテン式に関する知識を問われました。
図が2つ入っている問題ですが、必ずしも図の読解は必要なく、選択肢の文脈から考えると、問題を解くために必要な情報は、回帰式(Lineweaver–Burk plot)の理解と、その切片および傾きから、KmおよびびVmaxの計算式を導くことだけです。

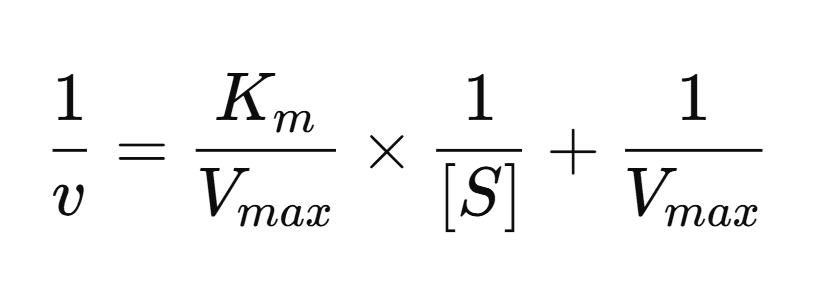

第109回薬剤師国家試験 一般問題|薬学理論問題【生物】 問115
それでは、論点を整理しておきましょう。
今回、Grok 2 mini (beta)にお願いして、論点をまとめてもらいました。
完全攻略を目指せ!
■■Grok 2 mini (beta)
総合的な論点
この問題は、酵素反応の速度論を扱っています。具体的には、β-ラクタマーゼによるペニシリンの加水分解反応の速度に関してミカエリス・メンテン式を用いて解析しています。
ミカエリス・メンテン式:
酵素反応の速度 v は、最大速度 Vmax、基質濃度 [S]、そしてミカエリス定数 Km に依存します。この式は、酵素の反応速度がどのように基質濃度の変化に応答するかを示します。

第109回薬剤師国家試験 一般問題|薬学理論問題【生物】 問115
図1の解析:
ここでは、ペニシリンの濃度を変化させて反応速度を測定しています。
反応速度が基質濃度にどのように依存するかを視覚的に示しており、基質濃度が増えると反応速度も増加するが、一定の濃度以上では飽和することを示唆しています。

図2のリニアリゼーション:
図1のデータをリニアリゼーション(Lineweaver–Burk plot)することで、ミカエリス・メンテン式のパラメータを簡単に求めることができます。ここでは、1/v vs. 1/[S] をプロットし、得られた回帰直線から Km と Vmax を計算します。

回帰直線の式からパラメータの求め方:
直線の式 1/v = 75.0 × 1/[S] + 15.0 から、切片は 1/Vmax、傾きは Km/Vmax であることが分かります。
したがって、切片15.0から Vmax を求め、傾き75.0を使って Km を求めることができます。

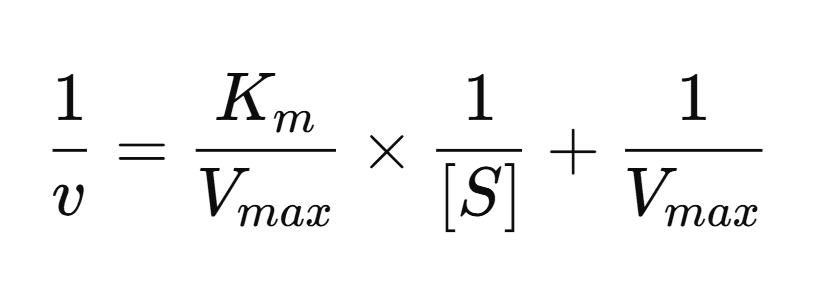
この分析を通じて、β-ラクタマーゼの反応特性を定量的に理解し、特に阻害剤の影響を考慮する際にどのような変化が予測されるかを評価することが目的です。
各選択肢の論点および解法へのアプローチ方法
選択肢1: β-ラクタマーゼは、酸化還元酵素である。
論点:
ここで問われているのはβ-ラクタマーゼの酵素としての分類です。
β-ラクタマーゼはβ-ラクタム環を持つ抗生物質を加水分解する酵素であり、その反応機構が酸化還元反応であるかどうかが問題となります。アプローチ:
β-ラクタマーゼの反応機構を確認します。β-ラクタマーゼはβ-ラクタム環を加水分解します。
この加水分解反応は、酸化還元反応を伴わないため、酸化還元酵素には分類されません。
この選択肢の正誤を判断するには、β-ラクタマーゼの反応機構を理解する必要があります。
選択肢2: 反応液中のβ-ラクタマーゼを2ngにしても、単位時間あたりの反応生成物量は変わらない。
論点:
この選択肢は、酵素の濃度が反応速度に与える影響を問っています。アプローチ:
酵素反応は酵素の濃度に比例します。
ミカエリス・メンテン式では基質濃度が一定の場合、酵素濃度の増加は反応速度を増加させます。
1ngから2ngに酵素量を倍増させた場合の影響を評価する必要があります。
酵素の濃度が低い範囲では、反応速度は酵素濃度に比例します。
他方、Vmaxの条件下では酵素濃度の増加は反応速度に影響を与えません。
ここでは、与えられた条件から、酵素の濃度が反応速度に与える効果を評価する必要があります。
選択肢3: この酵素のVmaxの値は0.067nmol/mL・min(有効数字2桁)である。
論点:
この選択肢は、β-ラクタマーゼの最大反応速度 Vmax の値を求める計算問題です。アプローチ:
図2の回帰直線式 1/v = 75.0 × 1/[S] + 15.0 から、切片 15.0 = 1/Vmax。
ここで Vmax を求めるには、切片を逆数にします。Vmax = 1/15.0。
これを計算すると、0.0666... となり、2桁の有効数字で表すと 0.067 となります。

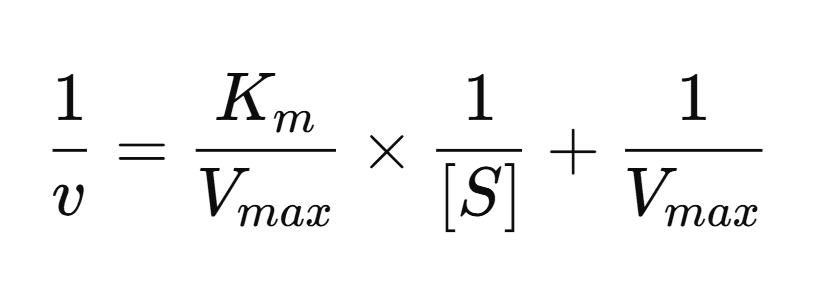
選択肢4: この反応系に競合阻害薬を加えて実験した場合、見かけ上のKmは5.0nmol/Lより大きくなる。
論点:
競合阻害薬の作用とそれがミカエリス定数 Km に与える影響を問っています。アプローチ:
競合阻害薬は酵素の活性部位と基質が競合して結合し、結果として見かけ上の Km を大きくします。
これは、競合阻害薬が存在する場合、実際の基質濃度より高い濃度が必要になるためです。
ただし、ここで注意すべきは、問題文に元の Km の値が明示されていない点です。選択肢の文脈から、競合阻害薬の影響を理解し、一般的な酵素反応の阻害理論に基づいて考察する必要があります。

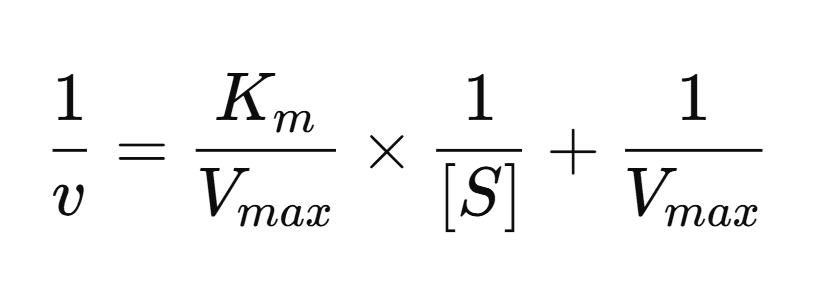
選択肢5: この反応系に非競合阻害薬を加えて実験した場合、図2の回帰直線の傾きは小さくなる。
論点:
非競合阻害薬の作用が反応速度論に与える影響、特にLineweaver–Burk plotにおける変化の理解を問うています。アプローチ:
非競合阻害薬は酵素の活性部位とは異なる部位に結合し、酵素の最大速度 Vmax を減少させます。Lineweaver–Burk plotでは、これは切片の増加(つまり、1/vの切片が大きくなる)として現れます。
傾き Km/Vmax は Vmax の減少により大きくなります。一方で、Kmは変化しないため、プロットの傾きは、Vmax が減少するため、理論上は傾きが大きくなると考えられます。
ここでは、非競合阻害の理論を適用し、プロットの変化を予測する必要があります。
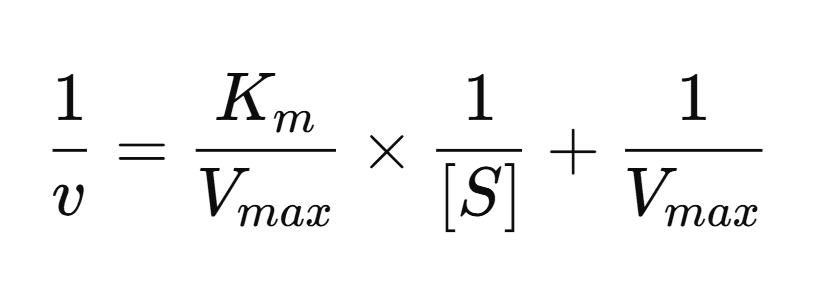

楽勝です!
はじめましょう。
薬剤師国家試験の薬学理論問題【生物】から酵素反応 / 速度論的解析 / ミカエリス・メンテン式を論点とした問題です。
なお、以下の解説は、著者(Yukiho Takizawa, PhD)がプロンプトを作成して、その対話に応答する形でGPT4o & Copilot 、Gemini 1.5 Pro、またはGrok 2 (beta) が出力した文章であって、著者がすべての出力を校閲しています。
生成AIの製造元がはっきりと宣言しているように、生成AIは、その自然言語能力および取得している情報の現在の限界やプラットフォーム上のインターフェースのレイト制限などに起因して、間違った文章を作成してしまう場合があります。
疑問点に関しては、必要に応じて、ご自身でご確認をするようにしてください。
松廼屋|論点解説 薬剤師国家試験対策ノート問109-115【生物】論点:酵素反応 / 速度論的解析 / ミカエリス・メンテン式|matsunoya (note.com)
Here we go.
第109回薬剤師国家試験|薬学理論問題 /
問115
一般問題(薬学理論問題)【生物】
問109-115
Q. ペニシリン耐性の黄色ブドウ球菌が発現するβ-ラクタマーゼを精製し、反応速度論的解析を行った。β-ラクタマーゼの反応は以下のミカエリス・メンテン式に従うものとする。
v=Vmax×[S]/(Km+[S])
異なる濃度のペニシリンを含む10mLの反応液中に1ngのβ-ラクタマーゼを加え、反応生成物の量を測定したところ、ペニシリン濃度([S])と1分間に生じる反応生成物の量(v)の関係は図1のようになった。また、ペニシリン濃度の逆数(1/[S])と1分間に生じた反応生成物量の逆数(1/v)をプロットしたところ、図2のようになり、回帰直線の式は1/v=75.0×1/[S]+15.0であった。
以下の記述のうち、正しいのはどれか。2つ選べ。なお、測定中のペニシリン濃度の低下は無視できるものとする。
図1: 縦軸は、1 分間に生じる反応生成物(v)[nmol/mL・min]、横軸は、ペニシリン濃度[S](μmol/L)
図2: 縦軸は、1/v、横軸は、1/[S]

選択肢|
1. β-ラクタマーゼは、酸化還元酵素である。
2. 反応液中のβ-ラクタマーゼを2ngにしても、単位時間あたりの反応生成物量は変わらない。
3. この酵素のVmaxの値は0.067nmol/mL・min(有効数字2桁)である。
4. この反応系に競合阻害薬を加えて実験した場合、見かけ上のKmは5.0nmol/Lより大きくなる。
5. この反応系に非競合阻害薬を加えて実験した場合、図2の回帰直線の傾きは小さくなる。
■■Grok 2 mini (beta)
生物|問 109-115
■論点|酵素反応 / 速度論的解析 / ミカエリス・メンテン式
この問題の論点は、酵素反応における、β-ラクタマーゼの反応特性をミカエリス・メンテン式を用いて定量的に評価し、競合阻害薬と非競合阻害薬が反応速度論に与える影響を理解することです。
■解説1|
選択肢3:
この酵素のVmaxの値は0.067nmol/mL・min(有効数字2桁)である。[正しい]
問題文にあった回帰直線の式 1/v = 75.0 × 1/[S] + 15.0 の切片 15.0 = 1/Vmax 。
したがって、Vmax = 1/15.0 = 0.0666...、
2桁の有効数字で表すと 0.067 となります。
選択肢4:
この反応系に競合阻害薬を加えて実験した場合、見かけ上のKmは5.0nmol/Lより大きくなる。[正しい]
競合阻害薬は基質と酵素の活性部位で競合するため、見かけ上の Km が大きくなります。
これは、基質が酵素に結合するのが困難になるため、より高い基質濃度が必要になること起因します。
回帰直線の式 から Km を求めます。
1/v = 75.0 × 1/[S] + 15.0
切片 1/Vmax = 15.0
従って、Vmax = 1/15.0 = 0.0666... ≒ 0.067 nmol/mL・min。傾き Km/Vmax = 75.0
ここで、Km を求めるために、Km = 傾き × Vmax を使用します。
Km = 75.0 × 0.0666... ≒ 75.0 × 0.067
Km ≒ 5.025 nmol/L
したがって、Km の値は約 5.0 nmol/L となります。
■解説2|
選択肢3:
この酵素のVmaxの値は0.067nmol/mL・min(有効数字2桁)である。[正しい]
回帰直線の切片 15.0 = 1/Vmax
これを元に Vmax を計算しました。
選択肢4:
この反応系に競合阻害薬を加えて実験した場合、見かけ上のKmは5.0nmol/Lより大きくなる。[正しい]
競合阻害薬の存在下では、酵素の活性部位で基質と阻害薬が競争するため、基質が酵素に結合する確率が下がります。
この現象は、ミカエリス定数 Km が見かけ上大きくなることとして現れます。
元の Km が 5.0 nmol/L であるので、競合阻害薬が加わった場合、この値は 5.0 nmol/L よりも増加します。
■結論|
選択肢3と選択肢4が正しいと結論付けられます。
選択肢3では、提供されたデータと計算からβ-ラクタマーゼの Vmax の値を正確に求めました。
選択肢4では、競合阻害薬の作用が酵素反応の速度論に与える影響を正しく理解しています。
■補足|
選択肢1:
β-ラクタマーゼは、酸化還元酵素である。[誤り]
β-ラクタマーゼはβ-ラクタム環を持つ抗生物質を加水分解する酵素です。
酸化還元反応を伴わないため、酸化還元酵素には分類されません。
β-ラクタマーゼの反応は、ヒドロラーゼに属し、化学的にβ-ラクタム環の加水分解を触媒化します。
選択肢2:
反応液中のβ-ラクタマーゼを2ngにしても、単位時間あたりの反応生成物量は変わらない。[誤り]
酵素の濃度が増加すれば、反応速度も比例して増加します。
酵素量を1ngから2ngに増加させれば、反応速度は2倍になります。
ただし、酵素反応が飽和状態に達していない場合に限ります。酵素の濃度が非常に高い場合、あるいは基質濃度が飽和した場合には、反応速度は一定に近づきます。
酵素反応が飽和状態に達していない範囲では2倍の酵素量は2倍の反応速度を引き起こします。
選択肢5:
この反応系に非競合阻害薬を加えて実験した場合、図2の回帰直線の傾きは小さくなる。[誤り]
非競合阻害薬の添加は、最大反応速度 Vmax を減少させます。
Lineweaver–Burk plotでは、切片(1/v軸との交点; 1/Vmax)が大きくなります。
他方、傾き(Km/Vmax) は変わらないか、理論上は Vmax が減少するので、傾きは大きくなることがあります。
したがって、選択肢の「小さくなる」は正しくありません。
■Lecture
論点解説 酵素反応 / 速度論的解析 / ミカエリス・メンテン式
■■Grok 2 mini (beta)
選択肢1:
β-ラクタマーゼは、酸化還元酵素である。[誤り]
深掘り
β-ラクタマーゼは加水分解酵素であり、β-ラクタム環を持つ抗生物質を加水分解することでその作用を無効化します。
この反応は、酸化還元反応を伴わないため、酸化還元酵素には分類されません。
酸化還元酵素は、基質を酸化または還元する反応を触媒化する酵素で、電子の移動が伴います。
酸化還元酵素の例:
デヒドロゲナーゼ (Dehydrogenases):
これらの酵素は、基質から水素を除去し、NAD+/NADHやFAD/FADH2などの補酵素に還元します。
例えば、乳酸デヒドロゲナーゼは乳酸をピルビン酸に変換します。
オキシダーゼ (Oxidases):
酸素を用いて基質を酸化する酵素です。
例えば、シトクロムcオキシダーゼは電子伝達鎖の最終的な酸化剤として機能し、酸素を水に変換します。
レダクターゼ (Reductases):
これらは基質を還元する酵素です。
例えば、NADPH-シトクロムP450レダクターゼは、シトクロムP450酵素系での還元反応を触媒化します。
カタラーゼ (Catalases):
過酸化水素を分解して水と酸素に変換する酵素です。
酵素の分類は、酵素委員会(EC)によって体系化されており、酵素はその触媒する反応の種類に基づいて分類されます。
酸化還元酵素は主にEC 1に分類され、さらに細かく分かれます。
EC 1.1 - シトクロムを介さないアルコールデヒドロゲナーゼ
EC 1.2 - アルデヒドまたはオキソ酸デヒドロゲナーゼ
EC 1.3 - シトクロムを介するデヒドロゲナーゼ
EC 1.4 - 塩酸化デヒドロゲナーゼ
EC 1.5 - シトクロムを介さないシトクロムデヒドロゲナーゼ
EC 1.6 - シトクロムを介するNADHデヒドロゲナーゼ
EC 1.7 - 酸素をオキシダントとする酸化酵素
EC 1.8 - 硫黄を酸化する酸化酵素
β-ラクタマーゼはEC 3.5.2.6に分類され、加水分解酵素(ヒドロラーゼ)に属します。
Ref.
酵素の体系的な分類と命名に関する文献として、"Enzyme Nomenclature"(国際生化学会と国際酵素連合による)や、関連する生物化学教科書(例えば、Nelson DL, Cox MM. "Lehninger Principles of Biochemistry")を参照してください。
このように、β-ラクタマーゼは加水分解反応を触媒化するため、酸化還元酵素には分類されません。
選択肢2:
反応液中のβ-ラクタマーゼを2ngにしても、単位時間あたりの反応生成物量は変わらない。[誤り]
深掘り
この選択肢は、酵素の量が反応速度に与える影響を問うています。
酵素反応速度論では、反応速度 v は酵素濃度 [E] に対して一次比例します。
考察:
ミカエリス・メンテン式:
v = Vmax × [S] / (Km + [S])ここで、酵素量が2倍になった場合、仮定として Vmax が2倍になると考えます。なぜなら、Vmax は酵素の最大反応速度を表し、酵素の総量に比例します。
酵素量が2倍の場合の反応速度:
もし E0 が元の酵素量で、その場合の Vmax を Vmax,1 とし、酵素量を2倍にした場合の Vmax を Vmax,2 とすると、
Vmax,2 = 2 × Vmax,1これをミカエリス・メンテン式に代入すると、
v2 = 2 × Vmax,1 × [S] / (Km + [S])
反応速度の比較:
元の酵素量 E0 での速度 v1 は
v1 = Vmax,1 × [S] / (Km + [S])2倍の酵素量での速度 v2 は
v2 = 2 × Vmax,1 × [S] / (Km + [S])これを比較すると、
v2 = 2 × v1
したがって、酵素量が2倍になれば、反応速度も2倍になることが分かります。
ただし、ここで重要なのは、反応が飽和状態に達していないことです。
もし基質濃度が非常に高く、反応がすでに Vmax に近ければ、酵素量の増加による反応速度の増加は限定的になります。
問題文ではそうした条件が与えられていません。
反応が飽和状態に達していない範囲では酵素量の増加は反応速度の比例増加を引き起こします。
Ref.
酵素反応速度論に関する基本的な文献として、"Enzyme Kinetics: Behavior and Analysis of Rapid Equilibrium and Steady-State Enzyme Systems" by Irwin H. Segelを参照してください。
このように、β-ラクタマーゼの量が2倍になった場合、反応速度は理論上2倍になると考察できます。
選択肢4:
この反応系に競合阻害薬を加えて実験した場合、見かけ上のKmは5.0nmol/Lより大きくなる。[正しい]
深掘り
競合阻害薬は、基質と同じ活性部位に結合するため、基質が酵素に結合する確率を減少させます。これにより、ミカエリス定数 Km の見かけ上の値が大きくなることが特徴です。
Kmの定義と競合阻害の影響:
Kmの定義: Km は、半分の最大速度 Vmax/2 で達成される基質濃度を示し、酵素が基質と結合する親和性の指標です。競合阻害薬の存在下では、酵素への基質の結合が困難になるため、より高い基質濃度が必要となり、これが見かけ上の Km の増加として現れます。
式を用いた解説:
ミカエリス・メンテン式の競合阻害の場合、以下のように修正されます:
v = Vmax × [S] / (Km (1 + [I] / Ki) + [S])
ここで、
[I] は競合阻害薬の濃度、
Ki は競合阻害薬の抑制定数(阻害薬の親和性を示す)。
この式から、競合阻害薬の存在下では、見かけ上の Km 値が以下のように修正されます:
Km,app = Km (1 + [I] / Ki)
ここで、Km,app は見かけ上のミカエリス定数を表します。
従って、競合阻害薬の濃度 [I] が増加するにつれて、Km,app も増加します。
Ref.
競合阻害に関する詳細な理論と実践的な解析については、"Enzyme Kinetics: Behavior and Analysis of Rapid Equilibrium and Steady-State Enzyme Systems" by Irwin H. Segel、および"Fundamentals of Enzyme Kinetics" by Athel Cornish-Bowdenを参照してください。
このように、競合阻害薬の存在は見かけ上の Km を大きくし、酵素の基質に対する親和性が低下したように見せかけますが、実際には酵素の最大反応速度 Vmax は変わりません。
選択肢5:
この反応系に非競合阻害薬を加えて実験した場合、図2の回帰直線の傾きは小さくなる。[誤り]
深掘り
非競合阻害薬は、酵素の活性部位とは異なる部位に結合し、酵素の構造を変化させたり、酵素-基質複合体の形成を阻害したりすることで、最大反応速度 Vmax を減少させますが、ミカエリス定数 Km には影響を与えません。
KmとVmaxの定義:
Km:
半分の最大速度 Vmax/2 で達成される基質濃度を示し、酵素と基質の親和性を表します。Vmax:
酵素が飽和状態で示す最大の反応速度を表し、酵素の総量に比例します。
非競合阻害の影響:
非競合阻害の場合、ミカエリス・メンテン式は以下のように修正されます。
v = Vmax × [S] / (Km + [S] (1 + [I] / Ki))
ここで、
[I] は非競合阻害薬の濃度
この式から、非競合阻害薬の存在下では、見かけ上の Vmax が以下のように修正されます:
Vmax,app = Vmax / (1 + [I] / Ki)
ここで、
Vmax,app は見かけ上の最大速度、
[I] は非競合阻害薬の濃度、
しかし、ミカエリス定数 Km 自体は変わらず、
Km,app = Km
となります。
Lineweaver–Burk plotの変化:
Lineweaver–Burk plot(1/v vs. 1/[S])では、切片は 1/Vmax を、傾きは Km/Vmax を示します。
非競合阻害薬の場合、切片が大きくなり(1/Vmax が増加)、傾き Km/Vmax は Vmax の減少により理論上大きくなります。
したがって、選択肢5の「傾きは小さくなる」は正しくありません。
実際には、非競合阻害下での傾きは変わらないか、理論上は Vmax の減少により傾きが大きくなることがあります。
Ref.
非競合阻害に関する詳細な理論と解析については、"Enzyme Kinetics: Behavior and Analysis of Rapid Equilibrium and Steady-State Enzyme Systems" by Irwin H. Segel、および"Fundamentals of Enzyme Kinetics" by Athel Cornish-Bowdenを参照してください。
このように、非競合阻害薬は Vmax を減少させますが、Km に影響を与えません。従って、Lineweaver–Burk plotの傾きは小さくならず、正確には切片が大きくなり、場合によっては傾きが大きくなることがあります。
必須問題の解説はこちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 必須問題 第106回-第109回 一覧 powered by Gemini 1.5 Pro, Google AI Studio & GPT4, Copilot|matsunoya (note.com)
薬学理論問題【生物】(1) の解説はこちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 薬学理論問題 生物(1) 第106回-第109回 19問 powered by Gemini 1.5 Pro, Google AI Studio & GPT4o, C|matsunoya (note.com)
お疲れ様でした。
🍰☕🍊
では、問題を解いてみましょう!
すっきり、はっきりわかったら、合格です。
第109回薬剤師国家試験|薬学理論問題 /
問115
一般問題(薬学理論問題)【生物】
問109-115
Q. ペニシリン耐性の黄色ブドウ球菌が発現するβ-ラクタマーゼを精製し、反応速度論的解析を行った。β-ラクタマーゼの反応は以下のミカエリス・メンテン式に従うものとする。
v=Vmax×[S]/(Km+[S])
異なる濃度のペニシリンを含む10mLの反応液中に1ngのβ-ラクタマーゼを加え、反応生成物の量を測定したところ、ペニシリン濃度([S])と1分間に生じる反応生成物の量(v)の関係は図1のようになった。また、ペニシリン濃度の逆数(1/[S])と1分間に生じた反応生成物量の逆数(1/v)をプロットしたところ、図2のようになり、回帰直線の式は1/v=75.0×1/[S]+15.0であった。
以下の記述のうち、正しいのはどれか。2つ選べ。なお、測定中のペニシリン濃度の低下は無視できるものとする。
図1: 縦軸は、1 分間に生じる反応生成物(v)[nmol/mL・min]、横軸は、ペニシリン濃度[S](μmol/L)
図2: 縦軸は、1/v、横軸は、1/[S]

選択肢|
1. β-ラクタマーゼは、酸化還元酵素である。
2. 反応液中のβ-ラクタマーゼを2ngにしても、単位時間あたりの反応生成物量は変わらない。
3. この酵素のVmaxの値は0.067nmol/mL・min(有効数字2桁)である。
4. この反応系に競合阻害薬を加えて実験した場合、見かけ上のKmは5.0nmol/Lより大きくなる。
5. この反応系に非競合阻害薬を加えて実験した場合、図2の回帰直線の傾きは小さくなる。
楽しく!驚くほど効率的に。
https://note.com/matsunoya_note
お疲れ様でした。
🍰☕🍊
またのご利用をお待ちしております。
ご意見ご感想などお寄せくださると励みになりうれしいです。
note からのサポート、感謝します。
今日はこの辺で、
それではまた
お会いしましょう。
Your best friend
Mats & BLNt
このコンテンツ
松廼屋|論点解説 薬剤師国家試験対策ノート問109-115【生物】論点:酵素反応 / 速度論的解析 / ミカエリス・メンテン式|matsunoya (note.com)
Here; https://note.com/matsunoya_note/n/n1dfaf4e538e8
よろしければこちらもどうぞ
このコンテンツの制作者|
滝沢幸穂(Yukiho.Takizawa)phD
■Facebook プロフィール
https://www.facebook.com/Yukiho.Takizawa
■X (Former Twitter) プロフィール 🔒
https://twitter.com/YukihoTakizawa
CONTACT|
mail: info_01.matsunoya@vesta.ocn.ne.jp (Matsunoya Client Support)
tel: 029-872-9676
日々の更新情報など、Twitter @Mats_blnt_pharm から発信しています!
🔒 🐤💕 https://twitter.com/Mats_blnt_pharm
https://note.com/matsunoya_note
note.com 右上の🔍で
( matsunoya_note 🔍 )
松廼屋 Mats.theBASE
https://matsunoya.thebase.in/
サポート感謝します👍
最後までお読みいただきましてありがとうございました。
Here; https://note.com/matsunoya_note/n/n1dfaf4e538e8
松廼屋|論点解説 薬剤師国家試験対策ノート問109-115【生物】論点:酵素反応 / 速度論的解析 / ミカエリス・メンテン式|matsunoya (note.com)
ここから先は
¥ 700
医療、健康分野のリカレント教育における「最強コンテンツ」を note で誰でもいつでも学習できる、 https://note.com/matsunoya_note はそんな場にしたい。あなたのサポートがあれば、それは可能です。サポート感謝します!松廼屋 matsunoya
