
松廼屋|論点解説 薬剤師国家試験対策ノート問 109-103【化学】論点:アルケンへの付加 / 電子の動き
第109回薬剤師国家試験|薬学理論問題 /
問103
一般問題(薬学理論問題)【物理・化学・生物】
化学|問 109-103
Q. 電子移動を示す矢印で記した機構が主となって、実際に進行し、生成物が得られる反応はどれか。1つ選べ。

電子移動を示す矢印で記した機構
■選択肢
1. 1
2. 2
3. 3
4. 4
5. 5
松廼屋|論点解説 薬剤師国家試験対策ノート問 109-103【化学】論点:アルケンへの付加 / 電子の動き|matsunoya
こんにちは!薬学生の皆さん。
Mats & BLNtです。
matsunoya_note から、薬剤師国家試験の論点解説をお届けします。
苦手意識がある人も、この機会に、薬学理論問題【化学】を一緒に完全攻略しよう!
今回は、第109回薬剤師国家試験|薬学理論問題 / 問103【化学】 、論点:アルケンへの付加 / 電子の動きを徹底解説します。
薬剤師国家試験対策ノート NOTE ver.
matsunoya_note|note https://note.com/matsunoya_note
Here; https://note.com/matsunoya_note/n/n174622a10e2c
松廼屋|論点解説 薬剤師国家試験対策ノート問 109-103【化学】論点:アルケンへの付加 / 電子の動き|matsunoya
薬剤師国家試験対策には、松廼屋の eラーニング
「薬剤師国家試験対策ノート」
マガジン|薬剤師国家試験対策ノート on note
👉マガジンをお気に入りに登録しよう!
このコンテンツの制作者|
滝沢 幸穂 Yukiho Takizawa, PhD
https://www.facebook.com/Yukiho.Takizawa
お友達や知り合いに、matsunota_note で学習したeラーニングを勧めてみたい方は、いいね!、口コミ、おススメなど、よろしくお願いします!
設問へのアプローチ|

第109回薬剤師国家試験の問103【化学】(問109-103)では、化学構造式からアルケンへの付加 / 電子の動きなどが問われました。
電子移動を示す矢印で記した機構については、各反応分類ごとに、自分で何度か書いてみて覚えるしかないです。
各反応分類ごとに、メカニズムに関する記載を読んで、矢印の意味を考えることも大事です。
まず基本的な知識について復習しておきましょう。
■Lecture

1. マルコフニコフ則による HBr の付加反応

Ref. Reaction of Alkenes With HCl, HBr, and HI - Chemistry Steps
2. カルベン付加反応によるシクロプロパン環の形成

Ref. 5: Carbene Reactions - Chemistry LibreTexts
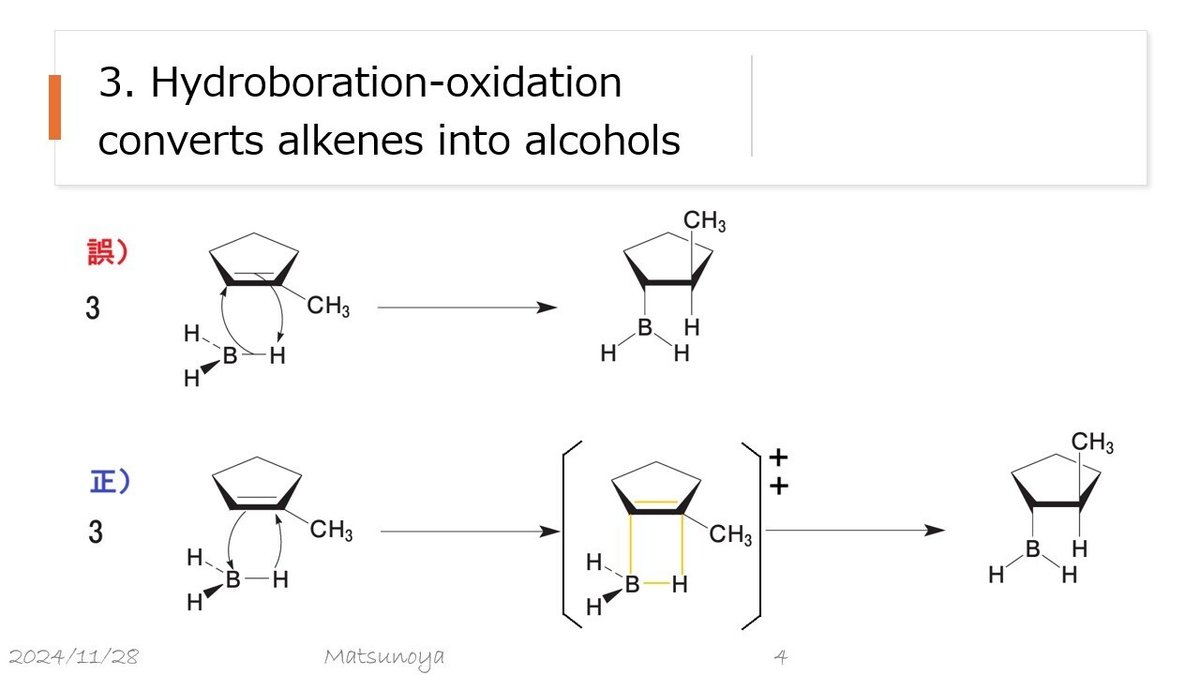
3. ヒドロホウ素化(反マルコフニコフ則の付加反応)

Ref. Hydroboration Oxidation of Alkenes - Chemistry Steps
4. ハロゲン化反応による trans 配置生成

Ref. Halohydrins from Alkenes - Chemistry Steps
5. MCPBA の反応|エポキシ化反応(立体化学の保存)
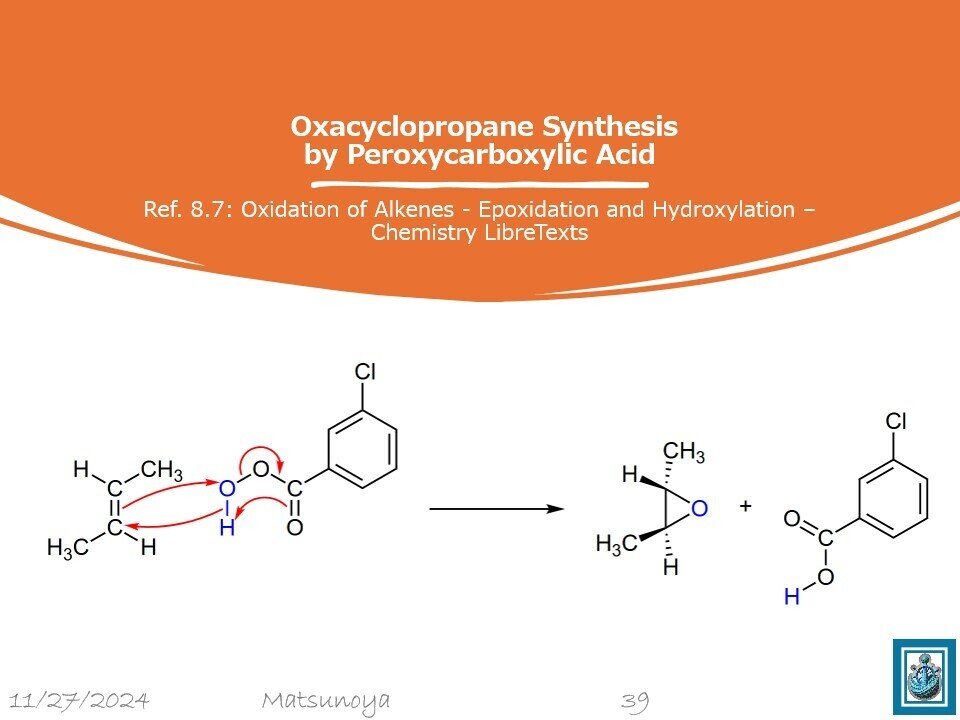
Ref. 8.7: Oxidation of Alkenes - Epoxidation and Hydroxylation - Chemistry LibreTexts
論点およびポイント
■■GPT4o
化学|問 109-103
論点| アルケンへの付加 / 電子の動き
ポイント|
1. イソブテンと臭化水素の反応
マルコフニコフ則による HBr の付加反応
HBr の極性分解
H-Br 結合が分極し、H⁺ と Br⁻ に分かれる。
二重結合が H⁺ を攻撃(π電子 → H⁺)。
カルボカチオン中間体の形成
二重結合の炭素上に第三級カルボカチオンが形成。
求核攻撃
Br⁻ が第三級カルボカチオンを攻撃し、2-メチル-2-ブロモプロパンを生成。
2. シクロヘキセンとジクロロカルベンの反応
カルベン付加反応によるシクロプロパン環の形成
ジクロロカルベンの生成
塩基性条件下で塩素化メタンが分解し、CCl₂ が生成(塩基 → HCl 抽出)。
π電子による攻撃
シクロヘキセンの二重結合のπ電子がカルベンの炭素を攻撃(π電子 → CCl₂)。
同時に CCl₂ の電子がもう一つの炭素に共有され、三員環を形成。
3. 1-メチルシクロペンテンとホウ素水素化物の反応
ヒドロホウ素化(反マルコフニコフ則の付加反応)
BH₃ の付加
BH₃ のホウ素が二重結合の炭素を攻撃(B-H 結合電子 → アルケンの 2 位炭素)。
同時に H⁺ が 1 位炭素に結合(シン付加)。
酸化反応(省略可能)
通常は H₂O₂/NaOH の酸化条件でアルコールが生成される。
4. シクロペンテンと臭素の反応
ハロゲン化反応による trans 配置生成
ブロモニウムイオン中間体の形成
シクロペンテンの二重結合が Br₂ の一つの Br を攻撃(π電子 → Br-Br)。
同時にもう片方の Br が負電荷を帯び、環状のブロモニウムイオン中間体を形成。
Br⁻ の攻撃(抗付加)
Br⁻ がブロモニウムイオンを反対側から攻撃し、trans 配置のジブロモ化合物を形成。
5. trans-2-ブテンと MCPBA の反応
エポキシ化反応(立体化学の保存)
π電子による攻撃
trans-2-ブテンのπ電子が MCPBA の酸素-酸素結合を攻撃(π電子 → O-O 結合)。
過酸の酸素が二重結合の両炭素に結合し、エポキシド環を形成。
副生成物の形成
MCPBA の分解により m-クロロ安息香酸が副生成物として残る。
■Lecture
問109-103 アルケンへの付加|電子の移動







薬剤師国家試験 出題基準
出典: 薬剤師国家試験のページ |厚生労働省 (mhlw.go.jp)
出題基準 000573951.pdf (mhlw.go.jp)
論点を整理します。
■■GPT4o
総合的な論点
この問題の核となる論点は、電子移動を伴う化学反応機構の正確な理解と、それが生成物の形成にどのように寄与するかを特定する能力にあります。反応機構を正しく理解するためには、以下の基本的な化学原理が鍵となります:
電子移動(矢印表記)の意味と方向性:
反応機構における矢印は電子の動きを示し、親電子性(電子不足)と求核性(電子供与性)の相互作用を表します。選択肢の各反応で、矢印が正しく描かれ、実際の反応進行を反映しているかを検討する必要があります。反応特性と反応条件:
反応が正しく進行するには、基質、試薬、環境条件が適切である必要があります。例えば、臭素(Br₂)や MCPBA などの試薬は、特定の環境で特有の反応を進行させます。これにより生成物の構造や立体化学が決まります。生成物の安定性と選択性:
生成物の立体化学(cis/trans 配置)や電子配置が反応の進行方向に影響します。また、反応の選択性(位置選択性や立体選択性)は生成物の構造を特定する際に重要な要因となります。科学的根拠:
各反応は有機化学の確立された知見に基づいています。反応機構が化学的に不可能である場合、あるいは選択性が反映されていない場合、その選択肢は正解とはなり得ません。
問題設定の特徴
この問題では、特定の基質と試薬の組み合わせに基づく反応について、電子移動の矢印で記された反応機構が実際に進行するかどうかを問うています。特に重要なのは、反応の矢印が正確に以下の要素を示しているかどうかです:
反応の進行を決定づける化学種間の相互作用(例:π電子の親電子攻撃)。
中間体の形成およびその役割(例:ブロモニウムイオンやカルベン)。
生成物の立体化学的な特徴(例:抗付加による trans 配置の生成)。


イソブテン(isobutylene)と臭化水素(HBr)の反応は、有機化学において一般的な付加反応の一例です。この反応の詳細を以下に分類、メカニズム、生成物について説明します。
1. 反応の分類
この反応は「電解質付加反応 (electrophilic addition reaction)」に分類されます。イソブテンの二重結合(C=C)が電子の豊富な部位として、臭化水素のH⁺が親電性試薬として反応します。
2. メカニズム
(1) イソブテンの構造と反応中心
イソブテンは分岐アルケンで、中央の炭素-炭素二重結合が反応の主な部位です。この二重結合はπ電子を持ち、電子密度が高いため、陽電荷を持つ親電性分子と反応しやすい特徴があります。
(2) プロトン化 (H⁺の付加)
臭化水素(HBr)が反応に加わると、まずHBrが解離してH⁺とBr⁻に分かれます。H⁺はイソブテンの二重結合に付加し、二重結合が切れて新たな単結合が形成されます。このとき、二次カルボカチオンが生成します(マルコフニコフ則に従い、H⁺は二重結合に結合している炭素のうち、水素がより多い側に付加します)。
中間体: 二次カルボカチオンが生成されます。
(3) ブロミドイオン (Br⁻) の攻撃
生成された二次カルボカチオンは不安定であり、すぐに陰イオンであるブロミドイオン(Br⁻)が求核攻撃を行います。この過程で、生成物が形成されます。
3. 生成物
反応の生成物は tert-ブチルブロミド (tert-Butyl bromide, (CH₃)₃CBr) です。
この化合物は第三級炭素に臭素が結合している構造を持ちます。
生成物の構造:

4. マルコフニコフ則との関連
この反応はマルコフニコフ則(Markovnikov's Rule)に従っています。この規則により、プロトン(H⁺)は二重結合の炭素の中で、すでに水素が多く結合している側に付加します。その結果、より安定なカルボカチオン(ここでは二次カルボカチオン)が生成し、反応が進みます。
5. 文献引用例
以下はこの反応に関連する文献の一例です。ご参考までに。
McMurry, J. "Organic Chemistry." 9th Edition, Brooks Cole, 2015.
Clayden, J., Greeves, N., Warren, S., Wothers, P. "Organic Chemistry." 2nd Edition, Oxford University Press, 2012.

シクロヘキセン(cyclohexene)とジクロロカルベン(dichlorocarbene, CCl₂)の反応は、炭素二重結合に対するカルベンの付加反応の一例です。この反応を以下のように分類し、メカニズムと生成物について説明します。
1. 反応の分類
この反応は「環化付加反応 (cycloaddition reaction)」の一種であり、具体的には二重結合とカルベンの「シクロプロパン環形成反応 (cyclopropanation reaction)」に分類されます。
カルベン(CCl₂)は、反応性の高い中間体であり、炭素原子に2つの結合と2つの非共有電子対を持つ中性分子です。この性質により、π結合と反応して新しい環状構造を形成します。
2. メカニズム
(1) ジクロロカルベンの生成
ジクロロカルベン(CCl₂)は一般に次のような方法で生成されます(試薬例: クロロホルムと強塩基)。
クロロホルム(CHCl₃)が強塩基によって脱プロトン化され、ジクロロカルベンが生成します。
(2) シクロヘキセンへのカルベンの付加
ジクロロカルベンは二重結合(π電子)を求核剤として攻撃し、シクロヘキセンの炭素原子に付加します。この反応は以下の2段階で進行します:
ジクロロカルベンの空のp軌道がシクロヘキセンのπ電子から供給される。
シクロヘキセンの二重結合により、カルベンと三員環(シクロプロパン環)が形成されます。
この反応は一段階で進行する協奏的(concerted)な反応と考えられています。
3. 生成物
生成物は 1,1-ジクロロ-2-シクロプロピルシクロヘキサン です。具体的には、ジクロロカルベンが付加した結果、シクロヘキセンがシクロプロパン環を含む構造に変換されます。
生成物の構造:

4. 反応特性
立体特異性:
この反応は立体特異的であり、二重結合の幾何異性(cis/trans)は生成物に反映されます。シクロヘキセンのcis配座に対応する生成物が得られます。選択性:
ジクロロカルベンは親電子性が高く、電子密度の高いアルケン部位で付加反応を起こします。
5. 文献引用例
以下はこの反応や類似のカルベン付加反応に関連する文献です:
March, J. "Advanced Organic Chemistry: Reactions, Mechanisms, and Structure." 6th Edition, Wiley, 2007.
Carey, F. A., Sundberg, R. J. "Advanced Organic Chemistry, Part A: Structure and Mechanisms." 5th Edition, Springer, 2007.
Vollhardt, K. P. C., Schore, N. E. "Organic Chemistry: Structure and Function." 8th Edition, Macmillan, 2018.

1-メチルシクロペンテン(1-methyl-cyclopentene)とホウ素水素化物(BH₃)の反応は、アルケンの水素化ホウ素化 (hydroboration) に分類される反応です。この反応は、アンチマルコフニコフ則に従い、アルケンに水素とホウ素を付加する過程で進行します。
1. 反応の分類
この反応は「付加反応 (addition reaction)」に分類され、具体的には 水素化ホウ素化/酸化 (hydroboration-oxidation) と呼ばれる2段階の反応です。第一段階でホウ素水素化物(BH₃)がアルケンに付加し、第二段階で過酸化水素 (H₂O₂) と水酸化ナトリウム (NaOH) による酸化が行われます。
2. メカニズム
(1) 水素化ホウ素化(Hydroboration)
ステップ1:
BH₃(ホウ素三水素)は空のp軌道を持つ親電子性分子であり、アルケンのπ電子に反応します。付加の立体特性:
水素(H)はアルケンの炭素原子のうち電子密度が少ない方(1位炭素、マルコフニコフ則の逆)に結合し、ホウ素(B)はより置換された炭素(2位炭素)に結合します。この際、反応は協奏的(concerted)に進行し、遷移状態で水素とホウ素が同じ方向(シン付加)に結合します。生成物:
中間生成物としてホウ素化合物が生成されます。ここでは、アルケン1分子がBH₃と反応し、モノホウ素化生成物(1-メチルシクロペンチルボラン)が得られます。

(2) 酸化(Oxidation)
ステップ2:
過酸化水素 (H₂O₂) と水酸化ナトリウム (NaOH) の水溶液中で酸化が進行します。この過程でホウ素が水酸基(–OH)に変換されます。酸化は立体特異的に進行し、最終的にアルコールが生成されます。
3. 生成物
反応の最終生成物は 1-メチルシクロペンタン-2-オール(1-methylcyclopentan-2-ol) です。この化合物はアンチマルコフニコフ則に従って形成されており、ヒドロキシ基 (–OH) がアルケンのより置換の少ない炭素(1位炭素)に結合しています。
4. 反応特性
立体選択性:
反応は「シン付加」で進行します。水素とホウ素(後に置換される水酸基)は同じ面から付加します。位置選択性:
アンチマルコフニコフ則に従い、ヒドロキシ基はより置換の少ない炭素に結合します。
5. 文献引用例
以下はこの反応に関連する文献です:
Carey, F. A., Sundberg, R. J. Advanced Organic Chemistry, Part B: Reactions and Synthesis. 5th Edition, Springer, 2007.
March, J. Advanced Organic Chemistry: Reactions, Mechanisms, and Structure. 6th Edition, Wiley, 2007.
Clayden, J., Greeves, N., Warren, S., Wothers, P. Organic Chemistry. 2nd Edition, Oxford University Press, 2012.

シクロペンテン(cyclopentene, C₅H₈)と臭素(Br₂)の反応は、アルケンに対する臭素分子の付加反応です。この反応はハロゲン化(halogenation)に分類され、結果として trans-ジブロモシクロペンタン(trans-dibromo-cyclopentane)が生成されます。以下に、反応の分類、メカニズム、生成物について段階的に論述します。
1. 反応の分類
この反応は「ハロゲン化反応 (halogenation reaction)」に分類されます。具体的には、シクロペンテンの二重結合(C=C)が臭素分子と反応し、炭素-炭素間に二つの臭素原子が付加する反応です。反応は抗付加(anti-addition)の特徴を持ち、生成物の立体化学に影響します。
2. メカニズム
(1) 臭素分子の極性誘起
臭素分子(Br₂)は非極性ですが、シクロペンテンの二重結合に近づくと、π電子によって臭素分子の片方の臭素原子に部分的な正電荷(δ⁺)、もう片方に負電荷(δ⁻)が誘起されます。
(2) 臭素カチオン(ブロモニウムイオン)の形成
誘起された極性により、二重結合が親電性中心である臭素原子(δ⁺)を攻撃し、三員環状のブロモニウムイオン(bromonium ion)が形成されます。この中間体では、臭素原子が二つの炭素に結合して正電荷を帯びています。
反応中間体の構造:

(3) ブロミドイオン(Br⁻)の求核攻撃
残った Br⁻(負電荷を帯びた臭素イオン)が環状中間体を求核攻撃します。この攻撃は、ブロモニウムイオンの反対側から起こるため、二つの臭素原子が二重結合の両側に反対方向(trans)に付加されます。
3. 生成物
反応の生成物は trans-ジブロモシクロペンタン(trans-dibromo-cyclopentane) です。この化合物では、シクロペンタン骨格上の隣接する二つの炭素に、それぞれ反対側に位置する臭素原子が結合しています。
生成物の立体化学:

4. 反応特性
立体選択性:
この反応は抗付加(anti-addition)で進行し、生成物は常に trans 配置になります。反応条件:
通常、この反応は二硫化炭素(CS₂)や四塩化炭素(CCl₄)などの非極性溶媒中で行われます。
5. 文献引用例
以下は、この反応に関する詳しい解説が含まれる参考文献です:
McMurry, J. Organic Chemistry. 9th Edition, Cengage Learning, 2015.
Carey, F. A., Sundberg, R. J. Advanced Organic Chemistry, Part A: Structure and Mechanisms. 5th Edition, Springer, 2007.
Solomons, T. W. G., Fryhle, C. B. Organic Chemistry. 11th Edition, Wiley, 2013.

trans-2-ブテン(trans-2-butene)とメタクロロ過酸化安息香酸(meta-chloroperoxybenzoic acid, MCPBA)の反応は、アルケンに対するエポキシ化(epoxidation)の一例です。この反応の詳細を以下に分類、メカニズム、生成物について段階的に説明します。
1. 反応の分類
この反応は「酸化反応 (oxidation reaction)」に分類され、具体的には アルケンのエポキシ化 (epoxidation of alkenes) と呼ばれます。アルケンの炭素-炭素二重結合(C=C)が酸化剤(ここでは MCPBA)によってエポキシド(オキシラン)に変換されます。
2. メカニズム
(1) MCPBAの構造と反応性
MCPBAは過酸(R-CO₃H)の一種であり、酸素-酸素結合が反応性の高い部分です。この部分がアルケンと反応して酸素を供与します。
(2) エポキシ化反応の進行
エポキシ化は単一の遷移状態を経て進行する協奏的(concerted)な反応です。
MCPBAの酸素原子がアルケンのπ電子に攻撃されると同時に、アルケンの炭素-炭素二重結合がMCPBAの酸素-酸素結合を切断します。
この過程でエポキシド(三員環のオキシラン)が形成され、MCPBAは副生成物として m-クロロ安息香酸(meta-chlorobenzoic acid, C₆H₄Cl-COOH)を放出します。
(3) 立体化学の保存
反応は立体特異的であり、出発物質の立体化学が生成物に保存されます。
trans-2-ブテン(基質) → trans-2,3-エポキシブタン(生成物)
反応全体は以下のように進行します:

3. 生成物
反応生成物は trans-2,3-エポキシブタン(trans-2,3-epoxybutane) です。この化合物は三員環のエポキシドであり、二つのメチル基が trans 配置を保持します。
生成物の立体化学:

4. 反応特性
立体特異性:
エポキシ化は基質の立体化学を保持します(cis-アルケンから cis-エポキシド、trans-アルケンから trans-エポキシドが生成)。選択性:
MCPBAはエポキシ化において高い選択性を示します。反応は二重結合の位置に限定され、副反応はほとんど起こりません。環境条件:
反応は通常、非極性または中程度の極性を持つ溶媒(例:ジクロロメタン、CH₂Cl₂)中で行われます。
5. 文献引用例
以下は、この反応に関連する参考文献です:
Clayden, J., Greeves, N., Warren, S., Wothers, P. Organic Chemistry. 2nd Edition, Oxford University Press, 2012.
Carey, F. A., Sundberg, R. J. Advanced Organic Chemistry, Part B: Reactions and Synthesis. 5th Edition, Springer, 2007.
McMurry, J. Organic Chemistry. 9th Edition, Cengage Learning, 2015.
以上で、論点整理を終わります。
理解できたでしょうか?
大丈夫です。
完全攻略を目指せ!
はじめましょう。
薬剤師国家試験の薬学理論問題【化学】からアルケンへの付加 / 電子の動きを論点とした問題です。
なお、以下の解説は、著者(Yukiho Takizawa, PhD)がプロンプトを作成して、その対話に応答する形でGPT4o & Copilot 、Gemini 1.5 Pro、またはGrok 2 (beta) が出力した文章であって、著者がすべての出力を校閲しています。
生成AIの製造元がはっきりと宣言しているように、生成AIは、その自然言語能力および取得している情報の現在の限界やプラットフォーム上のインターフェースのレイト制限などに起因して、間違った文章を作成してしまう場合があります。
疑問点に関しては、必要に応じて、ご自身でご確認をするようにしてください。
Here we go.
第109回薬剤師国家試験|薬学理論問題 /
問103
一般問題(薬学理論問題)【物理・化学・生物】
化学|問 109-103
Q. 電子移動を示す矢印で記した機構が主となって、実際に進行し、生成物が得られる反応はどれか。1つ選べ。

電子移動を示す矢印で記した機構
■選択肢
1. 1
2. 2
3. 3
4. 4
5. 5
■■GPT4o
化学|問 109-102
■論点|アルケンへの付加 / 電子の動き
スライドを参照してください。
■解説1

■解説2
4. ハロゲン化反応による trans 配置生成

Ref. Halohydrins from Alkenes - Chemistry Steps
■結論
選択肢4が正答です。
■補足




基質|試薬|生成物
1. イソブテン(Isobutylene)|臭化水素(Hydrogen Bromide)|2-メチル-2-ブロモプロパン(2-Bromo-2-methylpropane)= tert-ブチルブロミド (tert-Butyl bromide, (CH₃)₃CBr)
2. シクロヘキセン(Cyclohexene)|ジクロロカルベン(Dichlorocarbene、CCl2)|1,1-ジクロロ-2-シクロプロピルシクロヘキサン(1,1-Dichloro-2-cyclopropylcyclohexane)
3. 1-メチル-シクロペンテン(1-methyl-cyclopentene)|ホウ素水素化物(Borane、BH3)|
4. シクロペンテン(Cyclopentene、C₅H₈)|臭素(Bromine、Br2)|trans-ジブロモシクロペンタン(trans-dibromo-cyclopentane)
5. trans-2-ブテン(trans-2-Butene、CH3-HC=CH-CH3)|メタクロロ過酸化安息香酸(meta-chloroperoxybenzoic acid、MCPBA)|trans-2,3-エポキシブタン(trans-2,3-Epoxybutane)
必須問題の解説は、こちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 必須問題 第106回-第109回 一覧 powered by Gemini 1.5 Pro, Google AI Studio & GPT4, Copilot|matsunoya (note.com)
薬学理論問題の解説は、こちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 薬学理論問題 第106回-第109回 一覧 powered by Gemini 1.5 Pro, GPT4o, Copilot, and Grok 2|matsunoya
お疲れ様でした。
🍰☕🍊
では、問題を解いてみましょう!
すっきり、はっきりわかったら、合格です。
第109回薬剤師国家試験|薬学理論問題 /
問103
一般問題(薬学理論問題)【物理・化学・生物】
化学|問 109-103
Q. 電子移動を示す矢印で記した機構が主となって、実際に進行し、生成物が得られる反応はどれか。1つ選べ。

電子移動を示す矢印で記した機構
■選択肢
1. 1
2. 2
3. 3
4. 4
5. 5
楽しく!驚くほど効率的に。
https://note.com/matsunoya_note
お疲れ様でした。
🍰☕🍊
またのご利用をお待ちしております。
ご意見ご感想などお寄せくださると励みになりうれしいです。
note からのサポート、感謝します。
今日はこの辺で、
それではまた
お会いしましょう。
Your best friend
Mats & BLNt
このコンテンツ
松廼屋|論点解説 薬剤師国家試験対策ノート問 109-103【化学】論点:アルケンへの付加 / 電子の動き|matsunoya
Here; https://note.com/matsunoya_note/n/n174622a10e2c
よろしければこちらもどうぞ
薬学理論問題の論点解説 一覧です。
走る!「基本骨格」Twitter Ver.|薬剤師国家試験対策ノート @YouTube
このコンテンツの制作者|
滝沢幸穂(Yukiho.Takizawa)phD
■Facebook プロフィール
https://www.facebook.com/Yukiho.Takizawa
■X (Former Twitter) プロフィール 🔒
https://twitter.com/YukihoTakizawa
CONTACT|
mail: info_01.matsunoya@vesta.ocn.ne.jp (Matsunoya Client Support)
tel: 029-872-9676
日々の更新情報など、Twitter @Mats_blnt_pharm 🔒から発信しています!
🔒🐤💕 https://twitter.com/Mats_blnt_pharm
https://note.com/matsunoya_note
note.com 右上の🔍で
( matsunoya_note 🔍 )
松廼屋 Mats.theBASE
https://matsunoya.thebase.in/
サポート感謝します👍
最後までお読みいただきましてありがとうございました。
Here; https://note.com/matsunoya_note/n/n174622a10e2c
松廼屋|論点解説 薬剤師国家試験対策ノート問 109-103【化学】論点:アルケンへの付加 / 電子の動き|matsunoya
ここから先は
¥ 1,000
医療、健康分野のリカレント教育における「最強コンテンツ」を note で誰でもいつでも学習できる、 https://note.com/matsunoya_note はそんな場にしたい。あなたのサポートがあれば、それは可能です。サポート感謝します!松廼屋 matsunoya
