
人気講師ノート7 振動分光法
振動分光法といえば,赤外吸収分光法(Infrared Absorption Spectroscopy)とラマン分光法(Raman Spectroscopy)です。研究室に配属すると,先輩や指導教官から「IR測って~!」とか「ラマン測って~!」といわれます。
お気づきの方もいると思いますが,ここから一般の方には興味ないNoteが始まります。。。平易に書いています。質問どしどしコメントしてください。
お気に入りの機器分析LINEスタンプを紹介します!
1. 振動分光法で出来ること
先刻までに説明してきた電磁波のうち,赤外線や可視光線を使う分析法といえます。他の電磁波と比較すると以下のようなイメージになります。


振動分光法では,測定対象物の「元素環境」「官能基」「官能基の環境」などがわかります。官能基というのは,-CH4(メタン)とかーC6H5(ベンゼン)とか>C=O(ケトン)などのことを言います。
目的物質にどのような官能基が含まれているかを決定したいときに威力を発揮します。また,「官能基の環境」というのは,【水素結合の強さ】など,分子間で働く相互作用の【強さ】を見積もることができます。
2. 振動分光法の参考サイトについて
ラボや学生実験で赤外やラマンを使用した際には,必ず言われるのが
「それそれのピークを同定してきてね~」
と、結構【難しい】課題を出されます。結構時間をかけてもわからないです。というのも,有機系や薬剤系の方はわかると思いますが,①振動分光法は測定物質(大体の構造)がわかっている状態で目的物質ができているかを確認するために分析を行うためです。
未知試料のIRスペクトルから【何かを同定する】というのはかなり難しい。
といっても,学生実験では無茶ぶりされるので参考になるサイトを紹介します。
参考サイト1.SDBS
産総研が無償で提供している【有機化合物のスペクトルデータベース】です。アクセスしていただき,「免責事項に同意したうえでSDBSを利用する」をクリックすると,検索画面が開きます。
調べたい物質の
> 化合物名
> 分子式
を入力して,欲しいスペクトル(画面右上)にチェックを入れて【Search】をクリックすると検索してくれます。
参考サイト2.Analytical Chemistry Infrared (IR) Spectroscopy
英文ですが非常に簡潔にまとめられていて,一度は読んでみましょう。
3. 単位について
では、実際のIRスペクトルを見てみましょう。(スペクトル引用元)
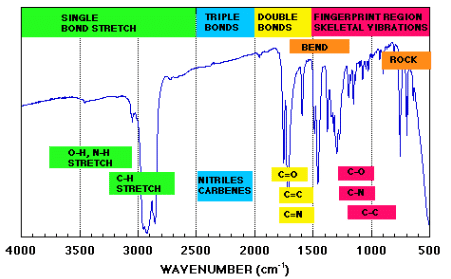
横軸は,cm-1(ウェーブナンバー)です。
※筆者が大学で学んでいた際には,「カイザー」と読んでいましたので,カイザーと読んでいる研究者がいれば大体の年齢がばれちゃいます。
Wavenumber=波数です。これまでのノートは,【波数】ではなく【波長】で議論してきましたし,他の電磁波分析においては【波長】が使われます。
波数,波長,ついでに【振動数】の関係式は以下のとおりです。

波数と波長は,反比例の関係にあることは覚えておいてもらいたい!!
波長は短いほうがエネルギーが大きいですが,波数は高いほうがエネルギーが大きくなります。
4. 赤外吸収スペクトルのチャートの見方
先ほどの赤外吸収スペクトルをしまします。
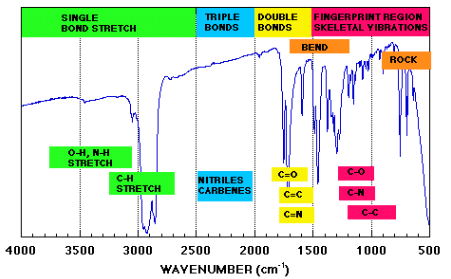
測定範囲は,4000~650(500)cm-1である。4000~1500cm-1と1500~650cm-1の二つの領域に分けて考えます。
※この時,波数が大きいほうが高いエネルギーを持っています。
高波数側には,官能基ごとに大体決まった位置にピークが出てくるので構造決定に利用できます。高波数側から,同じ元素であれば 三重結合→二重結合→単結合 の順に。官能基の片方が水素であれば,O-H→N-H→C-H の順にピークが出ることが多い。
一方、低波数側には「複雑な吸収スペクトル」が観測される代わりに,このあたりのピークは相互作用によってあまりシフトしません。つまり,分子構造に由来するピークがでるので、濃度(相互作用の影響)を考慮せずに,ピークが一致することで,未知化合物の同定が行えることがある。
この低波数側の領域を「指紋領域」といいます。
官能基の出るピーク位置を覚える必要があるのか??など,原理については人気講師ノート8に続きます。
本ノートは以上です。
おひねりいただければ、研究室の学生と焼肉でも食べに行ってきます!!
ここから先は
¥ 100
Amazonギフトカード5,000円分が当たる
学生から大好評だった授業ノートを公開します。役立てていただければ幸いです。また,家でできる実験も書いていきますね。
