
共有結合結晶①【改】
ダイヤモンドと黒鉛が最も有名です。ダイヤモンドは正四面体、黒鉛は主に正六角形が連なった構造 です。
非金属元素の原子が次々と共有結合で結びついた結晶を共有結合結晶といいます。炭素Cやケイ素Siの単体や、二酸化ケイ素SiO2などがあります。
共有結合結晶は、化学的に安定で、融点が高く、きわめて硬い。一般に、水に溶けにくく、電気を通しにくいです。
ダイヤモンド

ダイヤモンドは、各炭素原子が隣りの4個の炭素原子と共有結合して正四面体になり、それがくり返された構造をもちます。炭素原子C1コは価電子4コをもっています。正四面体のかたちになるとき、価電子4コを全て使い切ります。自由に動ける電子が1つもないため、電気を通しません。


ダイヤモンドは非常に硬く、熱を伝えやすいです。人工の薄層ダイヤモンドを電子機器の放熱板などに使う研究が進んでいます。
黒鉛

黒鉛は、各炭素原子が隣りの3個の炭素原子と共有結合して正六角形が連なった平面網目状構造をつくります。続いて、それぞれの層の間に弱い分子間力がはたらき、それが何層にも重なった構造です。
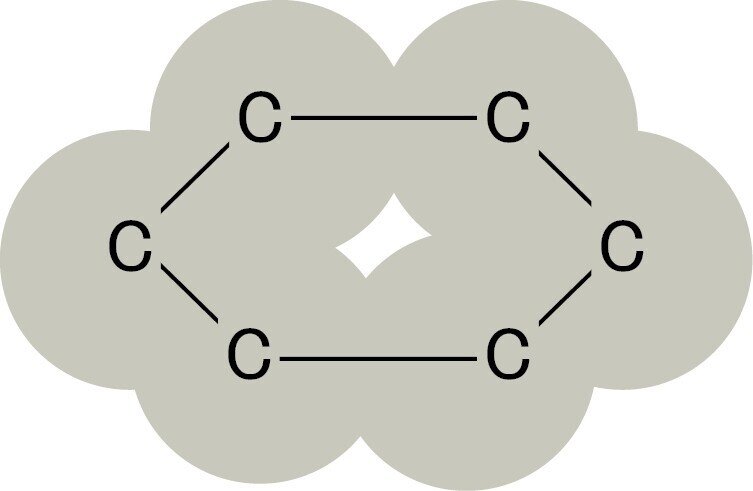

層と層の間は、弱い分子間力しかはたらいていないため、黒鉛はこの平面方向に沿ってうすくはがれやすく、やわらかいです。黒鉛の炭素原子の価電子は4コのうち3コが共有結合に使われています。残りの1コは、自由に動くことができるため、黒鉛は電気をよく通します。
ダイヤモンドと黒鉛は互いに同素体です。色、硬さ、電気伝導性などをまとめると次のようになります。

