化学の観点から解説する現代めっき技術シリーズ 第九回「めっき液・めっき皮膜の評価・解析法―めっき液の評価・分析法第一回―」
1.はじめに
お久しぶりです、Hazaculaです。今回は、めっき液の分析評価法についてお話ししましょう。めっきは、皮膜の物性も重要ですが、めっき液が扱いやすくないとお話になりません。また、めっき液の研究開発においてはめっき液の内容成分の分析も必要です。では実際、どのような分析評価法があるのでしょうか? 液分析法はそれこそ片手どころか両手の指を総動員しても間に合わない数がありますが、実際にめっき液の分析に使われるのはそのごく一部です。見ていってみましょう。
2.めっき液の各種分析・評価法
実際にめっき液でよく使われる分析・評価法には何があるかと言うと、
ハルセル試験
ハーリングセル試験
粘性
表面張力
ICP
原子吸光
クロマトグラフィー(HPLC、IC)
キャピラリー電気泳動
CVS
UV-Vis吸光光度法
等があります。まぁ他にもまだいろいろあると言えばありますが、とりあえず今回は上記9つをそれぞれ見ていってみましょう。
3.ハルセル試験とハーリングセル試験
この2つの試験法は溶液の分析法というわけではありませんが、どこかで紹介する必要があるため、ここでついでに紹介することにします。
ハルセル試験は、下図のような台形の容器にめっき液を入れてめっきをするやり方です。つまり、陽極に対して陰極の基板は斜めになっています。ちなみに基板は、図のような長方形のものを使います(めっきの色の違いが分かり易くなるように、また膜厚測定がしやすくなるように、銅基板や黄銅基板、ニッケル基板、などをめっき液に応じて使い分けます。)

なぜ斜めにするのかと言うと、電流密度の差を意図的に作り出すためです。セルを上から見ると、左側は陽極と近いため電流密度が高く、右側は陽極と遠いため電流密度が低くなります(電場は距離の近い方に集まろうとするので)。

つまり、一枚の基板で電流密度が高い領域から低い領域まで、めっき皮膜の外観を一発で確認できるのがハルセル試験となります。撹拌の有無による影響も、エア撹拌ができるハルセル試験層が市販されているので把握可能です。なお、どれぐらいの電流密度がかかっているかは、ハルセル早見板を使うことでわかります。大体低電流部の10倍量の電流密度が高電流部にかかることになります。ハルセル試験はめっき液の電流密度ごとの析出の様子などを一発で把握できるので、めっき液の大雑把な分析管理などにも使えます。実際のめっき後の基板の様子は下図のような感じです。高電側は大体の場合“焦げ”(ヤケとも呼ばれる)、低電側は光沢あるいは白くもりとなることが多いです。この時の焦げやくもりの範囲などで、どの程度の電流密度範囲できれいなめっきが可能か評価を行います。

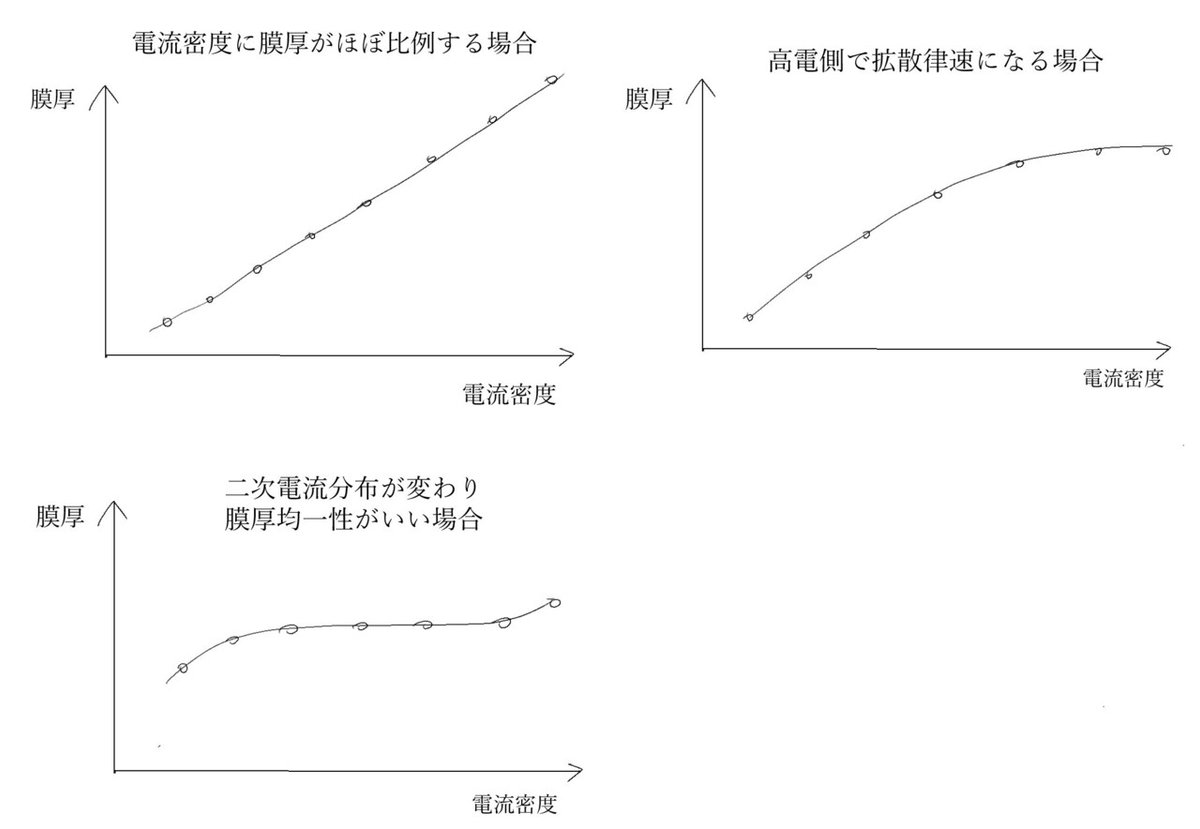
ただし、二次電流分布がめっき液によって変わるため、電流密度の完全な把握は難しく、あくまで大雑把な把握にしか使えません。ちなみに、電流密度に対する膜厚分布は大体下図のようになります。膜厚均一性のいい浴を使うと電流密度に対して膜厚は寝るようになり、膜厚均一性が悪い浴だと電流密度に対して右肩上がりになるようになります(ただしあくまで傾向であり、定量的な分析には向きません)
電流密度による影響をより正確に把握するには、下図のハーリングセルを使います。

図のような長方形の層の左右に陰極を配置し、真ん中に陽極を配置します。陽極の位置を変えることで、左右に陰極の電流密度を変えることができます。これにより、電流密度差に起因するめっき速度の差を知ることができるのです。
ただし、これでもめっき液の二次電流分布の影響などは完全には消せませんので、電流密度ごとのめっき速度を測りたかったら、ビーカーで小さいベタ銅板などにめっきを行ってみるしかありません。それでも、撹拌の影響は出てしまいます(特にバリア金めっきなど)。めっき液の電流密度の影響を正確に測るのは難しいのです。
4. 表面張力と粘性
表面張力と粘性を測るには、専用の器具を使います。
表面張力の測定には、白金製の輪っかを液面にくっつけ、これが表面張力を引きちぎる時に必要な力を測定します。
粘性の測定には、狭いガラス管内をどれぐらいの速さで通り抜けられるかで測ります。高粘度ほど通過に時間がかかります。

正確な計算には流体物理とかの面倒な計算が必要なのでここでは取り上げませんが(勉強不足で申し訳ない……)、大体の場合に於いて測定器具を買った時点で説明書に計算方法が書いてあるので、それに従えば問題ありません。
5. 浴中の元素分析法
さて、そろそろ専門的な話に移っていきましょうか。浴中の元素(特に金属種)の分析としてはどのような手法があるでしょうか? 個別の化学反応を利用する滴定は置いておくとして、機械的に分析する手法としては、ICPと原子吸光の2種類があります。これらはいずれも、金属原子と光との相互作用を利用して主に金属元素の種類と濃度を測定する手法です。それぞれ見ていってみましょう。
原子吸光分析では、金属を含む溶液を噴霧して高温の炎の中にぶち込みます。すると、溶液中の金属種がイオンだろうとなんだろうと高温の炎中で原子となります。ここに光を通すと、金属の種類に応じた特有の波長の光を“吸収”します(細かい原理は量子力学が絡んでくるのでここでは割愛)。光を吸収する量は溶液中の金属種の濃度によって決まるので、吸収量を調べることで浴中濃度を決定できるのです。
ICP発光分析も原子吸光分析と似ていますが、少々違います。ICPの場合は、金属を含む溶液を噴霧してアルゴンのプラズマ中にぶち込みます。すると、金属の種類に応じた特有の波長の光を“発光”します。このときの発光量が金属種の濃度によって決まるので、発光強度から浴中濃度を決定できます。

原子吸光もICPもそれぞれ似た分析法ですが、一長一短があります。まず原子吸光分析では、それぞれの原子に固有の波長の光(それこそ小数点以下3桁のオーダーで同一の波長の光)を出す必要があります。これはもう、同じ元素を使うしかありません。そこで、原子吸光では測定したい元素と同じ元素を用いたホローカソードランプというものを使います。別種の元素を測りたかったら、その元素のホローカソードランプに切り替えなくてはなりません。つまり、元素種ごとにこのホローカソードランプを交換する必要があるのです(これがかなりめんどい)。さらに、被測定溶液の濃度に対する要求がシビアです。原子吸光とは、つまり光の吸収量によって濃度を決めるのですが、大雑把に言ってしまうと、“被測定溶液中の金属濃度が濃すぎる”と“光がほとんど吸われて”しまい、濃度が測れなくなってしまうのです。また逆に、濃度が薄すぎてもいけません。1000粒の米粒と999粒の米粒の差がほとんど見分けられないのと同様に、濃度が薄すぎても正確な測定が出来なくなってしまいます。そのため、最適濃度範囲というものがあります。この濃度範囲を外れてしまった場合には、試料を希釈したりして濃度を調節せねばなりません。さらに、測定液のマトリックス(目的成分以外の他の成分濃度)の影響も大きいので、正確な測定のためには他の成分の濃度も合わせなくてはなりません。結構めんどいです。ただし、単一元素であれば測定に係る時間はICPより短くて済みます。使うガスもICPより安価で済みます。
一方で、ICPに関してはそのようなめんどさがありません。ICPは原子自体の発光を測るため、ホローカソードランプは不要ですし(つまりランプ交換の必要がない)、測定可能レンジも広いです(ただし、あまりに濃すぎると、発光が強すぎて測定器の測定可能範囲を越えてしまうが)。さらに、薄い試料にもつよいです。これは発光だからこその強みで、米粒0と1粒の差が明らかなように、ほんのちょっとでも金属が存在すれば発光が出てくるため低濃度での感度がいいのです。また、マトリックスの多少のブレにも強いです。ただし、使用するアルゴンガスのコストが結構かかってきますし、原子吸光より測定に時間がかかるので、そこがネックではあります。
6.浴中のイオン分析法
ICPと原子吸光は浴中の元素(特に金属元素)の濃度を測定するのに優れた方法ですが、しかし万能ではありません。例えば、浴中に硫酸イオンSO42-、亜硫酸イオンSO32-、硫化物イオンS2-、メタンスルホン酸イオンCH3SO3-が溶けていた場合、それぞれを区別して測定することはできません。いずれも硫黄Sの濃度として出てきてしまいます。これは当たり前で、原子吸光もICPも高温の炎やらプラズマやらの中に試料をぶち込むので、分子構造はみんな破壊されてしまうのです。しかし、これでは困ります。浴の維持には浴中の分子をそれぞれ分けて分析しなければなりません。なんとかこれらイオンを分離して測定できませんでしょうか?
その解答が、HPLC(高速液体クロマトグラフィー)、IC(イオンクロマトグラフィー)、キャピラリー電気泳動などの分析手法です。それぞれ見ていってみましょう。まずは、クロマトグラフィーと名付けられている奴から見ていきましょう。キャピラリー電気泳動はクロマトグラフィーとは原理が少々違うのですが、その分析結果たるグラフの見方はクロマトグラフィーと似ているので、これは後回しにます。
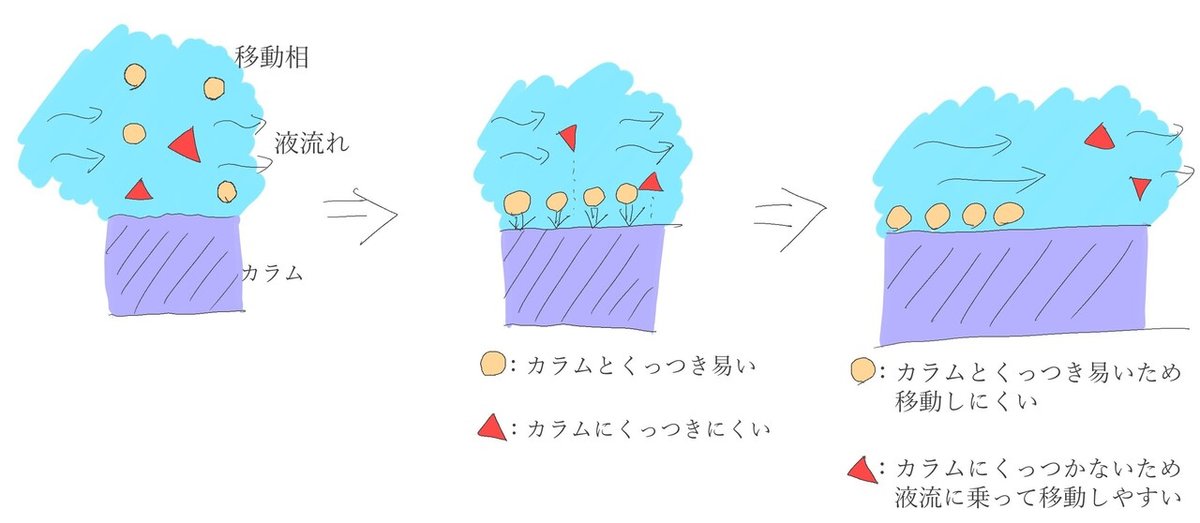
まずはクロマトグラフィーから見ていってみましょう。クロマトグラフィーでは、カラム(固定相)と移動相の二つを用います。分かり易く図示すると、以下の感じです。カラムにはシリカゲルや表面を有機分子で修飾したシリカゲルなどが、移動相には水やアセトニトリルやメタノール、及びそれらの混合物などが使われます。

クロマトグラフィーの原理は簡単です。分離したい成分を含む液を移動相と共に流します。分離したい成分はカラムと親和し、ミクロで見るとくっついたり離れたりします。このくっつきやすさは成分ごとに微妙に違うんですが、液を流していくとくっつきにくい成分はより流れ出る方向に動き、くっつきやすい成分はあまり動かないので、各成分が分離できます。こうして分離した後に各種検知器(UV-Vis吸収や屈折率測定)で成分量を測ります。
実際の結果(クロマトグラム)は以下の感じです。

キャピラリー電気泳動はクロマトグラフィーと似ていて、移動相ではなく電気の力で成分を流します。泳動液中に測定したい溶液を少量ぶち込み、左右に電圧をかけます。すると、陽イオンはマイナス側に、陰イオンはプラス側に引っ張られて、移動します。この時、移動のしやすさはイオンの電荷や大きさ、溶媒との相互作用などで微妙に変わるので、クロマトグラフィーのように成分の分離ができるのです。測定結果もクロマトグラムとほぼ同じなので、ここでは割愛します。

クロマトグラフィーもキャピラリー電気泳動も、様々な成分の分離が可能です。特に便利なのが、有機化合物の分離に使えるという点です。めっき液には結晶調整のための有機成分が色々と添加されますが、もちろんこれらの定量をしなければなりません。しかし、有機化合物はICPや原子吸光では測れないし、化学反応を活用するのも難しいです(有機化合物の反応は無機反応よりはるかに遅く、特異的な反応も難しいため、分離定量が困難です)しかし、クロマトグラフィーやキャピラリー電気泳動を使えば、これらの分離定量が可能なのです。そのため、特に有機化合物を多用するニッケルめっき液以上の貴金属めっきの管理には、HPLCなどが必須とされることもあります。
欠点としては、同じ位置にピークが出ても、本当に同じ成分か分からない点が挙げられます。これは特に有機成分に顕著で、有機化合物は色々な構造のものが多量に存在します。それらの中には当たり前ですが、ほとんどおんなじ親和性を示すものも無数にあるわけで、同じ位置にピークが出ても「本当に同じ成分」だとは断言できないのです。そのため、ある程度“何が入っているか”予想がついている液にしか使えません。内容成分が本当に同じものか分析したければ、何らかの方法でその成分を取り出して、IRなりMSなりNMRなりで分析しなければいけないのです。
7.CVS
CVSはちょっと風変わりな測定法です。クロマトグラフィーもキャピラリー電気泳動も、いずれも測りたい物質をなんらかの方法で分離して定量する方法です。一方でCVSは、測りたい物質を“分離せずに”測れる方法なのです。具体的には、その物質が“めっき析出反応に与える影響”を利用して測定します。
具体的に考えてみましょう。CVS分析がよく使われるめっき液として、電解銅めっき液があります。電解銅めっき液には、光沢制御や皮膜形状制御のために2~3種類の有機化合物を添加します。これらはクロマトグラフィーなどで分析することも可能ですが、CVSの方がより簡便に測れるためによく使われるのです。さて、電解銅めっきの成分の一つであるPEG(ポリエチレングリコール)を測ることを考えましょう。
PEGは、めっきされた銅表面に緩く吸着することで、銅めっき反応を“抑制”します。では、PEG添加量を増やすと銅めっきはどうなるかといえば、当然ながら銅めっき反応は進みにくくなり、同じ量の電気を流してもめっきされる銅の量は減ってしまいます。なら、一定の電気量を流した時の銅めっきの析出量を、PEGの添加量をふってそれぞれ測定してみたら、検量線が引けるのではないか? と考えられます。これを実際にやっちゃうのがCVS分析です。
CVS分析では、白金電極を一定量の銅めっき液につけ、この電極を負極として電流を流してめっきをつけ、次に逆に正側の電位で電流を流して銅めっきを剥がします(この時の電気の流れ方で、析出した銅量を測ることができます)。そしてこれを、PEG添加量をふってそれぞれ行い、検量線を作成します。検量線が出来たら、測定したいめっき液をぶち込んで同様にめっきと剥離を行い、めっきされた銅量を測定するのです。これを検量線と比較すれば、PEGの量が求められます。

CVS分析の利点は、クロマトグラフィーなどと比べて比較的短時間で測定できる点です。装置自体も比較的小型で済みます。実際のめっき液の自動測定装置にも応用されていることが多いです。また、有機化合物がめっき反応に関与しさえすれば、測定できるという点も魅力です。実はクロマトグラフィーやキャピラリー電気泳動では、有機化合物にある程度UV吸収が無ければ測定が難しいという問題があります(キャピラリー電気泳動ではUV吸収が無くても測る方法はありますが、あくまで無機成分のように大量に入っている物前提です。有機化合物の濃度では厳しいです)。PEGはUV吸収? 何それ美味しいの? っていう有機化合物のため、クロマトグラフィーやキャピラリー電気泳動では測れませんが、CVSであれば測れるのです。
逆に欠点としては、“めっき反応自体”の促進抑制を測るため、目的成分以外にめっき反応に関与する他成分が入っていた場合、目的成分が正確に定量できなくなってしまいます。しかも反応の進みやすさ進みにくさを測るため、温度依存性が激しく、0.1℃温度が狂っただけで正確な値が出なくなります。また当たり前ですが、目的成分が全く未知の場合にその成分を特定することもできません。ある程度“何が”“どれだけ”入っているか分かっていないと使えない方法なのです。そのため、既知成分しか入っていないめっき液の管理に使用されることがほとんどです。
8. UV-Vis吸光光度法
紫外可視吸光光度法とも呼ばれます。測定液に紫外線~可視光線にあたる波長の光を通し、液を通過してきた光を波長ごとに分離して吸光度を測定します。このときの波長ごとの吸光度をプロットしたスペクトルを元にめっき液中の物質の定量分析を行うのがUV-Vis吸光光度法です。遷移金属イオンや不飽和結合を有する有機物質は紫外~可視領域の光をよく吸収します(原理は量子力学が絡むため割愛)。その波長は物質毎に固有なため、波長毎の吸光度を測ることで、内容物質の種類と濃度を求めることができるのです。ちなみに溶液は、石英製のガラスセルに入れて測ります。

UV-Vis測定は、装置さえ立ち上がっていればそれことものの数分で測ることができるため、めちゃくちゃ手軽な測定方法です。ただし、UV-Visは多の測定法と比べて特定成分を特異的に測定するのがめちゃくちゃ不得意です。というのも、UV吸収はほとんどの場合スペクトルの吸収幅が広く、他の成分の吸収と重なることが多くなってしまいます。さらに、有機物を含む電解めっき液だと、使用に伴って分解した有機物が蓄積します。こういう分解生成物は、多くの場合色んな波長の光をまんべんなく吸収してしまうため、他の吸収ピークを覆い隠してしまいます。一応、微分法の適用により定量することもできるのですが、それもまた限られた場合にしか使えません。そのため、かなり限られた場合にしか有効ではありません。ただ、他の成分の邪魔がないのであれば手軽な分析定量法となりますし、特に芳香環などを有する有機物に関しては高感度な定量法となります(芳香環のUV吸収は凄まじく強い)。
9.まとめ
いかがでしたでしょうか? ここに挙げたのはあくまでめっき液分析法の一部です。これら各測定法の得意不得意を理解して、適宜使い分けることが必要なのです。次回はまた別の分析法や、固体皮膜の分析法をご紹介しましょう。
それでは、Adios,amici!
Hazacula.
