
53)ニコチンアミドアデニンジヌクレオチド(NAD+)の補充は、ミトコンドリアを活性化し、老化した組織幹細胞を若返らせ、寿命を延ばす
体がみるみる若返るミトコンドリア活性化術53
ミトコンドリアを活性化して体を若返らせる医薬品やサプリメントを解説しています。
【幹細胞が組織を若返らせる】
組織の細胞には幹細胞(stem cell)と成熟した体細胞が存在します。
組織の幹細胞とは、組織固有の多分化能を有して各臓器・組織を構成する細胞の供給源となる細胞です。組織幹細胞は自己複製によって幹細胞を維持すると同時に、不均等分裂により一部が自己複製のサイクルから逸脱して成熟細胞へと分化して、組織を構成する細胞(体細胞)を作り出しています。
例えば、大腸粘膜組織の幹細胞は陰窩の最低部、基底膜直上に存在しており、自己複製によって幹細胞を維持すると同時に、不均等分裂によって分化した粘膜上皮細胞を作り出しています。粘膜上皮細胞に分化した細胞は、消化管内腔側に向かって移動し、数日で細胞死(アポトーシス)を起こして消化管内に脱落します。胃や食道や小腸でも、粘膜上皮の底部付近に幹細胞が存在し、粘膜上皮細胞が供給されています。
組織幹細胞は、分裂して自分と同じ細胞を作り出すことができ(自己複製能)、またいろいろな細胞に分化できる(多分化能)という二つの重要な性質を持ち、この性質により、限られた寿命のある体細胞を絶えず供給し、傷ついた組織を修復することができるのです。(下図)

図(A)組織の細胞には幹細胞と成熟した体細胞が存在する。幹細胞は組織固有の多分化能を有して各臓器・組織を構成する細胞の供給源となる。組織幹細胞は自己複製によって幹細胞を維持すると同時に、不均等分裂により一部が自己複製のサイクルから逸脱して成熟細胞へと分化して、組織を構成する細胞(体細胞)を作り出している。
(B)消化管粘膜組織の幹細胞は陰窩の最底部に存在しており、自己複製によって幹細胞を維持すると同時に、不均等分裂によって分化した粘膜上皮細胞を作り出している。粘膜上皮細胞に分化した細胞(体細胞)は、消化管内腔側に向かって移動し、数日で細胞死(アポトーシス)を起こして消化管内に脱落する。
【ニコチンアミド・アデニン・ジヌクレオチド (NAD) は幹細胞を若返らせる】
以下のような研究報告があります。
NAD⁺ repletion improves mitochondrial and stem cell function and enhances life span in mice.(NAD⁺の補充は、ミトコンドリアと幹細胞の機能を改善し、マウスの寿命を延ばす)Science. 2016 Jun 17;352(6292):1436-43.
【要旨】
組織の幹細胞(stem cell)は組織の維持と再生に不可欠であるが、加齢の過程で老化の影響を受けやすい。筋肉幹細胞の老化の制御における、酸化型ニコチンアミドアデニンジヌクレオチド(NAD+)の量とミトコンドリア活性に対するNAD+の作用の重要性を示す。
NAD+の前駆体のニコチンアミドリボシドの補充による治療は、ミトコンドリアのストレス応答とプロヒビチン(prohibitin)タンパク質の合成を誘導し、これらの反応は老齢マウスの筋肉幹細胞を若返らせた。
ニコチンアミドリボシドの補充は、筋ジストロフィーのマウスの実験モデルで、筋肉幹細胞の老化を抑制した。さらに、ニコチンアミドリボシドの補充は神経細胞とメラノサイト(メラニン形成細胞)の幹細胞の老化を遅らせ、マウスの寿命を延ばした。
以上の結果から、細胞内の酸化型ニコチンアミドアデニンジヌクレオチド(NAD+)の量を維持する治療法は、哺乳動物において、老化した幹細胞を活性化し、寿命を伸ばす可能性が示された。
成人では、組織の恒常性は幹細胞の機能に大きく依存しています。成人の幹細胞は、継続的に増殖する組織(造血組織、胃腸粘膜上皮、皮膚など)だけでなく、損傷後に再生を必要とする場合は、通常は増殖を静止している組織(骨格筋や脳など)でも不可欠です。
老化に伴って組織の幹細胞の増殖能や機能が低下すると、組織の恒常性が低下し、損傷後の組織の再生能力や回復力が低下します。
老化に伴う組織幹細胞の機能の低下は、ミトコンドリア機能の低下が主要な原因となっています。
そして、老化によって引き起こされるミトコンドリア機能障害は、酸化型ニコチンアミドアデニンジヌクレオチド(NAD+)の枯渇に起因する可能性が報告されています。
したがって、ニコチンアミド・リボシド(NR)やニコチンアミド・モノヌクレオチド(NMN)などのNAD+の前駆体の補充は、老化で低下したミトコンドリア機能を活性化して、組織幹細胞の増殖能や機能を高めることが指摘されています。
つまり、NAD+の補充が哺乳類の寿命を延ばすための魅力的な戦略として期待されています。
【ニコチンアミド・アデニン・ジヌクレオチド (NAD) は補酵素として多くの酵素反応に関与する】
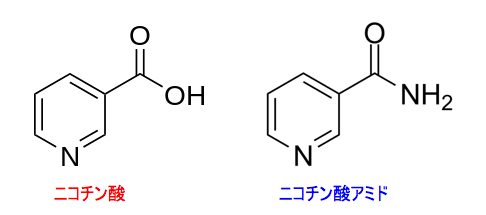
ニコチン酸とニコチン酸アミドは総称してナイアシン (Niacin) あるいはビタミンB3とも言います(図)。水溶性ビタミンのビタミンB複合体の一つで、糖質や脂質やタンパク質の代謝に不可欠です。
ナイアシンは電子伝達体のニコチンアミド・アデニン・ジヌクレオチド (NAD) やニコチンアミド・アデニン・ジヌクレオチドリン酸 (NADP) に変換され、酸化還元反応 (電子が供与体分子から受容体分子に転移する反応) に関与する酵素の補酵素として機能しています(図)。

NAD+は全ての真核生物で用いられる電子伝達体です。さまざまな脱水素酵素の補酵素として機能し、酸化型 (NAD+) および還元型 (NADH) の2つの状態を取ります。NAD+が水素の受け取り手となります。酸化型のNAD+が水素と電子を受け取って還元型のNADHになります。NADHは他の物質の還元に使われます。NAD+は生物のおもな酸化還元反応の多くにおいて必須成分(補酵素)であり、好気呼吸(酸化的リン酸化)の中心的な役割を担っています。
【長寿遺伝子サーチュインはNAD+ 依存性の酵素】
NAD+は古くから酸化還元反応の補酵素として知られていますが、サーチュインの基質としての役割が知られるようになりました。サーチュイン(サーチュインファミリー)は食物不足(飢餓状態)の時に活性化される遺伝子群で、NAD依存性脱アセチル化酵素です。
哺乳類では七つのサーチュイン(SIRT1~7)が存在し、核内(SIRT1、 6、7)、ミトコンドリア(SIRT3、4、5)、細胞質(SIRT2)に局在します。サーチュインがターゲットのタンパク質のリシン残基を脱アセチル化する反応をNAD+が促進することで、健康や長寿に関わる様々な生命現象に関与しています。
栄養素、特に糖が減少するとNAD+が増え、サーチュインが活性化します。サーチュインはNAD+/NADHの比率の変動を感知することによって、細胞内の栄養素の供給状況や物質代謝の状況を把握しているのです。
サーチュインはタンパク質の脱アセチル化(アセチル基を除去する)によって様々な酵素の活性を調整し、細胞周期、代謝、抗酸化システム、オートファジーなどの細胞機能の制御に関与しています。その結果、細胞老化や発がんを抑制し、寿命を延長する効果を発揮します。
カロリー制限(栄養不良を伴わない低カロリー食事療法)で、霊長類を含む多岐にわたる生物種において老化を遅延させ、寿命を延長させることが知られていますが、このカロリー制限のときに活性化されて寿命延長と抗老化作用に関与するのがサーチュイン遺伝子です。サーチュイン1はPGC-1αを脱アセチル化することによって活性化します。活性化したPGC-1αはミトコンドリア新生を亢進します。

図:NAD+前駆体のニコチンアミド・リボシドやニコチンアミド・モノヌクレオチドはNAD+/NADH比を高めてサーチュイン1を活性化する。サーチュイン1はPGC-1α(ペルオキシソーム増殖因子活性化受容体γコアクチベーター1α)を活性化し、PGC-1αはミトコンドリア新生を促進する。
加齢とともにNAD+の産生量や体内量が減少し、サーチュインの活性が低下し、ミトコンドリア新生が低下します。特にエネルギー消費の多い筋肉、脳、心臓などでミトコンドリアの機能や新生が低下します。カロリー制限や運動やレスベラトロールのような食品成分がミトコンドリア機能を維持し高める場合、NAD+とサーチュインが重要と考えられています。
【加齢とともにNADは減少する】
老化は、がん、糖尿病、心血管疾患などの成人病や、アルツハイマー病やパーキンソン病などの神経変性疾患の危険因子の一つです。各臓器,組織の恒常性は,それぞれの組織の幹細胞によって維持されています。組織幹細胞の多くは老化によりその機能が低下することが示されており、老化関連疾患の原因となっています。
サーチュインの活性化は、カロリー制限における寿命延長や健康増進に関わる効果の多くを説明すると考えられています。老化および多くの老化関連疾患は、ニコチンアミド・アデニン・ジヌクレオチド(NAD+)量の低下、およびNAD+依存性脱アセチル化酵素サーチュインの活性低下と密接な関わりを持つことが示されています。
老化に伴いNAD+量およびサーチュイン活性が低下しますが、ニコチンアミド・リボシド(nicotinamide riboside:NR)やニコチンアミド・モノヌクレオチド(nicotinamide mononucleotide:NMN)などのNAD+中間代謝産物の補充がサーチュインを効果的に再活性化することが明らかになっています(図)。

図:ニコチンアミド・アデニン・ジヌクレオチド(nicotinamide adenine dinucleotide:NAD+)はトリプトファンやニコチン酸やニコチンアミドなどから生成するルートもあるが、特にNAD+の前駆物質であるニコチンアミド・モノヌクレオチド(nicotinamide mononucleotide:NMN)とニコチンアミド・リボシド(nicotinamideriboside:NR)をサプリメントとして摂取すると体内のNAD+を増やすことができる。
NAD +前駆体であるニコチンアミドリボシド(NR)やニコチンアミドモノヌクレオチド(NMN)の投与は、筋肉や肝臓や心臓におけるミトコンドリア機能を改善し、これらの臓器機能を高めることがマウスなどの動物を使った複数の実験で示されています。
【ニコチンアミドリボシドの服用は血液中のNAD+を増やす】
NAD+の前駆体のサプリメントとしての補充は体内のNAD+の濃度を高めることができます。以下のような報告があります。
Nicotinamide riboside is uniquely and orally bioavailable in mice and humans(ニコチンアミド・リボシドはマウスおよび人間において、独特かつ経口的に生物学的に利用可能である)Nat Commun. 2016 Oct 10;7:12948.
【要旨】
ニコチンアミド・リボシドは、NAD+前駆体ビタミンとして広く使用されている。 ここでは、人間の血中NAD+代謝におけるニコチンアミド・リボシドの経時的および用量依存的な影響を検討する。
1人の個人の予備試験で、ニコチンアミド・リボシドの単回経口投与で血中のNAD+濃度は2.7倍も上昇し、マウスの肝NAD+を上昇させた。さらに、ニコチン酸とニコチンアミドより優れた薬物動態を示した。
さらに、100mg、300mg、および1,000 mgのニコチンアミド・リボシドの単回投与により、血中NAD+は用量依存的に増加することが示された。
以下のような報告があります。
An open-label, non-randomized study of the pharmacokinetics of the nutritional supplement nicotinamide riboside (NR) and its effects on blood NAD+ levels in healthy volunteers.(健康なボランティアにおける栄養補助食品ニコチンアミドリボシド(NR)の薬物動態と血中NAD+濃度に対する影響に関する非盲検非ランダム化研究)PLoS One. 2017; 12(12): e0186459.
【要旨の抜粋】
目的:この研究は、人間におけるニコチンアミドリボシドの経口投与における薬物動態と血液中のニコチンアミドアデニンジヌクレオチド(NAD+)レベルに対するニコチンアミドリボシドの影響を検討した。
背景:ミトコンドリア機能障害は心不全の発症と進行に重要な役割を果たすが、ミトコンドリアを標的とした治療法は行われていない。
最近のマウスを使った研究では、NADH / NAD+比の不均衡と、心筋を含む複数の組織のミトコンドリア機能障害との関連が報告されている。さらに、NAD+前駆体であるニコチンアミドモノヌクレオチド(NMN)は心機能を改善し、別のNAD+前駆体であるニコチンアミドリボシド(NR)は筋肉、肝臓、褐色脂肪のミトコンドリア機能を改善した。したがって、人間におけるニコチンリボシドの薬物動態研究は、将来の臨床試験にとって重要である。
方法:8人の健康なボランティアを対象としたこの非盲検非ランダム化研究では、1日目と2日目に250 mgのニコチンアミドリボシドを経口投与し、7日目と8日目に最大用量1000 mgを1日2回に増量した。9日目の朝に1000 mg のニコチンアミドリボシドを投与した後、被験者は24時間の薬物動態研究を完了した。全血中のニコチンアミドリボシドのレベル、臨床血液化学、およびNAD+レベルを分析した。
結果:経口ニコチンアミドリボシドは忍容性が良好で、有害事象は認められなかった。 ニコチンアミドリボシドとNAD+の両方で、投与前に比較して有意な増加が観察された。NAD+は100%の増加を認めた。 ニコチンアミドリボシドおよびNAD+レベルの投与前から投与後9日目までの絶対変化は、高い相関を認めた。
結論:人間において、ニコチンアミドリボシドは血液中のNAD+を増加させるため、ニコチンアミドリボシドは遺伝性および/または後天性疾患によるミトコンドリア機能障害の患者の治療法としての可能性がある。
この研究では、1日目と2日目は1日250mgを1回、3日目と4日目は250mgを1日2回(1日500mg)、5日目と6日目は500mgを1日2回(1日1000mg)、7日目と8日目は1000mgを1日2回(1日2000mg)と増やして投与しています。
9日目の朝に1000mgを投与した時点を0時としてそれ以降24時間の血中濃度を測定しています。
投与前に比べて、9日目にはNAD+の血中濃度は平均100%(35〜168%)の上昇を認めたという結果です。この研究ではニコチンアミドリボシド服用による副作用は認められていません。
ニコチンアミド・リボシドを毎日1から2グラム程度を摂取すると、筋力低下や心臓や神経系などの老化性疾患の進行予防に役立つ可能性は高いと言えます。
この記事が気に入ったらサポートをしてみませんか?
