
132章 免疫チェックポイント阻害薬のリウマチ性免疫関連有害事象(irAE) Autoimmune Complications of Immune Checkpoint Inhibitors for Cancer
キーポイント
がんの治療に用いられる免疫チェックポイント阻害剤は、リウマチ性表現型を含む免疫関連有害事象として知られる多種多様な炎症性症候群を引き起こす可能性がある。
免疫関連有害事象の根底にある正確な機序は十分に定義されておらず、事象の種類によって異なる可能性がある。
炎症性関節炎は、リウマチ患者が遭遇する免疫関連有害事象の中で最も一般的なものである。
炎症性関節炎は、リウマチ専門医が遭遇する最も一般的な免疫関連有害事象であり、重症度、発症までの期間、罹患関節などの点で不均一な症状を示すことがある。
リウマチ性免疫関連有害事象の治療は、通常コルチコステロイドから始まるが、ステロイドが無効な患者、重症の患者、ステロイドを断薬できない患者には、他の免疫抑制療法が有効である。
免疫チェックポイント阻害薬による治療を受けた自己免疫疾患の既往のある患者では、基礎疾患が再燃する可能性がある。


PD-1, PD-L1は疲弊したT細胞を活性化させる、樹状細胞やNK細胞への抑制作用を阻害する
活性化されたT細胞はCTLA-4がCD80もしくはCD86と結合し、T細胞の活性化を抑制する
イピリムマブ(ヤーボイ)(最初のICI):CTLA4阻害
ニボルマブ(オプジーボ):PD-1
ペンブロリズマブ(キートルーダ):PD-1
デュルバルマブ(イミフィンジ):PD-L1
irAEの基礎となるメカニズムは、臓器系を問わずよく理解されていない。臨床症状や特定の免疫抑制療法に対する反応の違いを考えると、複数のメカニズムが関与している可能性が高い。

Nat Rev Dis Primers. 2020 May 7;6(1):38.
免疫関連有害事象irAEマネジメント mini(三井記念 峯村先生)
機序(Trends immunol. 2019;40: 511-523)
潜在していた自己免疫病態の増悪
新規発症の自己免疫病態
消化管粘膜の免疫寛容の破綻による腸内細菌の変化
ICIの抗腫瘍効果に随伴した組織損傷
下垂体表面のCTLA-4抗原に対するCTLA-4阻害薬の結合
irAEの病型、頻度の規定因子
1) ICIの種類(ex:肺炎、甲状腺機能低下症、白斑は、PD-1阻害でより一般的である。)
2) 単剤か併用か →併用、特にCTLA-4i+ PD-1iだと致死的AEが早期に出現する可能性がある
3) CTLA-4阻害薬の用量依存性
Pearl: 下垂体炎はCTLA-4阻害薬でより一般的にみられるが、抗PD-1薬や抗PD-L1薬を投与している患者でも依然としてみられるため、組織との交差反応性だけが唯一のメカニズムではない。
comment: “Expression of CTLA-4 or PD-1/PD-L1 on target tissue: CTLA-4 is expressed on pituitary tissue, the target tissue of hypophysitis.36 Though hypophysitis is more common with CTLA-4 inhibitors, it still occurs in patients on anti-PD-1 or anti-PD-L1 drugs, thus cross-reactivity with tissue is not the only mechanism at play.“
CTLA-4は、下垂体組織に発現している(Am J Pathol 186(12):3225–3235, 2016.)。
Pearl: メラノーマを対象としたニボルマブの研究では、irAEを発症した症例では、irAEを発症していない症例と比較して抗癌治療の奏効率が高かった;腫瘍の退縮率が最も高かった(80%)のはグレード3以上のirAEを発症した症例であった。
comment: “In a study of nivolumab for melanoma, there was a higher response rate in those with irAEs as compared with those with no irAEs; the highest rate of tumor regression (80%) was in those with grade 3 irAEs or higher.(Oncol 22(10):1232–1237, 2017.)”
ICIの一般的な毒性発現機序が、免疫系の活性化と密接に関連していることは、多くのがん治療法の中でも独特であり、治療を複雑にする可能性がある。
進行期メラノーマに対するCTLA-4とPD-1阻害の併用療法では、3年生存率はほぼ60%である
進行期非小細胞肺がん(NSCLC)もICI療法の適応であるが生存利益はより緩やかである。腫瘍変異負荷の高い患者における併用療法の1年無増悪生存率は42.6%。
メラノーマ患者では、皮膚炎や消化器系のirAEが起こりやすいが、肺炎は起こりにくい(Ann Oncol 28(10):2377–2385, 2017.)
Pearl: 炎症性関節炎は最も一般的なリウマチ性irAEであり、その発生率はレトロスペクティブ研究で3%~7%と推定されている。
comment: “rheumatologic irAEs are rarely life threatening or severe by oncology adverse event grading and are therefore less likely to be reported. Information on epidemiology comes primarily from retrospective studies at single institutions or using databases for drug adverse event reporting. Inflammatory arthritis appears to be the most common rheumatic irAE, with estimates of prevalence ranging between 3% and 7% in retrospective studies.(Cancer Immunol Immunother, 2017)”
あるシリーズでは、ほとんどの患者は最初に大関節が侵されたが、3分の1は最初に指や手首の小関節が侵された(Semin Arthritis Rheum, 2018.)。
CTLA4/PD-1/PD-L1併用療法を受けた患者はPD-1/PD-L1単剤療法を受けた患者よりも炎症マーカーが高いようである。また、併用療法を受けた患者は膝から始まる関節炎を有し、反応性関節炎の表現型を有する可能性が高い(Semin Arthritis Rheum, 2018.)
関節炎はICI開始後数か月以内に起きる(Med Clin North Am. 2021 Mar;105(2):227-245.)
ただ1年以上経過してから起きることも、ICI中止後にもありうる。
頻度は、ICI併用>PD-1/PD-L1阻害薬>CTLA-4阻害薬
irAE関節炎は遷延する(Ann Rheum Dis. 2020 Mar;79(3):309-311.)
ICI中止後も12wks以上遷延する関節炎がある。
鑑別のフロー(Arthritis Rheumatol. 2021 Apr; 73(4): 553–565.)

Pearl: irAE関連のsiccaの小唾液腺の生検では、原発性シェーグレン症候群とは異なる炎症が認められている。
comment: “Biopsies of the minor salivary gland have shown inflammation dis- tinct from that of primary Sjogren’s syndrome .”
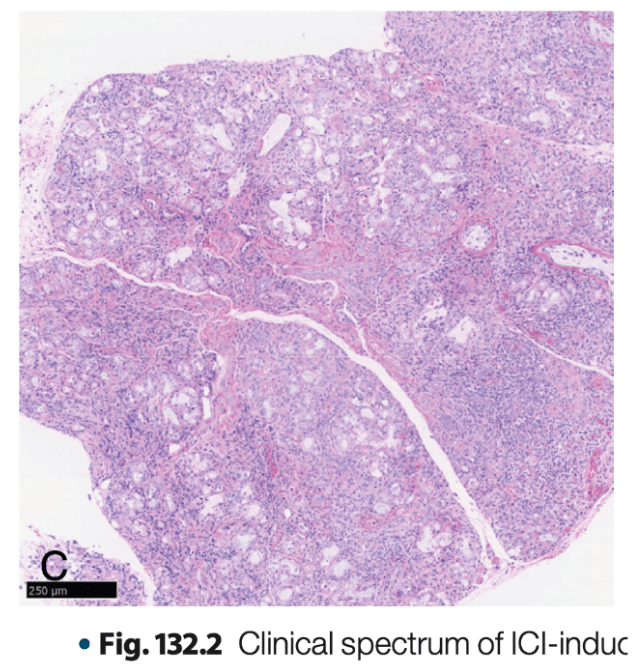
アベルマブ治療中に重篤な唾液腺炎を発症した転移性胸腺癌患者の小唾液腺生検はで、びまん性のリンパ球浸潤があり、広範な腺房細胞の壊死および管上皮の喪失と関連している。これらの病理組織学的所見は、一般的にリンパ球浸潤が限局性で管周囲に存在し、上皮や管上皮の急性壊死が認められないシェーグレン症候群の所見とは異なる (Fig. 132.2C)。
他の珍しい報告
好酸球性筋膜炎は、腕の皮膚肥厚、筋肉痛、MRI上の筋膜浮腫、末梢性好酸球増多を特徴とし、ペムブロリズマブ(PD-1i)治療を受けた患者に発症した(Cancer Immunol Res, 2016.)。
ICI治療でループス腎炎が発症したという症例報告は1例のみ(N Engl J Med 361(2):211–212, 2009)。亜急性皮膚ループスはより広範囲に報告されているが、明確な全身症状を伴わない。
ICI誘発サルコイドーシス様疾患で報告されたほとんどの症例は、肺と皮膚の両方に病変がある(J Am Acad Dermatol 69(5):e272–273, 2013.)
びまん性皮膚病変と限局性皮膚病変を伴う強皮症様皮膚変化の症例が少数報告されているが(Mayo Clin Proc 92(7):1158–1163, 2017.)、これまでに報告されたICI誘発の症例では、全身性硬化症に一致する内臓病変(例えば、間質性肺疾患や肺高血圧症)は認められなかった。
Pearl: 重症筋無力症/筋炎と心筋炎の重複が報告されている。
comment: “ Additionally, patients with myasthenia gravis/myositis overlap and myocarditis overlap have been described (J Dermatol 42(10):1008–1009, 2015).”
irAE筋炎の臨床的特徴(J Autoimmun. . 2019 Jun:100:105-113.)
ICI開始後2-3か月以内に出現、数日~数週の経過で進行
疲労、筋力低下、近位筋の筋痛、眼瞼下垂、球症状、呼吸困難などの症状呈した時に疑う
初発は眼瞼下垂多い
高頻度に眼筋症状(眼瞼下垂・複視)及び顔面筋の筋力低下を認める
四肢近位筋のみならず頸部伸筋を冒し43%で首下がり
MGに似るが易疲労性や日内変動はない
irAE筋炎の治療の第一選択は高用量ステロイド。ステロイド以外の治療として~40%で用いられるのはIVIGまたは血漿交換
心筋炎合併
筋力低下が著明/急速進行性
呼吸不全をきたしている
状況ではステロイドパルスでの治療開始(Arthritis Rheumatol. 2021 May;73(5):866-874.)
Pearl: プレドニゾンの投与量が1日10〜20mg未満であれば、多くの腫瘍医はICIを継続する。患者がより高用量のステロイドを必要とする場合は、ICIを中断されるのが一般的である。ステロイドを低用量に減量できない場合、または4〜6週間で中止できない場合は、他の免疫抑制剤を使用する。
comment: “If a patient is on less than 10 to 20 mg daily of prednisone, many oncologists will often con- tinue the ICI rather than hold it. If the patient requires higher steroid doses, the ICI is typically held. If steroids cannot be weaned to a low dose or off in 4 to 6 weeks, then other immuno- suppressive agents will be used.”
PSL10mg以下に減量できない時には以下のフローでDMARDsを追加します。
炎症性関節炎の治療のフロー(Arthritis Rheumatol. 2021 Apr; 73(4): 553–565.)
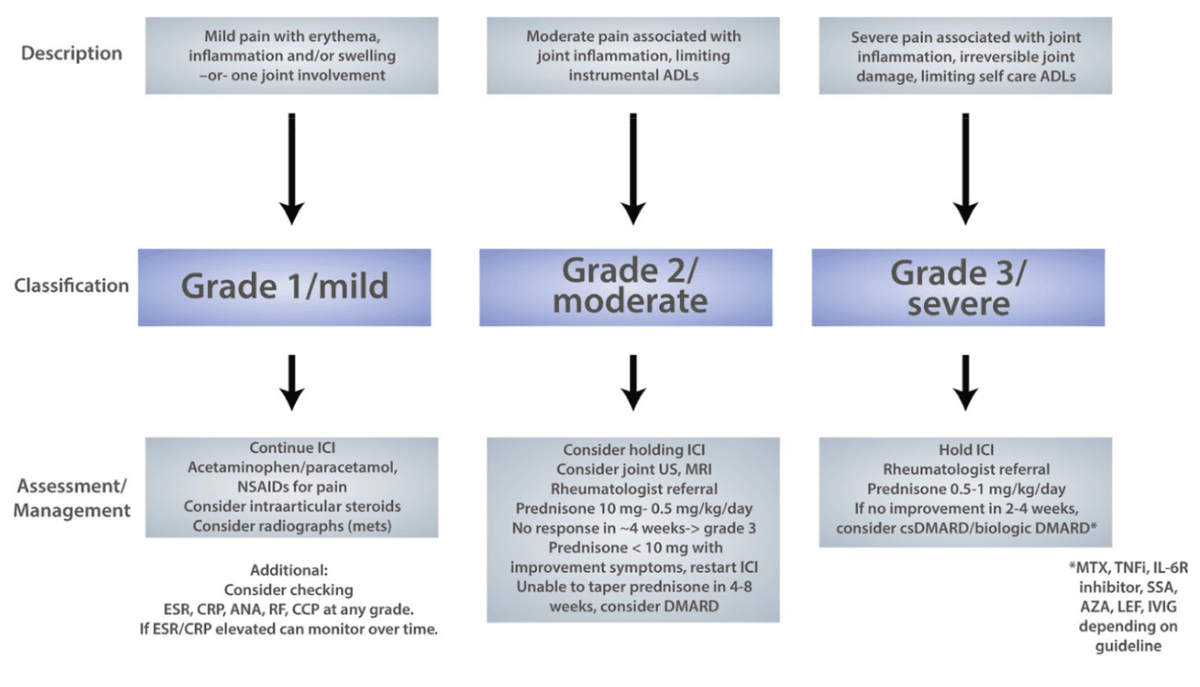
PMRの治療のフロー

Pearl: 免疫抑制によるirAEsの治療は腫瘍反応に悪影響を及ぼすという理論的な懸念がある。しかし、イピリムマブやニボルマブによる治療を受けたメラノーマ患者のirAEsに対する副腎皮質ステロイドやTNF阻害剤による短期療法では、このようなことはないようである。
comment: “There are theoretical concerns that treating irAEs with immuno- suppression will negatively impact the tumor response. This does not seem to be the case for short-term therapy with corticosteroids or TNF inhibitors for irAEs in melanoma patients treated with ipilimumab or nivolumab (J Clin Oncol 33(28):3193–3198, 2015).”
ただICI治療開始時に副腎皮質ステロイドを使用することは有害かもしれない。
NSCLCに対して抗PD-1薬および抗PD-L1薬による治療を受けている患者を対象とした研究では、ベースラインでの1日10mg以上のプレドニゾンの使用は、全奏効率、無増悪生存期間、および全生存期間の悪化と関連していた。
Pearl: 自己免疫疾患の既往がある患者におけるICIの投与では、一般に、PD-1/PD-L1阻害では増悪の割合が高く、CTLA-4阻害ではde novo irAEの割合が高かった。
comment: “In general the rate of exacerbations was higher with PD-1/ PD-L1 inhibition, while the rate of de novo irAEs was higher with CTLA-4 inhibition.”
自己免疫疾患(RA、炎症性腸疾患、乾癬、全身性エリテマトーデスなど)の既往がある患者を対象とした最初のレトロスペクティブ研究は、メラノーマを対象としたもので、イピリムマブ(CTLA-4)で治療した患者30人を対象としたもの(JAMA Oncol 1–7, 2015)と、抗PD-1薬で治療した患者52人を対象としたものであった(Ann Oncol 28(2):368–376, 2017.)。再燃率はそれぞれ27%と38%であり、グレード3以上のde novo irAEはイピリムマブ治療群の33%に発生した。
ただICIの忍容性は一般的に良好であり、再燃が治療中止につながることはほとんどないようである。
