山頂で水を沸かしたら沸点上がるか下がるか、説明できますか?
指導をしていて、意外と抜けてる生徒多いなというテーマについて。水の飽和蒸気圧と沸点のお話です。
本題に入る前に、前提知識の確認を。
そもそも飽和蒸気圧というのはその空気中に存在できるmaxの水蒸気があった時の圧力。言い換えれば、水蒸気の定員のようなものです。もし仮に飽和蒸気圧よりも多くの水蒸気があったならばそれらは飽和水蒸気圧(最大定員)になるまで、水蒸気を液体の水に戻して気体のmol数を減らします。
飽和蒸気圧についてはひとまずこんなイメージを持ってほしくて、これが水の飽和蒸気圧曲線です。温度が上がれば飽和蒸気圧も上がる。要は受け入れられる定員が増えるわけです。
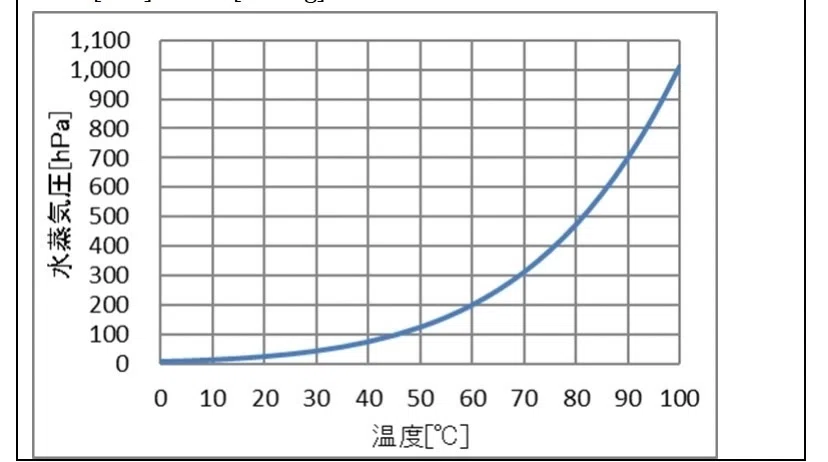
さて、ここでいわゆる沸点、100℃のところを見てほしいのですが、なんとこれが1000hPaとなっており、1気圧、760mmHg、と地上での大気圧と一致しています!!
これは、沸騰という現象が液体内部でできた気泡の圧力が大気圧に打ち勝ったからこそ起こる現象だからです。例えば、地上では90℃の時、液体内部で出現した気泡内の圧力は高々700hPaくらい(要は90℃の時の飽和蒸気圧が700hPa)なので、大気圧(=1000hPa)に負けて押しつぶされます。
ただ、これが100℃になった時、大気圧と真っ向勝負できるようになるのです。これが沸騰という現象。
では、タイトルにある話に進みますが、山頂では大気圧が地上に比べて小さくなっています。富士山頂だったら地上に比べて約3800m分の空気が乗っていないのでその分大気圧が小さいです。つまり、大気圧に打ち勝つのに必要な飽和蒸気圧も低くなる、ということは地上に比べて低い温度で沸騰という現象が起きるのです。
理論化学の範囲は理屈で物事の説明がつくのが魅力の学問です。ぜひ、化学現象を理解して何かの役に立ててもらえたらと思います。
この記事が気に入ったらサポートをしてみませんか?
