
添付文書の電子化?!
どうも、MEです。
皆さん、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)の改正で、添付文書が電子化しなければならないことをご存知でしょうか。
2021年8月からこれまで医薬品などの製品と一緒に同梱されていた紙の添付文書は原則として廃止され、電子的な方法で閲覧することが基本になります。
※一般用医薬品等の消費者が直接購入する製品については、引き続き、紙の添付文書が同梱されます。
改正薬機法が施行される2021年8月以降は、医薬品等が入っている箱につけられたバーコードまたは二次元コードをスマートフォンやタブレットのアプリケーションなどを使って読み取り、その情報をもとにインターネットを経由して最新の添付文書にアクセスし、電子的に閲覧することが基本となります。
ちなみに2023年7月31日までに製造販売された製品においては、経過措置により添付文書の同梱が認められていますが、2023年8月1日以降は消費者が直接購入する製品を除いて、電子的に添付文書を提供することが義務付けられるようになります。
薬機法が改正されることで、常に最新の情報を使って安全対策を行うことが可能になり、医療現場でより安全な治療が可能になるとのことです。
また、箱につけられたバーコード等からは、添付文書の他、審査報告書などの関連文書も閲覧することが可能になります。
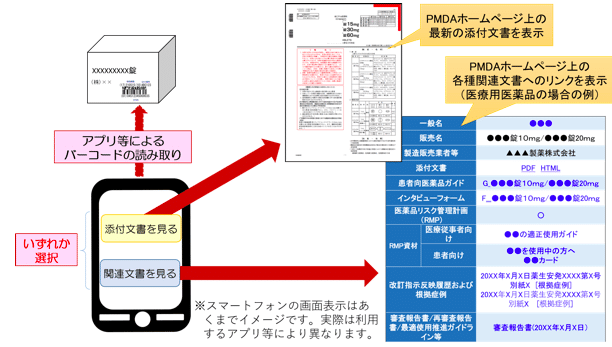
PMDAの具体的な閲覧イメージは上記の通りです。
ちなみに表示される関連文書(案)は以下の通りです。

<添付文書アクセスへの仕組み>
”製品を特定する情報:GTIN14” と ” 添付文書を特定する情報: 添付文書固有の添付文書番号”を紐づけることでアクセスを可能にします。PMDAのデータベースには、各製造販売業社が登録することとされています。
<添付文書電子化によるメリット・デメリット>
メリット① :臨床現場に最新の情報が提供される
メリット② :環境負荷の軽減に貢献できる
デメリット① :利用者によっては情報格差が生じる可能性がある
デメリット② :医薬品の梱包方法や輸送方法を見直す必要がある
電子書籍の普及やタブレット端末の活用など、身の回りでペーパーレス化を実感する機会も増えてきました。今後、添付文書などの公的文書についてもますます電子化が進むことで、よりデジタル格差が広がる可能性も出てきそうです。
どちらにしても学びをやめてはいけないということですね。
興味がある方は医機連でこのようなWebセミナーもやっているので、受講してもらえればと思います。
https://www.jfmda.gr.jp/course/【web配信】「添付文書の電子化」説明会/
<参考>
https://www.pmda.go.jp/safety/info-services/0003.html
https://www.pmda.go.jp/files/000238432.pdf
