バンコマイシンのTDMガイドライン改訂版 (米国版)
2020年3月に公表 (パブリックコメントは昨年12月に募集)された米国病院薬剤師会などによるバンコマイシン (VCM)のTDMガイドラインの改訂版が、CIDにも掲載されています。
VCMのTDMを巡っては、2009年にガイドラインが米国で公表され、AUC/MICが臨床的効果の指標となるが、トラフ値を代替指標とするとし、目標濃度は10〜20 μg/mL (海外では10〜20 mg/Lと表記だが、意味は同じ)とされていました。
今回の改訂は、トラフ値のみのモニタリングでは、有効性が担保されない(代替指標とならない患者群がいること)、副作用の懸念(主に腎機能障害)があることから、AUC/MICをみていきましょうという内容に変更になっています。
また、AUC/MIC>400-600という範囲ですが、MICは1として考える、つまり、AUC>400-600を指標に投与設計しなさいという内容です。
AUCは、実測値で測定しようと思うと、血中濃度の測定が何回も行う必要がある=何回も採血を伴うという事態になります。
このため、ガイドラインでは、2ポイント採血して予測するか、ベイジアン法 (母集団パラメータから推測する方法)を用いて推算しなさいと、推奨をしております。
ソフトウェアは国内では、メーカー作成分を用いてば、AUCを推定可能です。
実は、国内のTDMガイドラインも2021年に改訂予定 (第68回 日本化学療法学会のシンポジウムなどで散々宣伝されていました)で、VCMについては、米国のものと同様の改訂になり、尚且つ、AUC算出可能なソフトウェアまで提供してくれるということです。
ますます、VCMの投与設計などについては、薬物療法の専門家である、薬剤師の活躍が期待をされることと思います。
そういう意味でいうと、今回改訂されたガイドラインについては、意味合いを理解しておく必要があるかと思います。
それでは、本文について和訳したものを記載していきます。
なお、CIDの記事を和訳していますが、ガイドラインの要約になっています。詳細は、米国病院薬剤師会のHPで公表されているバージョンをみていただけると、推奨の理由など、細かな部分も読めるかと思います。
では、本文の和訳に入っていきます。
Therapeutic Monitoring of Vancomycin for Serious Methicillin-resistant Staphylococcus aureus Infections: A Revised Consensus Guideline and Review by the American Society of Health-system Pharmacists, the Infectious Diseases Society of America, the Pediatric Infectious Diseases Society, and the Society of Infectious Diseases Pharmacists
Michael J Rybak, Jennifer Le, Thomas P Lodise, Donald P Levine, John S Bradley, Catherine Liu, Bruce A Mueller, Manjunath P Pai, Annie Wong-Beringer, John C Rotschafer, Keith A Rodvold, Holly D Maples, Benjamin Lomaestro, Therapeutic Monitoring of Vancomycin for Serious Methicillin-resistant Staphylococcus aureus Infections: A Revised Consensus Guideline and Review by the American Society of Health-system Pharmacists, the Infectious Diseases Society of America, the Pediatric Infectious Diseases Society, and the Society of Infectious Diseases Pharmacists, Clinical Infectious Diseases, , ciaa303, https://doi.org/10.1093/cid/ciaa303
抄録
バンコマイシンの薬物動態および薬力学に関する最近の臨床データは、現在の投与およびモニタリングの推奨事項の再評価を示唆している。以前の2009年のバンコマイシンのコンセンサスガイドラインでは、最小阻害濃度(AUC/MIC)までの24時間の曲線下の目標面積の代替マーカーとしてトラフモニタリングを推奨していた。しかし、最近のデータは、トラフモニタリングがより高い腎毒性と関連していることを示唆している。本書は、バンコマイシンの投与とモニタリングに関する新しいバンコマイシンのコンセンサスガイドラインをまとめたものである。これは、米国ヘルスシステム薬剤師協会、米国感染症学会、小児感染症学会、および感染症薬剤師会バンコマイシンコンセンサスガイドライン委員会によって作成された。本コンセンサスガイドラインでは、重篤なメチシリン耐性黄色ブドウ球菌感染症の治療を受けている患者に対して、臨床効果を達成し、安全性を確保するために、AUC/MIC比400~600mg*hour/L(微量希釈法によるMIC 1mg/Lを想定)を推奨している。
EXECUTIVE SUMMARY
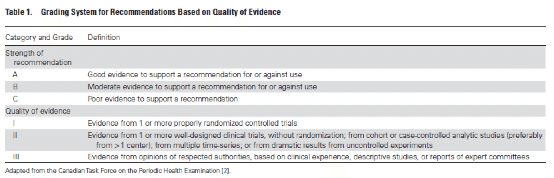
改訂版バンコマイシンコンセンサスガイドライン(バンコマイシンの投与・モニタリングに関するガイドライン)は、米国保健システム薬剤師会、米国感染症学会、小児感染症学会、感染症薬剤師会バンコマイシンガイドライン委員会が作成した2009年のガイドラインを更新したものである。以下は、本書で使用した主要な推奨事項と成績評価システムの要旨である(Table 1、2)[1、2]。


バンコマイシンの臨床使用が61年以上にもわたっているにもかかわらず、治療を最適化し、毒性を最小化するための最も適切なアプローチに関する知識のギャップが依然として存在している。最小阻害濃度比(AUC/MIC)に対する24時間の曲線下面積は、バンコマイシンを含む糖ペプチドの主要な薬物動態/薬力学(PK/PD)目標として文書化されている。2009年の前回のコンセンサスガイドラインでは、治療管理を容易にし、投与量の調整やモニタリングを容易にするために、AUC/MIC(目標400mg*hour/L)の代替マーカーとしてトラフモニター(目標15~20mg/L)を使用することが推奨されていた。当時、特定のトラフモニタリング目標を用いてバンコマイシンの曝露量を増加させる主な理由は、AUC/MIC目標である400mg*hour/Lを達成する可能性を高め、それによって有効性を高めることであった。しかし、これらの推奨事項が実施されて以来、これらの目標値を用いたトラフレベルモニタリングを適用した場合に、成人及び小児における腎毒性が増加したとの報告が多数なされている。最近の PK/PD および毒性力学的研究は AUC/MIC の監視が従来のトラフの監視アプローチと比較して採用されたとき結果を損なうことなくバンコマイシン曝露および nephrotoxicity 率はかなり減少を示した。
AUC/MICを用いた経験的投与を行う場合、微量希釈包、広範な抗菌薬感受性データ、自動感受性検査の不正確さやばらつき(±1 log2希釈)に基づいて、MICは1 mg/Lと仮定すべきである。MIC評価および自動感受性試験に関する具体的な情報は、ガイドライン全文のMIC感受性の項に記載されている[1]。成人および小児におけるメチシリン耐性黄色ブドウ球菌(MRSA)の浸潤性感染症に対しては,臨床的有効性および安全性のデータに基づき,400~600mg*hour/LのAUC目標値が示唆されている。早期かつ適切な治療の重要性を考慮すると,これらのAUC目標は治療の早期(24~48時間)に達成すべきである。重症患者、腎代替療法を必要とする患者、継続的な輸液療法を受けている患者には、実際の体重に基づいた投与量が推奨される。腎代替療法を必要とする肥満患者、および初めて小児患者に対する具体的な推奨事項が、改訂されたガイドラインに含まれている[1]。
バンコマイシンのPK/PDおよび毒性力学に関する利用可能なほとんどすべてのデータは、MRSAの重篤な感染症の治療を受けた患者から得られたものであることに留意すべきである。さらに、データの大部分は複雑な血流感染症の患者から得られたものである。したがって、軽度の非侵襲性感染症やバンコマイシンに感受性のある他の細菌種にこの情報を外挿する際には注意が必要である。これらのガイドラインは、AUC-guided dosing and monitoring が最も正確で安全なバンコマイシンの投与方法であると結論づけている。本書の推奨事項は、バンコマイシン療法を必要とする患者の管理において、健全な臨床的判断を迂回すべきではない。参考文献を含む本文書の各セクションの具体的な詳細は、一次出版物[1]に記載されている。
Table 2の内容(和訳)
Primary Recommendations for Vancomycin Dosing and Therapeutic Drug Monitoring
A. ADULTS AND PEDIATRICS
1. 重篤なMRSA感染症が疑われる、あるいは確定的な重篤なMRSA感染症の患者においては、患者の安全性を向上させながら臨床効果を得るために、AUC/MICBMD比400~600(バンコマイシンのMICBMDを1mg/Lと仮定)の個別目標を提唱する(A-II)。
2. AUC/MICモニタリングに移行する際には、ほとんどの施設でバンコマイシンのMICBMDが1mg/L以下であることを前提に、MRSAによる重篤な感染症が疑われる、または報告されている患者に対しては、保守的にAUCを目標とすべきである。早期に適切な治療を行うことの重要性を考えると、バンコマイシンを標的とした曝露は、治療期間中の早期、好ましくは最初の24~48時間以内に達成されるべきである(A-II)。このように、ベイジアン由来のAUCモニタリングの使用は、AUC目標達成の早期評価を可能にするための定常状態の血清バンコマイシン濃度を必要としないため、このような場合には賢明であるかもしれない。
3. MRSA(A-II)による重篤な感染症患者における有効性と腎毒性のデータに基づいて、15~20mg/Lを目標としたトラフオンリーモニタリングは推奨されなくなった。非侵襲的な MRSA または他の感染症を有する患者において、トラフオンリーまたは AUC ガイド付きバンコマイシンモニタリングを使用すべきかどうかについての推奨を提供するための十分な証拠がありません。
4. バンコマイシンのモニタリングは深刻な MRSA の感染のためのバンコマイシンを投与されている患者のために持続された目標とされた AUC を達成するために推薦される(BMD によってより大きいかより少し 1 mg/L であることが知られていなければ、1 mg/L の MICBMD を仮定する)。MRSA の感染から独立して、vancomycin の監視はまた nephrotoxicity (例えば、同時の nephrotoxins を受け取っている重症の患者)、不安定な(すなわち、悪化するか、またはかなり改善する)腎臓機能の患者、およびそれらの療法の延長されたコースを受け取っているすべての患者のために推薦されます(3-5 日以上)。血行動態的に不安定な患者(例えば、末期腎疾患)では頻繁にまたは毎日のモニタリングが、血行動態的に安定した患者(B-II)では週に1回のモニタリングが賢明かもしれません。
5. 現在のバンコマイシン感受性サーベイランスデータに基づいて、ほとんどの場合、経験的投与の場合、バンコマイシンの MIC は 1 mg/L と仮定されるべきである。MICBMDが1mg/Lを超える場合、従来の投与ではAUC/MIC≧400の目標値を達成できる可能性は低く、高用量投与では不必要な毒性が生じる可能性があり、治療法の変更の決定は臨床的判断に基づいて行うべきである。また、MICBMDが1mg/L未満の場合、AUC/MIC目標を達成するために投与量を減らすことは推奨しない。自動化された感受性検査法の限界として、使用する方法によってMIC結果の精度の低さやばらつきがあることなどに留意することが重要である(B-II)。
6. 連続点滴のPKから、AUC目標が達成できない場合には、このようなレジメンが従来の間欠点滴投与に代わる合理的な選択肢となりうることが示唆されている(B-II)。
7. バンコマイシンやICUで一般的に同時投与される他の薬剤との不適合性は、バンコマイシンを持続的に注入することを検討している場合(A-III)には、独立したラインまたは複数のカテーテルを使用する必要があります。
B. ADULTS
8. 治療効果と最小の AKI のためのバンコマイシンの AUC 範囲が狭いことを考えると、バンコマイシンの投与を管理するための最も正確で最適な方法は、AUC ガイド付きの投与とモニタリング(A-II)によって行われるべきである。
2つの方法のうち1つの方法でこれを達成することを推奨する。
a. 1つのアプローチは、2つの濃度(定常状態付近で得られる、注入後1~2時間後の分布後ピーク濃度と投与間隔の終了時のトラフ濃度)の収集に依存するが、好ましくは同じ投与間隔中には必要ない(可能であれば)、そしてAUCを推定するために一次PKの式を利用する(A-II)。b. AUCをモニターするための好ましいアプローチは、豊富にサンプリングされたバンコマイシンのデータに基づくPKモデルをBayesian priorとして組み込んだBayesianソフトウェアプログラムの使用を含み、少なくとも1つのトラフを有する1または2つのバンコマイシン濃度の収集に基づいて、バンコマイシンのデータを最適化する。ベイズ的アプローチ(A-III)でAUCを推定するために、2個のPKサンプル(すなわち、1〜2時間後の輸液後および投与間隔の終了時)を得ることが好ましい。患者によっては、ベイズ法による AUC の推定にはトラフ濃度のみで十分な場合もありますが、トラフのみのデータを使用することの有効性を確認するためには、異なる患者集団にまたがってより多くのデータが必要です(B-II)。
9. MICBMD1mg/L(A-II)を想定した場合、正常腎機能を有する多くの患者には15~20mg/kg(実体重ベース)を8~12時間毎に間欠的に投与することが推奨されている。腎機能が正常な患者では、MICが2mg/Lの場合、治療上のAUC/MIC目標を達成できない場合がある。
10. 継続的に注入する。現在利用可能なデータに基づき、重症患者に対しては、目標定常状態濃度20~25mg/Lを達成するために、15~20mg/kgのローディング用量を投与し、その後、30~40mg/kgの1日維持CIを60mg/kgまで継続して投与することが検討される(B-II)。AUC24は、定常状態濃度(すなわち、投与間隔全体を通して20~25mg/Lの望ましい治療範囲)に24倍の係数を乗じて単純に算出することができる(B-II)。所望の薬物曝露を達成することは、サンプリング時間および投与量の調整が容易であることを考えると、重症患者において非常に望ましい特徴である輸液速度を変更することによって、より容易に達成され得る(B-II)。
11. 継続的な注入と腎臓毒性を発現するリスクは、それぞれ定常状態濃度 15-25 mg/L とトラフ 10-20 mg/L を目標とする場合、断続的な投与と比較して同様またはより低いようです (B-II)。決定的な研究は、測定された AUC24 に基づいて薬物曝露を比較するために必要とされ、継続的な注入対バンコマイシンの断続的な注入を受けている患者の腎障害薬剤の併用、利尿剤、および/または昇圧剤による治療ような腎機能障害の発現に影響を与える要因。
12. 重篤なMRSA感染が疑われる、または診断された重症患者において、目標濃度を迅速に達成するために、バンコマイシン(B-II)の間欠投与では、20~35mg/kgの負荷量を考慮することができる。負荷量は実際の体重を基準とし、3000mgを超えないようにすべきである。また、肥満患者(B-II)では、より集中的かつ早期の治療モニタリングを行うべきである。
13. 成人肥満。重篤な感染症(B-II)を有する肥満の成人患者では、最大 3000mg の実体重を用いて 20~25mg/kg のバンコマイシン装填量が考慮されるかもしれない。ほとんどの肥満患者に対する経験上の維持用量は、通常、腎機能に応じて 4500 mg/日を超えない(B-II)。特に経験的維持用量が4000mg/日を超える場合には、投与量の調整のために、早期かつ頻繁にAUC曝露のモニタリングを行うことが推奨される(A-II)。
14. 間欠的血液透析。AUC<400mg*h/Lについては有効性のデータがないため、透析前血清濃度をもとにモニタリングを行い、その値を外挿してAUCを推定することが最も実用的である。透析前血清濃度を15~20mg/Lに維持することで、過去24時間のAUCは400~600mg*h/Lとなる可能性が高い(C-III)。透析前の血中濃度のモニタリングは、週に1回以上行われるべきであり、厳密な重量ベースの推奨用量ではなく、その後の投与を促進すべきであるが、これらの推奨用量は、血清濃度が決定されるまでの有用な出発点を提供する(B-II)。
15. ハイブリッド透析療法(例:低速低効率透析)。これらのハイブリッド透析療法がバンコマイシン(B-III)を効率的に除去することを認識した上で、20~25mg/kg(実体重)の負荷量を使用すべきである。透析治療の終了を待つために初期投与量を遅らせてはならない。標準的な血液透析(B-III)と同様に、ハイブリッド透析終了後、または透析の最後の60~90分の間に15mg/kgの維持投与を行うべきである。濃度モニタリングにより、維持投与量の目安とすべきである。
16. 継続的な腎代替療法。従来のKDIGO推奨の排液率20~25mL/kg/hでCRRTを受けている患者には、実体重で20~25mg/kgの負荷量を使用すべきである(B-II)。排水量 20~25mL/kg/h の CRRT の初回維持投与は、12 時間ごとに 7.5~10mg/kg とする(B-II)。維持投与量と投与間隔は、血清濃度のモニタリングに基づいて行うべきであり、AUC/MICの目標値を確実に達成するために、最初の24時間以内に実施すべきである。体液過多の患者では、患者が正常血液量になり、薬剤のVdが減少するにつれて、投与量を減らしてもよい。CRRTを受けている患者におけるバンコマイシンの連続注入の使用は増加しているようであり、バンコマイシンの断続的な投与の代わりに使用することができ、特にCRRTの限外濾過液/透析液の流量が多い場合に使用することができます(B-II)。
C. PEDIATRICS
17. 成人のデータから得られたAUC目標値400mg*h/L(ただし、MICが1mg/L以下と仮定すると600mg*h/Lまで可能性がある)に基づき、正常な腎機能を有し、重篤なMRSA感染症が疑われる小児へのバンコマイシンの初期推奨投与量は、生後3ヶ月以上の小児(A-II)では、60~80mg/kg/日を6~8時間ごとに分割して投与する。
18. 腎機能が十分な小児(C-III)では、通常、経験的に1日の最大投与量は3600mg/日である。ほとんどの小児は一般的に1日3,000mg/日を超えてはならず、AUC/MIC目標を達成するために、観察された濃度に基づいて投与量を調整すべきである。投与量が2000~3000mg/日(A-III)を超える場合は、観察濃度の早期モニタリングを行うことが推奨される。さらに、腎機能が治療開始後5日以内に回復する可能性があるため、腎クリアランスの悪い患者又は腎機能が増強している患者では、観察された濃度及び腎機能の詳細なモニタリングを行うことが賢明である。
19. 新生児から青年期までに記録されたバンコマイシンCLの発達変化に基づいて、好ましくはベイズ推定を用いたバンコマイシンのAUC-guided治療モニタリングが、すべての小児科の年齢層に対して提案されている。現在利用可能なデータに基づいて、小児科における AUC ガイド付きモニタリングの提案は、1 トラフ濃度のベイズ推定の適用、または 2 濃度の 1 次 PK 式(B-II)を含む成人のアプローチと一致しています。ベイズ式AUC誘導投与法は、小児科におけるバンコマイシン療法を個別化するための最適なアプローチであり、年齢、体重、腎機能の違いを考慮することができる。小児科ではバンコマイシンのCLとクレアチニンのCLは常によく相関しているわけではないので、バンコマイシンの血清中濃度と腎機能の両方をモニターすべきである。さらに、MRSA感染症の治療において、目標AUC曝露量を維持し、潜在的なAKIのリスクを減少させるために積極的な投与を行うには、薬物モニタリングが必要である。
20. 小児の重篤なMRSA感染症に対しては、成人(B-III)と同様にバンコマイシン治療後24~48時間以内に治療モニタリングを開始してもよい。治療的モニタリングの遅延は、感染の重症度と臨床的判断に基づいて行うべきである。投与量の調節は腎臓の機能不全、肥満とのそれらのために、または同時に 腎機能障害を発現しやすい薬物療法を受けている、それらのためになされるべきです。初回投与後、急性腎不全を有する者には投与量の調整が重要であるが、その後の調整(特に治療開始から5日以内)は、腎機能の回復を経験している者には必要であるかもしれない。投与量の持続的またはその後の減少は、特に慢性腎不全のある方や、腎毒性のある薬物療法(B-III)を併用されている方に必要となる場合があります。
21. バンコマイシン曝露は、AKI(B-II)を最小化するために、AUCが800mg*h/L、トラフ濃度が15mg/Lのしきい値以下に最適に維持される可能性がある。80mg/kg/日を超えるバンコマイシンの安全性は、プロスペクティブに評価されていない。バンコマイシンの投与量が100mg/kg/日以上の場合は、これらの閾値を超える可能性があるため、投与を避けることが推奨される(B-III)。
22. 非肥満の小児集団における負荷量の推奨の根拠となるデータが不十分である。成人の研究からの負荷量を考慮してもよいが、新生児から青年期(C-III)までの様々な小児集団に対する適切な負荷量を解明するためには、さらなる研究が必要である。
23. 小児肥満。データは、投与量をmg/kgベースで計算した場合、肥満児は正常体重児よりも統計的に大きいバンコマイシン曝露量を有している可能性が高いことを示唆しているが、これらの違いは、現時点では肥満児における異なるmg/kgの経験的バンコマイシン投与量を示唆するのに十分な臨床的重要性を有することは知られていない。非肥満児と同様に、12歳未満の肥満児は、12歳以上の肥満児と比較して、より高いmg/kg用量を必要とする可能性がある(B-II)。
24. 小児肥満。治療的モニタリングは、治療反応とAKIのリスクの両方において、肥満児において特に価値があると思われる。非肥満児における治療的モニタリングの具体的な推奨事項は、肥満児(B-II)にも適用される可能性がある。肥満児(A-III)では、総体重で20mg/kgの負荷量が推奨されている。
25. 新生児。新生児および生後 3 ヶ月までの乳児において AUC 400 mg*h/L(MIC 1 mg/L を想定)を達成するために推奨される用量は、月経後年齢、体重、および SCr(A-II)に応じて、8~48 時間ごとに 10~20 mg/kg の範囲である。
いいなと思ったら応援しよう!

