
日本におけるドラッグ・ラグ
2024年にFDAで承認された新薬のまとめの記事を作成している際に、KEGG DRUG Databaseに日本(PMDA)、アメリカ(FDA)、ヨーロッパ(EMA)からの承認について整理されているのを発見しました。https://www.genome.jp/kegg/drug/br08328.html
今回の記事では、このサイトに記載されているデータをもとに、日本の「ドラッグ・ラグ」について簡単な分析を行いたいと思います。リストの中には1,052個の医薬品が記載されています。
日本、アメリカ、ヨーロッパの全てで承認されている医薬品:363個
アメリカのみで承認されている医薬品:265個
ヨーロッパのみで承認されている医薬品:31個
日本のみで承認されている医薬品:94個
アメリカのみで承認されていない医薬品:23個
ヨーロッパのみで承認されていない医薬品:106個
日本のみで承認されていない医薬品:170個

これらの結果、以下のような傾向が明らかになりました:
全ての地域(USA、Europe、日本)で承認されている医薬品
全体の35%がすべての地域で承認されており、この数字は意外と高いと感じる方もいるかもしれません。
日本で承認されていない医薬品
45% (265+31+170=466個)が日本で未承認です。
ヨーロッパで承認されていない医薬品
44%(265+94+106=465個)がヨーロッパで未承認です。
アメリカで承認されていない医薬品
14%(31+94+23=148個)がアメリカで未承認です。
日本で未承認の医薬品は確かに多いのですが、ヨーロッパと大きな違いはありません。ただし、以下の要因がドラッグ・ラグの印象を強めている可能性があります:
1. 「日本のみ承認」の薬物がヨーロッパより多い
• 日本: 全体の8.8%
• ヨーロッパ: 全体の3.0%
2. 「日本のみ未承認」が「ヨーロッパのみ未承認」より少ない。
• 「日本のみ未承認」: 16.3%
• 「ヨーロッパのみ未承認」: 10.1%
この差は、日本が独自の医療ニーズや規制に基づいた承認を行っていること、日本の承認プロセスが他の市場に比べてグローバル化されていないことを反映している可能性があります。
ただし、アメリカやヨーロッパと比べ、日本は人種の多様性が著しく低い(大半を東アジアの人々が占めています)ことから、「日本のみ承認」「日本のみ未承認」が多くなるのは合理的であり、PMDAの慎重さは妥当であるとも考えられます。
次に、日本、アメリカ、ヨーロッパの全てで承認されている363個の医薬品に注目して分析を行います。
FDA(アメリカ)の承認からPMDA(日本)の承認までの日数とFDA(アメリカ)の承認からEMA(ヨーロッパ)の承認までの日数を計算すると、
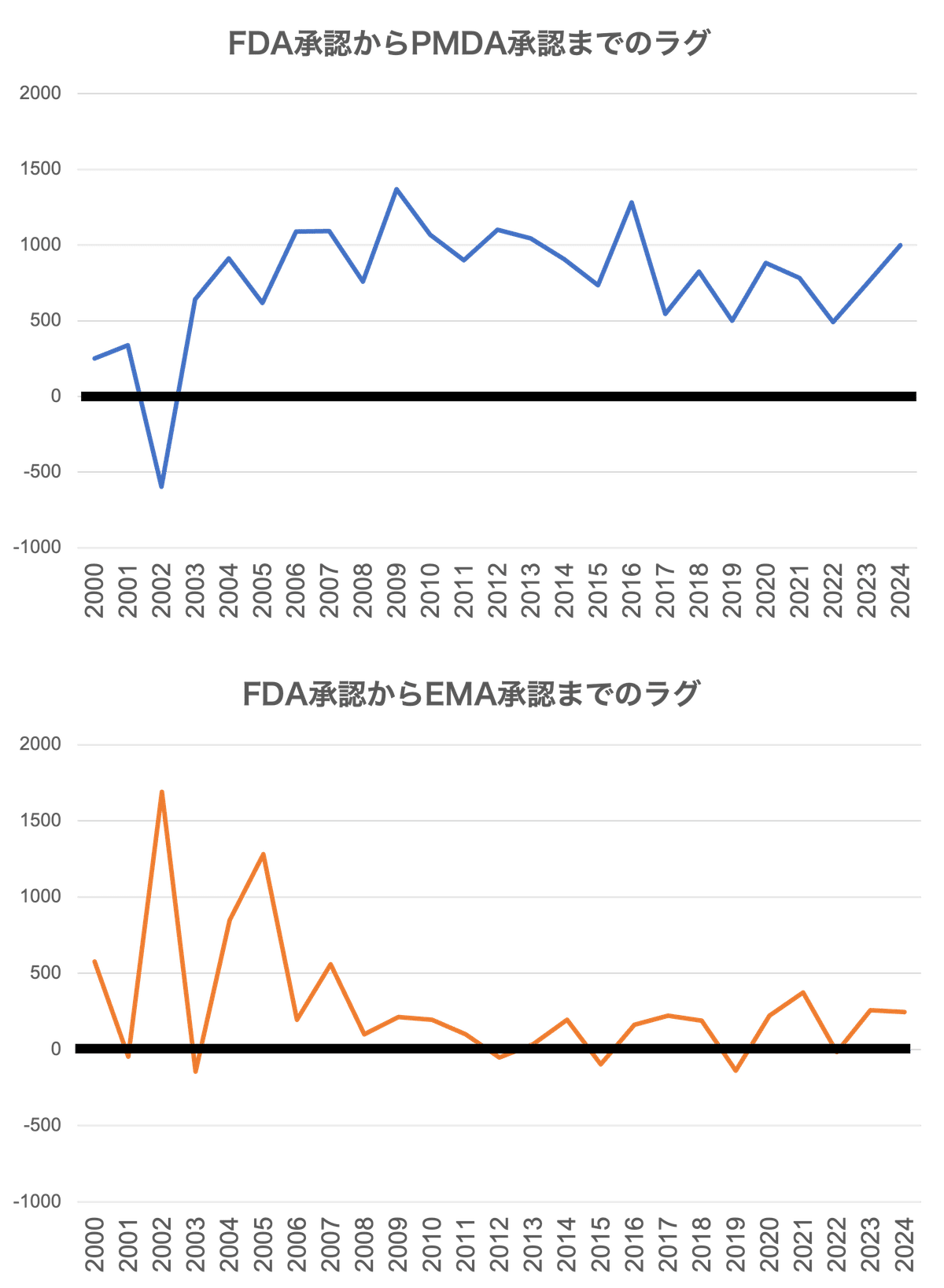
このようになっています。
アメリカで承認されてから日本で承認されるまでの日数、いわゆるドラッグ・ラグは2000年代前半から大きく増えています。2010年代に入ってラグはやや減少していますが依然として2年以上の「ラグ」が存在することがわかります。
一方、アメリカとヨーロッパのドラッグ・ラグは縮小傾向で、1年程度しか存在しません。
日本におけるドラッグ・ラグが強く意識される背景には、2002年のイレッサ事件が影響を与えていると考えられます。この事件は、日本が世界に先駆けて承認したEGFR阻害薬イレッサが、アジア人特有の薬物反応性を考慮しきれず、多くの致死的な間質性肺炎の症例を引き起こしたものです。
医薬品の承認には有効性だけでなく、安全性にも十分配慮する必要があります。「絶対安全」な医薬品はこの世に存在しませんが、PMDAが慎重な姿勢を崩さないのは日本人の「絶対」を求めがちな考え方に起因するのかもしれません。
いいなと思ったら応援しよう!

