
環境計量士(環境計量に関する基礎知識(化学))
濃度と合わせて30点を取ることを目指しましょう。
最初5問は環境基本法、大気汚染防止法、水質汚濁防止法をメインに出題されます。公害防止管理者で見たような感じです。
その後は高校化学の内容に加えて大学化学の内容が含まれています。
環境計量士を受けるような人が高校化学の内容を履修していないとは思いませんが、大学化学の内容は知らない人も多いかと思います。
法律系のやつはともかく、化学系のものについては高校化学履修者向けの説明を記載したところがいくつかあります。
講義らしいところは小見出しにしてあります。正確な書き方じゃないことも多いですが試験用です。
濃度は知識というかJISの暗記ゲーみたいになってるので化学と濃度のどちらで多く点数を取るのかは考えた方がいいかもしれません。
濃度はこちら
平成30年

答え 1
そのまま

答え 2
第2条 この法律において「ばい煙」とは、次の各号に掲げる物質をいう。
1燃料その他の物の燃焼に伴い発生するいおう酸化物
2 燃料その他の物の燃焼又は熱源としての電気の使用に伴い発生するばいじん
3物の燃焼、合成、分解その他の処理(機械的処理を除く。)に伴い発生する物質のうち、カドミウム、塩素、弗化水素、鉛その他の人の健康又は生活環境に係る被害を生ずるおそれがある物質(第一号に掲げるものを除く。)で政令で定めるもの

答え 5
第1条 この法律は、工場及び事業場における事業活動並びに建築物等の解体等に伴うばい煙、揮発性有機化合物及び粉じんの排出等を規制し、水銀に関する水俣条約(以下「条約」という。)の的確かつ円滑な実施を確保するため工場及び事業場における事業活動に伴う水銀等の排出を規制し、有害大気汚染物質対策の実施を推進し、並びに自動車排出ガスに係る許容限度を定めること等により、大気の汚染に関し、国民の健康を保護するとともに生活環境を保全し、並びに大気の汚染に関して人の健康に係る被害が生じた場合における事業者の損害賠償の責任について定めることにより、被害者の保護を図ることを目的とする。

答え 4
シアン化合物は2, 六価クロム化合物は5, 四塩化炭素は12, ベンゼンは22
公害防止管理者を受けたときはだいたい危なそうなものが有害物質という覚え方でした。まあヒドラジンも毒物ですが


答え 3
そのまま

答え 3
ベンゼン環の反応
さて大学化学の話を始めましょう
ベンゼン環についている水素原子を何かに置き換える反応を置換反応と言います。硝酸硫酸で水素がNO₂のニトロ基に置換されることは高校でも習います。で、この置換反応は①求電子置換反応 ②求核置換反応の大きく分けて2種類あります。
求電子というのは字の通りで「電子を求める」反応です。どういうことかというとベンゼン環の中でも「電子な豊富な場所」で反応したがるということです。「いや電子が豊富な場所ってどこだよ」となると思いますが、ただのベンゼン環であれば水素が6つついてる対称な形をしているので、電子に偏りはありません。ただ、今回はXとしてHとは違う何か変なものがついています。Xが電子をベンゼン環側に押し出すような、「電子供与性」と呼ばれる性質を持ってる場合はXの両隣(オルト位)とXの反対側(パラ位)が電子が豊富な場所になります。
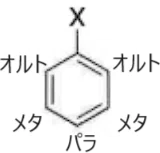
オルト位じゃなくてメタ位の方が物理的に近いじゃないかと思うところですが、物理的に近いというよりベンゼン環は仕様上2つ隣がセットみたいなものなので、オルト位とパラ位が電子が豊富になります。これをオルトパラ配向性と呼んでいます。
ただし、この電子吸引電子供与以外にも、そもそもこのX自体が正か負かという要素も強く影響します。電子吸引だと言ったところでXに電子が元々たくさんあるならむしろ全体としては電子が豊富みたいなこともあるということです。
結果的には
電子供与性→アルキル, OH, OやNHで始まるもの,
電子吸引性→ハロゲン、メタ配向性組、ベンゼン環
オルトパラ配向性→ハロゲン、アルキル、OやNHで始まるもの,
メタ配向性→COやCNの組み合わせ
(例外はあります)
ハロゲンがやや変な立ち位置になっています
とりあえずなんとなく全体像が分かったところでじゃあ今回の反応は何反応なのかの話です。とはいえ実質暗記に近いです。
-NO₂やアルキル、すなわちCH₃とかCH₂CH₃(Rと略されます)や、ハロゲンことX, SO₃Hことスルホン化は求電子置換反応です。
これらを踏まえて今回の問題の話をすると
ニトロ化反応は求電子置換反応なので電子が多いところで反応する
1のX=CH₃はアルキルなのでオルトとパラが多いです。
2のX=COOCH₃はCOではじまるのでメタが多い
3のX=NHCOCH₃はNHなのでオルトパラ
4のX=Clはハロゲンなのでオルトパラ
5のX=CF₃はメタです(上にはないですが)

答え 2
共役酸
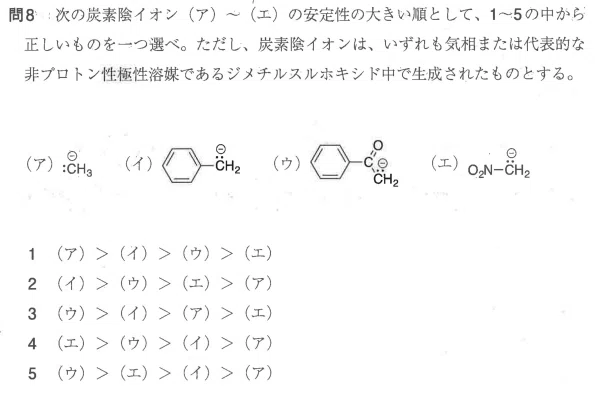
アミンはご存知でしょうが共役酸とはなんでしょうか
共役酸というのは要はH⁺がついたものです。例えばイのNH₃の共役酸はNH₄⁺です
でpKa=-logKaの値の大小はどのように見ればよいのか。そもそもpKaというのはpHみたいなもので、値が小さいと酸性、大きいと塩基性です。
考え方として、NH₂(NH₃)の開いている部分にH⁺がつくわけですが、Hのつくための空いている部分にある電子が強ければH⁺がたくさんつきます。であれば、水溶液としてはOH⁻がたくさんできるので塩基性というわけです。

電子が強い(正確には非共有電子対の濃度が高い)ってなんだよって話ですが、「ベンゼン環の反応」で説明した電子供与性/電子吸引性というものをここでも使います。
アはCH₃CH₂がアルキルなのでR-NH₂なのですが、Rは電子供与性です。
であればこのNH₂の部分は普通のNH₃よりは電子が多くて強そうです。
となれば↑でいった通り塩基性が強いということになるので、pKaも大きいです。なのでア>イになります
次にイとウですが、ベンゼン環は電子吸引性なのでさっきと逆になります。よってイ>ウ
ウとエはClの差です。ハロゲンは電子吸引性なので塩基が弱く、ウ>エ
エとオは同じ電子吸引性ですが、Clの方が強いのでエ<オ
オとカも同じですが、NO₂の方が強いのでオ>カです
答え 4
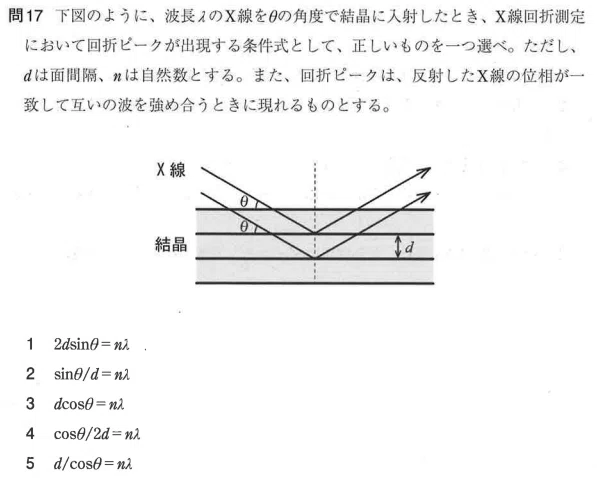
イオンの安定性
イオンが安定しているとはどういうことでしょうか
これは「電子が非局在化している」が答えです。
電子が非局在化しているというのは電子の位置がいろいろ動けるという意味です
下の画像みたいに書き換えられる奴は電子が非局在化しているという扱いです。

逆にアのようなやつは書き換えようがないので局在化しており、不安定です。
アが一番不安定で、次はベンゼン環がある分少しマシなイ、次が↑に書いたウで、一番安定なのがNO₂で2つとCH₂側1つの計3つ記載できるエです。

答え 3
3はNG。分解したらもう塩化ナトリウムじゃないですが…

答え 5
リチウムは金属なので水素化リチウムLiHは共有結合というよりイオン結合です。

答え 2
D=Ce/Cwに代入します。
Cw=W/Vwで、ジエチルエーテル側の質量はW-W₀なのでCe=(W-W₀)/Veです
あとは変形するだけ

答え 4
混成軌道
メタンCH₄は四面体、アセチレンHC≣CHは直線みたいな話がありますね
すごく省略して言うとこれの言い換えとして、四面体になるものがsp₃混成軌道、平面になるものがsp₂混成軌道、直線になるものがsp混成軌道です。
さらに雑に言うなら単結合がsp₃混成軌道、二重結合がsp₂混成軌道、三重結合がsp混成軌道です。
今回だと平面をとるのはベンゼン環の6つの炭素なので6個です。

答え 4
また有機化学ですね
アのアルドール反応というのはアルデヒドかケトンが合体するもので
アセトアルデヒドだとCH₃CHO+CH₃CHO→CH₃CH(OH)CH₂CHOみたいになります
カルボン酸ではないのが分かるかと思います
イのGrignardですが、これはCH₃COCH₃みたいになっているCOのところに、いい感じのアルキル(R)をくっつけて真ん中のCの4本の手にCH₃が2つとOHとそのRがくっつくような第3級アルコールを生み出すものです。
知識がすべてみたいなところですが無水エーテル中で行います
ウのクレメンゼン還元はイと少し似ていてCH₃COCH₃みたいになっているCOのところをCH₃CH₂CH₃とO部分を消し去る(ケトン→アルカン)もので、酸性条件下で行います
エのCannizzaro反応はCH₃COHをCH₃OHとCH₃COONaみたいにアルデヒドを強塩基で処理するとアルコールが出てくるというものです。記述は正しいです。

答え 1
白川英樹は導電性高分子(ポリアセチレン)の発見でノーベル化学賞を2000年に受賞しています
ケクレはベンゼンの構造式の発見。ケクレ構造って言いますよね
桜田一郎はビニロン合成。1939年に現在の京大で発明してます。
オストワルトは硝酸の製造。オストワルト法(NH₃+2O₂→HNO₃+H₂O)は非常に有名。

答え 4
蒸発熱の単位がkJ/molで蒸発エントロピーの単位がJ/(K・mol)なことを思えば蒸発熱を沸点で割ればよさそうですね
39.3kJ/mol ÷ (78.3+273.15) K ≒ 111.8J/(K・mol)

答え 1
2 アンチノック剤はテトラエチル鉛やテトラメチル鉛で、酢酸鉛ではありません。
3 有機水銀が人体が無害なはずがありません。
4 酸化クロム(Ⅲ)なんて大した酸化力はありません。酸化クロム(Ⅵ)CrO₃は強く、めっき液にも使います。要は六価クロムがだめという話
有名なニクロム酸カリウムK₂Cr₂O₇と同じく六価クロム仲間です。
5 硫化カドミウムはカドミウムイエローです。水には難溶です。
おそらくこの文書は硫酸カドミウムの記述です。
答え 1
ブラッグの法則です。

答え 3
地殻は酸素50%弱、ケイ素30%弱、アルミニウム10%弱です。炭素なんて0.02%くらいです。
地殻に炭素が大量なら火が付いたとき大変なことになるでしょう

答え 3
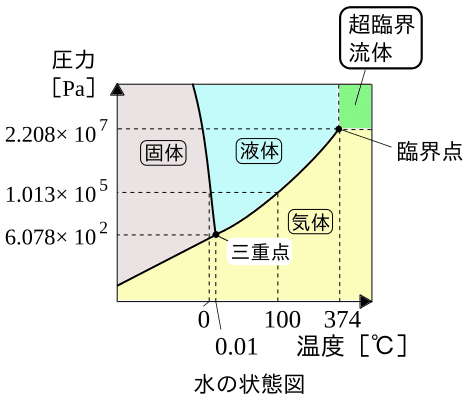
水は↓の状態図にあるように圧力を上げると融点が下がります。

答え 2
ミラー指数
立方体の中で4点をうまく取って結べば面が出来上がると思います。
これを誰かと共有する場合はどのように説明したらよいでしょうか
座標なんかを使って説明するのがいいような気はしますが、
結晶の世界ではミラー指数というのが使われます。
問題にabcとxyz軸みたいなものが書いてありますが、このabc軸との交点を持ってきて、逆数をとって、最小公倍数をかけて整数にするとミラー指数です。
ただ今回はa=1, b=1, c=∞なので、1/1=1と1/∞→0ということで(1,1,0)です

答え 3
C : 2x=y
O : 8+4x+12=8+4+2y+z
H : 2x+6=2z
これらを解くと(x,y,z)=(5,10,8)なので5+10+8=23

答え 4
ア : 水酸化銅は沈殿します
イ : 反応がそもそもありません
ウ : 炭酸カルシウムは沈殿します
エ : 臭化銀は沈殿します
オ : 水酸化鉄は沈殿します

答え 5
ダニエル電池の正極は銅で、負極は亜鉛です。
そしてそもそも電池において正極は電子を受け取る側なので還元反応が起きます。
CuとZnのどっちが2+の形になりやすいかと言えば当然Znなのですよ
標準起電力は-0.763Vと+0.337Vの差である1.10Vで、最初期はこの値よりも大きい起電力を示します。

答え 2
CH₄+2O₂→CO₂+2H₂O
2C₂H₂+5O₂→2CO₂+2H₂O
C₃H₈+5O₂→3CO₂+4H₂Oなので
メタンの必要酸素量は1/16 × 2 =1/8 mol
アセチレンは1/26 ×2.5 = 5/52 mol
ブタンは1/44 × 5 =5/44 mol
比較するとメタン(0.125mol)>ブタン(0.114mol)>アセチレン(0.096mol)

答え 5
(毎回書くのは面倒なので)³⁵ClをA, ³⁷ClをBとすると塩素分子はA:B=3:1なので、(A₁A₂A₃B₁)×(A₄A₅A₆B₂)の組み合わせに等しい。
A₁A₄, A₁A₅, A₁A₆, A₂A₄, A₂A₅, A₂A₆, A₃A₄, A₃A₅, A₃A₆の組み合わせが9個、
A₁B₂, A₂B₂, A₃B₂, A₄B₁, A₅B₁, A₆B₁が6個、B₁B₂が1個なので9:6:1
いやまあ3²:₃C₁×1×2:1²=9:6:1ですよ
令和元年

答え 2
第16条 政府は、大気の汚染、水質の汚濁、土壌の汚染及び騒音に係る環境上の条件について、それぞれ、人の健康を保護し、及び生活環境を保全する上で維持されることが望ましい基準を定めるものとする。

答え 4
そのまま

答え 2
第15条 都道府県知事は、いおう酸化物に係るばい煙発生施設で季節により燃料の使用量に著しい変動があるものが密集して設置されている地域として政令で定める地域に係るいおう酸化物による著しい大気の汚染が生じ、又は生ずるおそれがある場合において、当該地域におけるいおう酸化物に係るばい煙発生施設において発生するいおう酸化物を大気中に排出する者が、当該ばい煙発生施設で燃料使用基準に適合しない燃料の使用をしていると認めるときは、その者に対し、期間を定めて、燃料使用基準に従うべきことを勧告することができる。

答え 3
そのまま

答え 1
第1条 この法律は、工場及び事業場から公共用水域に排出される水の排出及び地下に浸透する水の浸透を規制するとともに、生活排水対策の実施を推進すること等によつて、公共用水域及び地下水の水質の汚濁(水質以外の水の状態が悪化することを含む。以下同じ。)の防止を図り、もつて国民の健康を保護するとともに生活環境を保全し、並びに工場及び事業場から排出される汚水及び廃液に関して人の健康に係る被害が生じた場合における事業者の損害賠償の責任について定めることにより、被害者の保護を図ることを目的とする。

答え 2
解説が困難である旨の解説があったので貼っておきます
https://peing.net/ja/q/8d7e368d-9fde-43eb-8855-e6fda8cbba53

答え 2
緩衝液(追記)
緩衝液というのは少量であれば強酸や強塩基を加えてもpHがほとんど変化しない液体のことです。高校化学でも性質の紹介くらいはされています。
大学化学の範囲ですが、この緩衝液のpHを求めるにはHenderson-Hasselbalchの式を使います。pH=pKa + log₁₀[A⁻]/[HA]
CH₃COOH + NaOH →CH₃COONa + H₂Oで等モルの反応なので、この反応後の酢酸のモル濃度は0.10mol/L × (75-25)m = 5mmol
酢酸イオンのモル濃度は10mmolなのであてはめると4.75-0.30=4.45です


答え 3
[Mg²⁺][OH⁻]²=1.0×10⁻¹¹で[Mg²⁺]=1.0×10⁻³なら[OH⁻]=1.0×10⁻⁴です
((11-3)÷2)だったら[H⁺][OH⁻]=1.0×10⁻¹⁴だし[H⁺]=1.0×10⁻¹⁰でpH=10ですね

答え 5
ベンゼンはC-C=C-…みたいになっているのでC1つあたりだと3個でしょというもので、グラファイトやダイヤモンドは4個で、ポリエチレンはC-C-C-C-…なので2個、O=Oは当然2個だしO₃は3個です

答え 3
国語かな
1 質量分率なので質量÷質量が基本
%というのは基本的に同じ単位のものを割り算するものですよ
2 物質量濃度は物質量÷体積
3 mol/L ÷ g/molならg/LなのでOK
4 mol÷molで単位的にはOKですが考え方が間違い。物質量分量は溶質物質量÷溶媒中に含まれる物質の物質量の合計
5 混合前なら同じです

答え 2
アはOが-2なことを思えば x-8=-2よりx=6
イはCOが分子で0なので-2
ウはBrが-1なのでx-4=-2よりx=2
エはCNが-1なのでx-3=-2よりx=1
CNが-1なのはHCNが分子で、Hが+1ならCNは-1という話です

答え 4
Grignard試薬は完全に大学有機化学
R-MgXと書くので答えはマグネシウム

答え 1
ブタジエンゴムは有名 スチレンを混ぜることも多い
生分解高分子といえばポリ乳酸
有機溶剤は残り二つで見たらジエチルエーテル 吸わないように
解熱鎮痛剤はアセチルサリチル酸 要はアスピリン
4つとも高校化学の範囲でした
答え 5
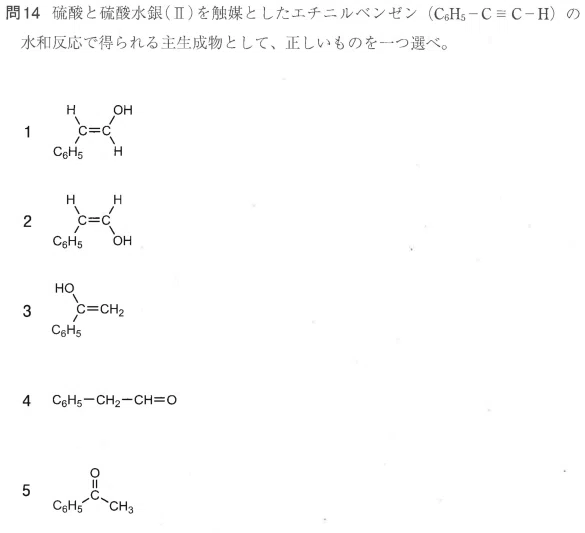
三重結合に水を添加する水添反応について
アセチレン(HC≡CH)の場合はビニルアルコール(CH2=CHOH)になるところ、不安定だからアセトアルデヒド(CH3COH)になるのでした

答え 2
双極子モーメントというのは難しいところですが、ベクトルの考え方が近いです。H₂SはH-S-Hみたいな結合ですが、このHSHの位置関係は直線ではなく、角度的には92°くらいです(問題では90°)。で、S-Hの結合をxで表すとS-Hが2個あるのでこれを合成した長さの√2xがこの分子の双極子モーメントと呼ばれるものになります。
なので√2x=3.2×10⁻³⁰でこれを解くとよいです。


答え 1
水なのでp=1, T=373を代入してAを求めて変形しましょう

答え 5
その通りです
4は「うん?」と思ったかもしれませんが、電離度の関係でpH1.0にはならず2.0弱くらいです。

答え 4
アは昇温だ吸熱だ言ってる時点で示差熱でしょう
イはX線のどっちかですが、回折は結晶の用語で、光電子分光は電子の状態を見るものです。
答え 3
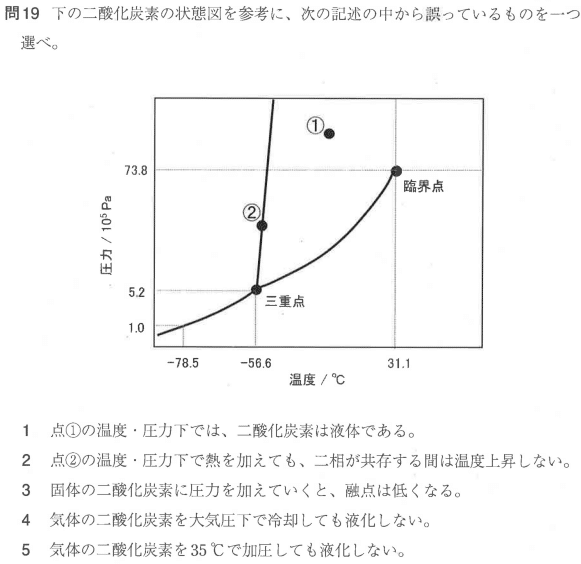
融点は②の点のある部分の線です
グラフを見ていると圧力を上げれば上げるほど温度が少しずつ上がっているので融点も高くなっています

答え 2
ケイ素は共有結合ですね

答え 2
1はイオン化エネルギー 電子親和力は電子を取り込むときのもの
2はその通り ちょっと核から最外殻電子が遠いしね
3は実際そんなことはないという話
4は第3周期だと逆になります。
5も逆。まあ余分なものがついてるんだし

答え 5
双極子モーメントはH₂Sのときにベクトルがどうとか言いましたが、永久双極子モーメントもにたようなもので、きれいな形をしていると打ち消しあってなくなる、変な形をしていると存在するものです
NH₃は三角錐で永久双極子モーメントがありますが、BF₃は正三角形なので打ち消しあってなくなります。
CO₂も直線なのでなし、CH₄は正四面体でなし、H₂OはH₂Sのように折れ線なのでありです
なんとなく感覚が分かりますでしょうか

答え 4
そもそも4,5くらいしか水に溶けません
5は溶けますがイオンじゃないので電気伝導率は4ほどじゃありません
4は硝酸ができるしH⁺とNO₃⁻になります

答え 1
1はその通り 知識みたいなものですが
2はナトリウムエトキシドができますね
3はエタノールのOが非共有電子対持ち
4はヘキサンは水に溶けない
5はヘキサン86でエタノール62ですよ

答え 2
半減期
突然放射性物質が出てきた
半減期というのは文字通り元の量から半分になる期間ということで、半減期が4年なら4年で半分になるということです
で、この減少量というのは直線的ではありません。
どういうことかというと4年で半分だからと言って1年で1/2×1/4=1/8だけ減るというわけじゃないということです。1/8だけ減るなら8年で0になりますからね。正解は8年で1/2×1/2=1/4になるのです
半減期というかこの減衰は指数関数の形の数式があるのですが、半減期だけなら半減期の半分の期間で1/√2≒0.71になることを覚えておいた方が環境計量士の計算的には有利です

Aは半減期4年で6年たったのでまず4年で1/2, 追加の2年で1/√2になるので1/2√2になっています。
Bは半減期3年なので、2回半減期を迎えたということで1/4です
この比をとればB/A=2√2/4=1/√2≒0.71です
昔は範囲外だったので一応項目作って書きましたが、
半減期やらは今の高校の化学基礎の範囲ですよ
令和2年

答え 4
第2条
2 この法律において「地球環境保全」とは、人の活動による地球全体の温暖化又はオゾン層の破壊の進行、海洋の汚染、野生生物の種の減少その他の地球の全体又はその広範な部分の環境に影響を及ぼす事態に係る環境の保全であって、人類の福祉に貢献するとともに国民の健康で文化的な生活の確保に寄与するものをいう。

答え 1
第4条 法第2条第17項の政令で定める物質は、次に掲げる物質とする。
1 一酸化炭素
2 炭化水素
3 鉛化合物
4 窒素酸化物
5 粒子状物質

答え 5
第18条の12 特定粉じん排出者は、環境省令で定めるところにより、その工場又は事業場の敷地の境界線における大気中の特定粉じんの濃度を測定し、その結果を記録しておかなければならない。

答え 2
第3条 法第2条第2項第号の政令で定める項目は、次に掲げる項目とする。
1 水素イオン濃度
2 生物化学的酸素要求量及び化学的酸素要求量
3 浮遊物質量
4 ノルマルヘキサン抽出物質含有量
5 フエノール類含有量
6 銅含有量
7 亜鉛含有量
8 溶解性鉄含有量
9 溶解性マンガン含有量
10 クロム含有量
11 大腸菌群数
12 窒素又は燐りんの含有量(湖沼植物プランクトン又は海洋植物プランクトンの著しい増殖をもたらすおそれがある場合として環境省令で定める場合におけるものに限る。第4条の2において同じ。)

答え 3
第15条 都道府県知事は、環境省令で定めるところにより、公共用水域及び地下水の水質の汚濁(放射性物質によるものを除く。第17条第1項において同じ。)の状況を常時監視しなければならない。

答え 4
2n²なのでn=4を代入して32

答え 4
硝酸銀と塩化ナトリウムが反応して塩化銀と硝酸ナトリウムができます
同体積の2液を混ぜた場合、体積が2倍になるので混ぜた直後は濃度が半分なことと、塩化ナトリウムが過少なことを考えると、硝酸銀が0.10mol/L,
塩化銀と硝酸ナトリウムが0.005mol/Lとなることがわかります。
硝酸銀はほぼ電離するので硝酸銀からの[Ag⁺]は0.10mol/Lですが、
塩化銀は微妙です。これをx[mol/L]とすると[Ag⁺]=0.10+x, [Cl⁻]=xです
[Ag⁺][Cl⁻]=1×10⁻¹⁰に代入して解けば答えの通りです。

答え 3
KMnO₄とH₂O₂は2:5であると式から読み取れます。
KMnO₄が0.100×12.0=1.2mmolならこの5/2である3.0mmolのH₂O₂が必要ということで、20×x[mol/L]=3.0よりx=0.150mol/Lです

答え 1
1はCOの電子数が6+8=14, CN⁻が6+7+1=14個でOK
2はCO₂が6+8×2=22, NO₂⁻が7+8×2+1=24個でNG
3はCO₃²⁻が6+8×3+2=32, NF₃が7+9×3=34
4はC₂H₆が6×2+6=18, B₂H₆が5×2+6=16
5はCS₂が6+16×2=38, SiO₂が14+8×2=30

答え 1
ア ダニエル電池の負極は亜鉛で正極は銅
イ マンガン乾電池の負極は亜鉛で正極は二酸化マンガン
ウ 鉛蓄電池の負極は鉛で正極は二酸化鉛
エ リン酸形燃料電池の負極は水素で正極は酸素
答え 3
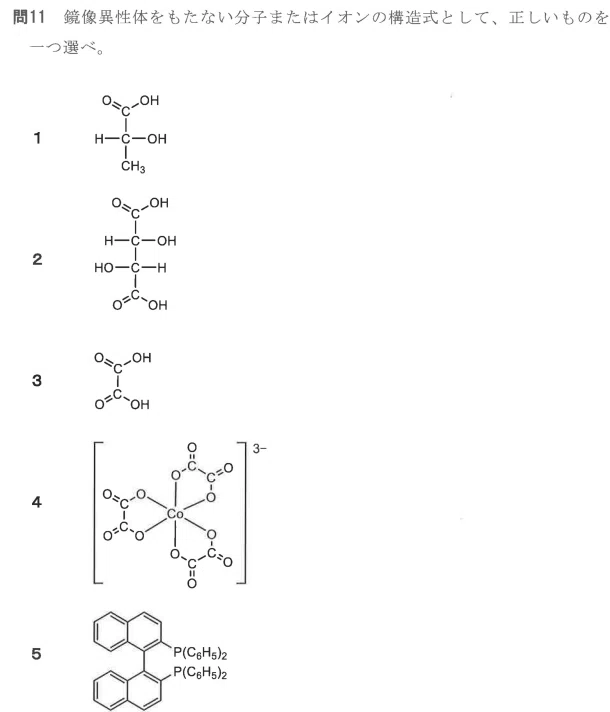
鏡像異性体、つまりくるくるまわしても決して同じ形にできないような異性体があるかどうかの話
正直書くのは大変なのですが、1の真ん中の炭素のように4本の手にくっついているものがすべて違う物であればそれを不斉炭素と呼び、鏡像異性体があると判断できます。2の上から2つ目の炭素もそうですね
4,5あたりになるともはやよくわかりませんが、3は不斉炭素がないのでこれが正解

答え 2
アルキルの長さと水素がフッ素になったらどうなるかという物
Fは特に負で、電子吸引性が非常に強いです
するとどうなるかというと後ろのCOOHのHはCH₃のときよりも簡単に遊離する、つまり水中にH⁺が増えて酸性が強くなります
そしてCF₃COOHの方がCF₃CH₂COOHよりもCOOHに近いので強いとなれば
イ>エ>アが決まるので2となってます

答え 3
「ベンゼン環の反応」を参照
OHがオルトパラ配向なので3です
オルトとメタとかメタとパラ、オルトだけ、パラだけというのはまずないので実質2,3の2択ですよ

答え 5
CH₂=CH-CH=CH₂+CH₂=CH₂で何ができるのか
環になるのですが、まあ二重結合が1つ残るので5になります
そういう物って思った方がよい

答え 4
H₂→2H⁺+2e⁻とO₂+4H⁺+4e⁻→2H₂Oで、
H₂+1/2O₂→H₂Oにするなら2eが基本です
なら-237kj/mol=-2×96500C/mol×EよりE≒1.23V

答え 5
水180g=10molとグルコース0.1molなので全部で10.1molありますね
なら水の蒸気圧は10/10.1×3.17≒3.14kPaです

答え 2
ブラウン運動は衝突によるものです

答え 4
窒素が2240/22.4=100molあるということは2800あるということで、2800/0.800=3500cm³=3.5Lということです

答え 3
凝固点は②③の部分の直線を左に伸ばしたときの放物線(直線?)との交点です
定義なのでそう思ってください

答え 5
ランベルトベールはどちらかというと濃度でよく出てきます
透過率はI/I₀(=50%)なので、これとランベルトベールの法則で
0.5=e^(-kct), 0.5=e^(-2kc't)としてc'=c/2が導かれます

答え 2
久々の混成軌道
エチレンなんて二重結合もないしsp₃です
2,4以外は二重化三重結合なので除外
4は平面で実はsp₂なので2が答えです

答え 3
ただの弱酸です。
CH₃COOHが弱酸なのでCH₃COOH⇆CH₃COO⁻+H⁺の反応は完全に進みません。[H⁺]=xなら[CH₃COO⁻]=xで、[CH₃COOH]=0.10-xなので、
Ka=[CH₃COO⁻][H⁺]/[CH₃COOH]に代入して10^(-4.8)=x²/(0.10-x)ですが、
0.10-xは実質0.10とみなせば10^(-5.8)=x²なのでx=10^(-2.9)です
じゃあpH=2.9となります

答え 3
沸点上昇と凝固点降下は質量モル濃度が大きければ大きいです
1,2,5は電離しないので元が1なら1ですが、3はCa(NO₃)₂→Ca²⁺+2NO₃⁻で4はNaCl→Na⁺+Cl⁻なので3の方がモル数が多くなる(2倍になる)というので3が答えです 3倍じゃないよ

答え 1
もはや知識ですがアルブミンはたんぱく質です

答え 1
プランク定数はJ・s
令和3年

答え 5
第1条 この法律は、環境の保全について、基本理念を定め、並びに国、地方公共団体、事業者及び国民の責務を明らかにするとともに、環境の保全に関する施策の基本となる事項を定めることにより、環境の保全に関する施策を総合的かつ計画的に推進し、もって現在及び将来の国民の健康で文化的な生活の確保に寄与するとともに人類の福祉に貢献することを目的とする。

答え 2
第4条 都道府県は、当該都道府県の区域のうちに、その自然的、社会的条件から判断して、ばいじん又は有害物質に係る前条第一項又は第三項の排出基準によつては、人の健康を保護し、又は生活環境を保全することが十分でないと認められる区域があるときは、その区域におけるばい煙発生施設において発生するこれらの物質について、政令で定めるところにより、条例で、同条第一項の排出基準にかえて適用すべき同項の排出基準で定める許容限度よりきびしい許容限度を定める排出基準を定めることができる。

答え 4
第5条の3 前条第1項の指定ばい煙総量削減計画は、当該指定地域について、第1号に掲げる総量を第3号に掲げる総量までに削減させることを目途として、第1号に掲げる総量に占める第2号に掲げる総量の割合、工場又は事業場の規模、工場又は事業場における使用原料又は燃料の見通し、特定工場等以外の指定ばい煙の発生源における指定ばい煙の排出状況の推移等を勘案し、政令で定めるところにより、第4号から第6号までに掲げる事項を定めるものとする。この場合において、当該指定地域における大気の汚染及び工場又は事業場の分布の状況により計画の達成上当該指定地域を二以上の区域に区分する必要があるときは、第1号から第3号までに掲げる総量は、区分される区域ごとのそれぞれの当該指定ばい煙の総量とする。
1 当該指定地域における事業活動その他の人の活動に伴つて発生し、大気中に排出される当該指定ばい煙の総量
2 当該指定地域におけるすべての特定工場等に設置されているばい煙発生施設において発生し、排出口から大気中に排出される当該指定ばい煙の総量
3 当該指定地域における事業活動その他の人の活動に伴つて発生し、大気中に排出される当該指定ばい煙について、大気環境基準に照らし環境省令で定めるところにより算定される総量
4 第二号の総量についての削減目標量(中間目標としての削減目標量を定める場合にあつては、その削減目標量を含む。)
5 計画の達成の期間
6 計画の達成の方途
3 都道府県知事は、前条第1項の指定ばい煙総量削減計画を定めようとするときは、あらかじめ、第1項第4号及び第5号に係る部分について、環境大臣に協議しなければならない。

答え 5
第1条 この法律は、工場及び事業場から公共用水域に排出される水の排出及び地下に浸透する水の浸透を規制するとともに、生活排水対策の実施を推進すること等によつて、公共用水域及び地下水の水質の汚濁(水質以外の水の状態が悪化することを含む。以下同じ。)の防止を図り、もつて国民の健康を保護するとともに生活環境を保全し、並びに工場及び事業場から排出される汚水及び廃液に関して人の健康に係る被害が生じた場合における事業者の損害賠償の責任について定めることにより、被害者の保護を図ることを目的とする。

答え 1
ベンゼンは22、ポリ塩化ビフェニルは8、トリクロロエチレンは9、ジクロロメタンは11
ヒドラジンが対象外なのは前に出た通り


答え 2
内容はよくわかりませんが、n₁=1のときのλの最大値を求めたらいいらしい。n₂=n₁+1=2ならn₂=n₁+2=3のときよりλが大きそうなのでこれで計算すると1/λ=1.0×10⁷(1/1-1/4)よりλ≒130nmになります。なんだろうこれ

答え 4
やや抽象的な問題 環境計量士でよく出てくる等量混ぜたら濃度が半分ということで、混ぜた直後に[M]は0.02÷2=0.01でしたが、完全に反応しないらしいです。求める[M]がxなら反応自体は0.01-xだけ起きたということになります。であれば[ML]=0.01-xで、[L]=0.04÷2-(0.01-x)=0.01+xです
あとはKに代入するとx≒1×10⁻¹⁰です

答え 3
CH₃COOH⇆CH₃COO⁻+H⁺と
CH₃COO⁻+H₂O⇆CH₃COOH+OH⁻の話
式を見てればわかるのですがKaKb=[H⁺][OH⁻]=1×10⁻¹⁴なのでKa代入すればよいです。

答え 5
似たような形の酸の強さについて
基本はClの酸化数が大きいと強いので、+7になるHClO₄が強くて+3になるHClO₂が弱いです

答え 1
この中で一番反応性高いのリチウムだよねとしか言えることがない

答え 4
数えればわかりますがP-Pの結合が6個あるので200×6=1200が基本で、
式を見るとこれが1/4らしいので300です

答え 2
-olとなっているイはアルコールなので溶解度高め
ヘキサとペンタではペンタの方が炭素が少ないので比較すると溶解度が高め

答え 1
「ベンゼン環の反応」は読んだ方がよさげ
ニトロ化は求電子なのでベンゼン環に電子が豊富な方が良いです。
トルエンはCH₃のアルキル、電子供与性なものがあるので電子が豊富で反応性も高いです

答え 2
自己縮合というのは名前の通りでそのままアセトアルデヒド×2が合体したもの
CH₃C=OH+CH₃C=OH→CH₃CH(OH)-CH₂-C=OHが脱水して2のようになります

答え 5
謎の式に見えると思いますが、PV=nRT(n=1)を入れてみるとRT∫(1/P)dpになるのでRTln(p₂/p₁)=RTln10=8.31×300×2.30≒5.73kJ

答え 3
アでAgClが沈殿します。塩化鉛は微妙なところ
イでBaSO₄が沈殿します 硫酸鉛も微妙なところ
ウで水酸化鉛と水酸化鉄が沈殿します。銅はテトラアンミン銅(Ⅱ)イオンになって溶けているのでまあこれでしょう

答え 3
一次式で、100秒で1/2になるなら
1/16になるのは100×4=400秒でしょうね

答え 5
イオン化エネルギーは貴ガスが高い
希ガスは過去の言葉ですよ

答え 3
端の1/8×8と中心の1/2×6で4

答え 4
ブラッグの式は2dsinθ=nλでdが大きくなってθが大きくなったら
sinθも大きくなるのでおかしいでしょう

答え 3
エは1/1840くらいです

答え 2
フッ素は水素結合もあるので沸点が高めですね
フッ化水素は19.5℃で塩化水素は-85℃くらいです

答え 4
ダイオキシン類の名前
ベンゼン環がつながっているところが1で、左側のベンゼン環の右上Clが2です。その横に見ていくと2,3,4まではわかりますね
右側のベンゼン環は2'がないけど3'と4'があるので4が答え
左右のベンゼン環で半時計、時計周りが逆になります


答え 2
とりあえずチオ硫酸ナトリウムがCV[mmol]あり、ヨウ素はチオ硫酸ナトリウムの1/2なので2つ目の式で反応したヨウ素はCV/2[mmol]です
1つ目の式ではヨウ素酸カリウムとヨウ素が1:3なのでヨウ素酸カリウムだとCV/6[mmol]です。これが100mLらしいのでCV/600[mol/L]ですね

答え 1
ルシャトリエって覚えてますかね
ア 圧力が増えたらmol数の少ない右へ平衡が移動します
イ 発熱反応なので温度が上がれば左
ウ アンモニアが減ればそりゃ増える方向の右
エ 特に影響ありません
オ 反応は早くなりそうですね
令和4年

答え 5
そのまま

答え 4
第2条の2 法第2条第4項の政令で定める物質は、次に掲げる物質とする。
1 メタン
2 クロロジフルオロメタン(別名HCFC-22)
3 2-クロロ-1,1,1,2-テトラフルオロエタン(別名HCFC-124)
4 1,1-ジクロロ-1-フルオロエタン(別名HCFC-141b)
5 1-クロロ-1,1-ジフルオロエタン(別名HCFC-142b)
6 3,3-ジクロロ-1,1,1,2,2-ペンタフルオロプロパン(別名HCFC-225ca)
7 1,3-ジクロロ-1,1,2,2,3-ペンタフルオロプロパン(別名HCFC-225cb)
8 1,1,1,2,3,4,4,5,5,5-デカフルオロペンタン(別名HFC-43-10mee)

答え 5
第1条 この法律は、工場及び事業場における事業活動並びに建築物等の解体等に伴うばい煙、揮発性有機化合物及び粉じんの排出等を規制し、水銀に関する水俣条約(以下「条約」という。)の的確かつ円滑な実施を確保するため工場及び事業場における事業活動に伴う水銀等の排出を規制し、有害大気汚染物質対策の実施を推進し、並びに自動車排出ガスに係る許容限度を定めること等により、大気の汚染に関し、国民の健康を保護するとともに生活環境を保全し、並びに大気の汚染に関して人の健康に係る被害が生じた場合における事業者の損害賠償の責任について定めることにより、被害者の保護を図ることを目的とする。

答え 2
ホルムアルデヒドは1, ヒロドキシルアミンは3, 塩化水素は5, アクリロニトリルは7


答え 5
第14条の4 事業者は、この章に規定する排出水の排出の規制等に関する措置のほか、その事業活動に伴う汚水又は廃液の公共用水域への排出又は地下への浸透の状況を把握するとともに、当該汚水又は廃液による公共用水域又は地下水の水質の汚濁の防止のために必要な措置を講ずるようにしなければならない。

答え 4
ひっくり返すというかnmとcmの問題
5000nm=5000×10⁻⁷cm=5×10⁻⁴cmなので1/(5×10⁻⁴)で2000cm⁻¹

答え 5
放射性物質系はあまり出ないし詳しくは書きません
原子番号が1つ増えるのでPがSになります

答え 2
AgClができて[Ag⁺]=[Cl⁻]になるように電離するので、溶解度積から1×10⁻⁵

答え 1
10℃なら[H⁺]=1.0×10⁻⁷より[OH⁻]は1.0×10^(-7.54)で定義から酸性
40℃なら逆ですね

答え 2
ア 水酸化アルミニウムの白色沈殿の話
イ 同上
ウ 別にみょうばんは塩基性ではない
エ カリウムの赤紫が見えますね

答え 3
気合で数える
六角形の中のCが24個でKは中心が1ですが他の6つは1/3(120°)なので1/3×6=2
3:24なら1:8ですね

答え 1
1はCH₃, H, OH, ベンゼン環の4つがついてる不斉炭素があります

答え 3
まあ言われてもわからんわなというような問題
ケト形とエノール形だとケト形が多いというのが基本なのですが、
アセチルアセトンだけはエノール形が多いとして紹介されることが多いです

答え 3
CH₃-C(OH)H-CH₂-CH₂-CH₃を脱水するとCH₃-CH=CH-CH₂-CH₃

答え 5
xA+yB→Cのときの反応速度はk(定数)×[A]^x[B]^yなので代入してみる
1.0×10⁻³=k×0.10^x×0.10^y
2.0×10⁻³=k×0.10^x×0.20^y
1.6×10⁻²=k×0.20^x×0.20^y
少しめんどくさいですが割り算していくとx=3, y=1になります

答え 1
とりあえず代入してみると-log(1/100)=ε×5.0×10⁻²×l
10%なら-log(1/10)=εClなのでこれに代入してみるとC=2.5×10⁻²です

答え 1
自由エネルギーの式が与えられていますが、足し算するときは⊿G=xA⊿GA
+xB⊿GBのようにモル分率をかけてから足すというのを知らないと解けません。
今回は等量なのでxA=xB=0.5です。
なので⊿G=0.5⊿GA+0.5⊿GB=0.5RTln0.5=-0.5×8.31×300×0.693≒-1728J

答え 2
Aが1/8×8+1/2×6=4個
Bが8個で1:2

答え 4
低温になれば分子間の相互作用の影響を受けるので理想気体からは遠のきます

答え 2
代入してみます。半減ということは濃度はC₀/2なので
1/2=e^(-kt)です。じゃあt=ln2/k=0.693/(7.0×10⁻²)≒10分です

答え 4
LiがLi⁺になるとHeと同じであって、Neと同じとは思いませんね

答え 5
PV=nRTに入れるだけ
とりあえず1Lなら1000cm³なので、0.13g/cm³より130gで、130/4.0=32.5molなので、V=32.5×0.082×300≒800L

答え 5
酸化数はHが+1, Oが-2を基本にして計算します。ただ過酸化水素のときはOが-1になること、Hはたまに-1になることを覚えておくといいですね
1は-1, 2は+1, 3は-1, 4は-1, 5は+7

答え 2
J=Nm=kgm²/s²

答え 4
フッ化水素酸は弱酸ですよ
令和5年

答え 4
第16条 政府は、大気の汚染、水質の汚濁、土壌の汚染及び騒音に係る環境上の条件について、それぞれ、人の健康を保護し、及び生活環境を保全する上で維持されることが望ましい基準を定めるものとする。

答え 3
第2条
3 物の燃焼、合成、分解その他の処理(機械的処理を除く。)に伴い発生する物質のうち、カドミウム、塩素、弗化水素、鉛その他の人の健康又は生活環境に係る被害を生ずるおそれがある物質(第1号に掲げるものを除く。)で政令で定めるもの

答え 3
第6条 法第三条第三項の政令で定める限度は、硫黄酸化物については第一号、ばいじんについては第2号に掲げるとおりとする。
1 大気中における含有率の1時間値(以下この条において単に「1時間値」という。)の1日平均値百万分の0.04。ただし、一時間値の一日平均値百万分の0.04以上である日数が年間7日を超えない場合を除く。
2 大気中における量の年間平均値1立方メートルにつき0.15ミリグラム

答え 2
シアン化合物は2, テトラクロロエチレンは10、六価クロム化合物は5、四塩化炭素は12


答え 1
第3条
3 都道府県は、当該都道府県の区域に属する公共用水域のうちに、その自然的、社会的条件から判断して、第1項の排水基準によつては人の健康を保護し、又は生活環境を保全することが十分でないと認められる区域があるときは、その区域に排出される排出水の汚染状態について、政令で定める基準に従い、条例で、同項の排水基準にかえて適用すべき同項の排水基準で定める許容限度よりきびしい許容限度を定める排水基準を定めることができる。

答え 5
α壊変はHeが飛び出るので質量は-4, 陽子は-2
β壊変は中性子が陽子になるので質量は不変で陽子は+1

答え 3
HA⇆H⁺+A⁻で[H⁺]=[A⁻]なことを思えばKa=[H⁺][A⁻]/[HA]=[H⁺]²/[HA]です
1.0×10⁻⁵=[H⁺]²/0.10より[H⁺]²=1.0×10⁻⁶でpH=-log[H⁺]=-1/2×(-6)=3です

答え 5
十酸化四りんは乾燥剤なので水に入れません。

答え 1
この対称形で奇数にはならんやろという発想
+2が正解です

答え 1
両方正です。
というかイオン化エネルギー(電子を無限遠に飛ばすために必要なエネルギー)が負というのはまずないと思う

答え 1
たびたび出てくる酸塩基の強さ
アルキルは電子を供与するけどベンゼン環は電子を吸引します
なのでHが出ていきやすくなるイの方がアより酸性が強い=アの方が塩基性が強い
ウはこの真ん中くらいでエのニトロ基は電子吸引なのでもっと塩基が弱いです
結果まとめると1になる
答え 2
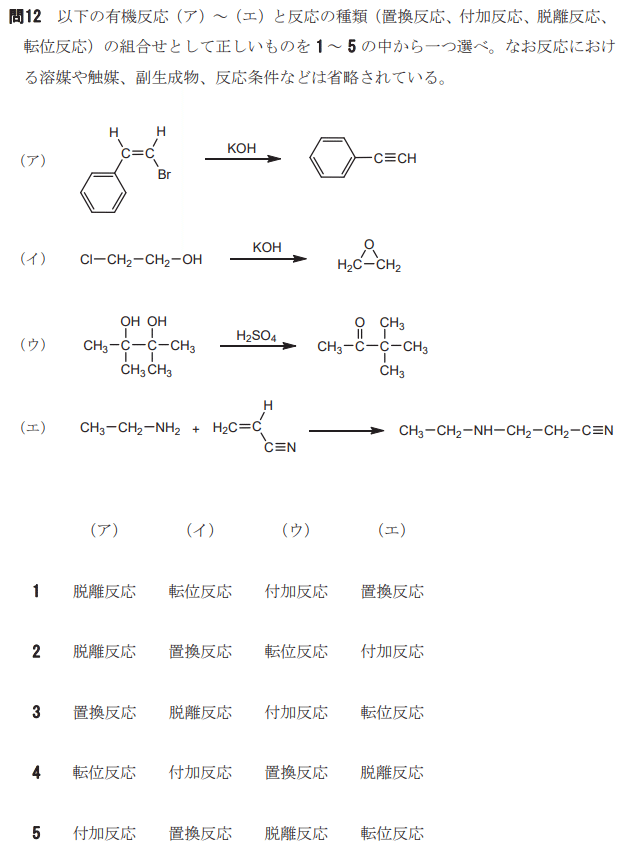
ア HBr消えたし脱離だろう
イ ClがOに代わる置換です
ウ 脱水なのですが、実は転移反応が関係しています
エ 見たまま付加です

答え 2
Grignard試薬ですね C₆H₅にCO₂がついて、そのC₆H₅COOに何がつくってHClのHなのでC₆H₅COOHの安息香酸

答え 2
抽出係数Kは(ヘキサン中のA/ヘキサン量)/(水中のA/水量)で、これは(0.80/100)/(0.40/100)=2.0です。これが変わらないというのが分配の法則
2回抽出する場合の1回目の抽出でx抽出できるとすると
2.0 = (x/50) / ((1.20-x)/100)よりx=0.60gです。
2回目をyとすると2.0=(y/50)/((0.60-y)/100)より=0.30gで足すと0.90gです

答え 5
⊿G=⊿H-T⊿Sという式があります。
今回気相から固相というので秩序だった方向への変化ですからエントロピーは負です。
そして温度が変わらないは普通⊿Gは負なので、⊿Hも負になります。

答え 4
I=12W/0.6V=20Aで16分なら20×16×60=19200C
これが9.6×10⁴×M[mol]に等しいならM=0.2molで、22.4をかけると4.48L
H₂→2H⁺+2e⁻で水素1で電子2なので水素的には4.48/2=2.24

答え 2
三平方の定理を二回使います。要は中心の原子から立方体の頂点までの距離が分かればよいので、√((a/2)²+(a/2)²)=a/√2より√((a/2)²+(a/√2)²)=√3a/2
これが原子間の距離になるので、半径は半分の√3a/2

答え 4
理想気体だとそうですが、実際の気体だと相互作用的なところで少しずれます

答え 5
π結合は基本二重結合以上でしか出てきません
そして手の数を考えると他と共有結合はできないので水素結合ということで5になります。まあイウだけでも解けはする

答え 1
ちょうどいい説明があったのでどうぞ
https://junkchem.sakura.ne.jp/chem2/chem2_52.htm

答え 4
数えようという話
まずCH₂=CH₂で¹²Cのみの場合と¹²C¹³Cの組の場合と¹³Cのみの場合の3つあり、分子量が30なので¹²CのみならDが2個Hが2個です。
付き方はどちらかに偏るパターンと1個ずつ付くパターンでシストランスを考慮して3つあります
組の場合はDが1個で¹²C¹³Cのどちらかにつくしかないので2つ
¹³CはHしかないのでその1つで合計6つでした

答え 4
しゅう酸って(COOH)₂って書くのが普通だよなと思います
なんであれ分子量90なので二水和物なら126です
6.3mgなら6.3/126=0.05mmolです
で過マンガン酸カリウムとしゅう酸は2:5らしいので過マンガン酸カリウム
2.0×10⁻³×x[mL]×5=0.05×2ならx=10mLです
一応書きますが過マンガン酸カリウム2でしゅう酸が5ということは
例えば10mL:25mLみたいになってるということで
10×5=25×2ですからね

答え 3
ア 普通二重結合三重結合になると結合距離は短くなります
イ じゃないと数あいませんからね
ウ アルコールは参加したらアルデヒド
エ はい

答え 4
1,5は酸化剤 2,3は還元剤

答え 3
縮合重合は付加重合と違って重合時に何かとれるもの
PETは水が抜けます
